浓硫酸的性质实验 知识点题库
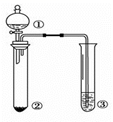
某同学设计如图装置来检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物.下列说法正确的是( )

某化学兴趣小组设计如图所示装置来检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物.下列说法不正确的是( )

用右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应的产物,下列有关说法正确的是( )


-
(1) 装置中盛浓硫酸的仪器名称是;实验过程中大玻璃管内无水硫酸铜表面的现象是;图中4个洗气瓶装有的试剂请从下列药品中选择:澄清石灰水;酸性高锰酸钾溶液;品红溶液;(可重复选用)试指出各洗气瓶内试剂名称①,②,③,④.
-
(2) 检验所得产物含SO2的实验现象为
-
(3) 检验所得产物含CO2的实验现象为.
-
(4) 写出木炭和浓硫酸反应的化学方程式.
a | b | 实验现象预期 | 结论 | |
A | 铜丝 | 浓硝酸 | 试管c中有大量红棕色气体 | 硝酸有强氧化性 |
B | 木条 | 18.4mol/L硫酸 | 木条变黑 | 浓硫酸有酸性及氧化性 |
C | 生铁 | NaCl溶液 | 导管处发生倒吸 | 生铁发生吸氧腐蚀 |
D | 铁丝 | 含少量HCl的H2O2溶液 | 试管c中有大量无色气体 | 该反应中铁作催化剂 |

请回答下列问题:
-
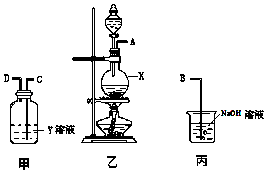
(1) 仪器X的名称为.
-
(2) Y溶液可以是,相应的实验现象是.
-
(3) 丙装置的作用是.写出丙装置中反应方程式
-
(4) 写出铜与浓硫酸反应方程式.

-
(1) 若在烧瓶中放入1.30g锌粒,与c mol/L H2SO4反应,为保证实验结论的可靠,量气管的适宜规格是 .A . 200mL B . 400mL C . 500mL
-
(2) 若1.30g锌粒完全溶解,测得盛氢氧化钠溶液的洗气瓶增重1.28g,则圆底烧瓶中发生反应的化学方程式为:.
-
(3) 若烧瓶中投入a g锌且完全反应,氢氧化钠洗气瓶增重b g量气管中收集到VmL气体,其依据得失电子守恒的原理,可得出a、b、V之间的关系为:是.
-
(4) 若在烧瓶中投入d g锌,再加入VL c mol/L 浓硫酸,充分反应后锌有剩余,测得盛氢氧化钠溶液的洗气瓶增重m g,则整个实验过程产生的混和气体中H2和SO2物质的量之比
 =(用含字母的代数式表示).若撤走盛有无水氯化钙的U型管,
=(用含字母的代数式表示).若撤走盛有无水氯化钙的U型管,  的比值将(填偏大、偏小或无影响)
的比值将(填偏大、偏小或无影响)

-
(1) 【实验探究】
木炭与浓硫酸反应的化学方程式:C+2H2SO4(浓)═CO2↑+2SO2↑+2H2O,其中浓H2SO4所起的作用是(填“氧化剂”或“还原剂”).若有0.2mol的H2SO4完全参加反应,则消耗碳的质量是g,(碳的摩尔质量为12g•mol﹣1)同时产生的CO2的体积是(标况下)L
-
(2) A装置中品红溶液颜色(填“褪色”或“不褪色”),证明含有气体.
-
(3) B装置的作用是列用足量的酸性高锰酸钾溶液除尽SO2气体.
C装置中的澄清石灰水是用来检验CO2气体,现象是产生沉淀(填“白色”或“黄色”).
-
(4) 【实验讨论】
有同学对B装置能否除尽SO2气体有有疑义,你认为应该在B、C装置之间连接右图中装置,以确定SO2是否除尽.
-
(5) 【联系实际】
煤和石油的燃烧过程中都有二氧化硫和二氧化碳排放,其中二氧化硫造成的环境影响主要是,二氧化碳造成的环境影响主要是.(每空格只填一个选顼)
A.酸雨 B.破坏臭氧层 C.温室效应
-
(6) 目前,发展低碳经济、倡导低碳生活成为国民的共识.请你举一个体现低碳理念的事例.
实验目的 | 实验方法 | |
A | 确认Fe(OH)3胶体是否制备成功 | 用可见光束照射 |
B | 确认铜与浓硫酸反应生成CuSO4 | 向反应后混合液中加水 |
C | 确认钠与水反应生成NaOH | 向反应后混合液中滴加酚酞 |
D | 确认Cl2无漂白作用 | 将有色纸条放入干燥Cl2中 |
| 操作 | 结论 | |
| A | 将火柴梗伸入溶液中 | 变黑者为浓硫酸 |
| B | 加入金属铝片 | 产生刺激性气味者为稀硫酸 |
| C | 分别加入到盛水的试管中 | 放热者为浓硫酸 |
| D | 加到CuSO4·5H2O晶体中 | 变白者为浓硫酸 |
| 选项 | 实 验 操 作 | 现 象 | 解 释 或 结 论 |
| A | 过量的Fe粉中加入稀HNO3 , 充分反应后,滴入KSCN溶液 | 溶液呈 红色 | 稀HNO3将Fe氧化为Fe3+ |
| B | 将少量浓硫酸滴入浓盐酸中 | 大量气体产生 | 硫酸的酸性比盐酸强 |
| C | 向蔗糖晶体中滴入几滴浓硫酸 | 白色固体变为黑色海绵状,有气体放出 | 说明浓硫酸有吸水性、氧化性 |
| D | 常温下,Fe、Al放入浓HNO3或浓H2SO4中 | 无明显 现象 | Fe、Al与浓HNO3或浓H2SO4发生钝化 |
| 选项 | 实验操作和现象 | 结论 |
| A | 某溶液 | 原溶液中一定含有CO32- |
| B | 用湿润的pH试纸测某碱液的pH,测定值偏小 | 湿润的pH试纸测量任何溶液都会产误差 |
| C | 将浓硫酸倒入蔗糖中搅拌蔗糖迅速变黑并伴有刺激性气味 | 浓硫酸具有脱水性和强氧化性 |
| D | 将乙烯和苯分别加入到溴水中,都能使溴水层褪色 | 乙烯和苯分子中都含有碳碳双键 |
| 选项 | ① | ② | ③ | 实验结论 | |
| A | 稀盐酸 | CaCO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si | |
| B | 浓硫酸 | 蔗糖 | Ba(NO3)2溶液 | 验证SO2与可溶性钡盐可生成白色沉淀 | |
| C | 浓氨水 | 生石灰 | 酚酞溶液 | 氨气的水溶液呈碱性 | |
| D | 浓硝酸 | Fe | NaOH溶液 | 铁和浓硝酸反应可生成NO2 |
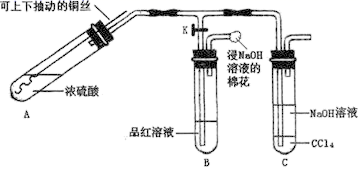
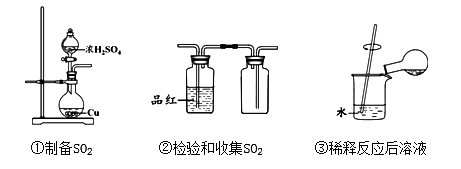
实验步骤与现象如下:
①检查装置气密性,向A中加入5 mL浓硫酸,打开K,将铜丝伸入浓硫酸中,给A处加热,观察到B中品红溶液褪色,再关闭K。
②实验观察到A中液面下铜丝变黑,产生气泡,液面上方产生大量白雾,一段时间后溶液中有白色固体出现,拉出铜丝,停止加热。回答下列问题:
-
(1) 溶液中白色固体是(填化学式),C中CCl4的作用是。
-
(2) 取出铜丝,用蒸馏水洗净后伸入到稀硫酸中,铜丝变亮、溶液变蓝。写出A中可能发生反应的化学方程式:、。
-
(3) 分离出C中的上层液体,滴加过量稀盐酸和BaCl2溶液,有白色沉淀产生。
①分离的操作名称为::
②白色沉淀为:;
③产生白色沉淀的原因可能是。
 CO2↑+2SO2↑+2H2O]的生成产物。下列说法正确的是( )
CO2↑+2SO2↑+2H2O]的生成产物。下列说法正确的是( ) 
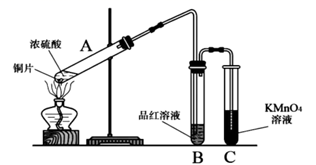
-
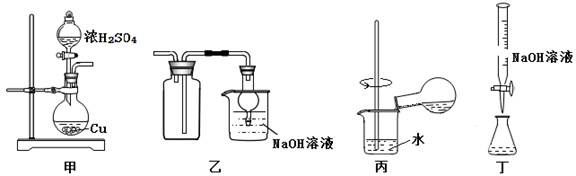
(1) 装置A中发生的化学反应方程式为。
-
(2) 实验过程中装置C中溶液褪色说明装置A中产生的气体具有性。
-
(3) 实验结束拆开装置后,加热装置B的试管,观察到的现象是。
-
(4) 实验结束后,发现试管A中底部出现了白色固体,设计实验方案检验该固体中含有CuSO4。
-
(5) 将6.4 g铜片加入到盛有含0.2mol H2SO4的浓H2SO4试管中加热,充分反应后,铜片有剩余,原因是。
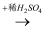 生成使石灰水变浑浊的无色气体
生成使石灰水变浑浊的无色气体