物质检验实验方案的设计 知识点题库
将盛有H2O2溶液和氨水混合液的三颈烧瓶置于冷水浴中,在搅拌下滴入CaCl2溶液,析出固体CaO2·8H2O。对所得固体过滤,用5mL无水乙醇洗涤2  3次,转移至坩埚于烘箱内105℃下脱水干燥,冷却后称重,得产品CaO2。回答下列问题:
3次,转移至坩埚于烘箱内105℃下脱水干燥,冷却后称重,得产品CaO2。回答下列问题:
-
(1) 仪器A的名称为:;恒压分液漏斗的导管a的作用为。
-
(2) 三颈烧瓶中发生反应的化学方程式为;将三颈烧瓶置于冷水浴中,其主要目的为。
-
(3) 用无水乙醇代替水洗涤的目的是:;判断脱水干燥是否完全,需要至少冷却后称重次。
-
(4) 过氧化钙纯度的测定,装置如下图所示:

检查装置气密性后,精确称取m g过氧化钙样品加入试管中,调整甲管内液面读数在0-1mL之间,并与乙管的液面相平,记下甲管内液面的初读数V1mL。加热,过氧化钙逐渐分解放出氧气,完全分解,停止加热冷却至室温后,使甲乙两管的液面相平,记下甲管内液面的终读数V2mL,设在此温度和压强下气体摩尔体积为VmL·mol-1 , 则样品中CaO2的质量分数为%。
-
(5) 过氧化钙用于长途运输鱼苗,可能的原因是。

已知:溶解度表:
Li2CO3 | LiOH | LiI | |
0℃ | l.54g | 12.7g | 151g |
100℃ | 0.72g | 13.6g | 179g |
回答下列问题:
-
(1) 由滤液1到沉淀1反应的离子方程式为。
-
(2) 向滤渣1加入H2SO4、H2O2混合溶液时,磷酸铁锂溶解,反应的离子方程式为。
-
(3) 对滤渣1酸浸操作,下列实验条件控制正确的是(填字母代号) 。
a.加入H2O2溶液适当过量,有利于滤渣1的转化
b.适当提高硫酸溶液浓度并搅拌
c.用HNO3代替所加H2SO4和H2O2 , 节约药品更环保
-
(4) 滤液2加氨水时,调节pH=3,此时溶液中c(Fe3+)= (常温下,Ksp[Fe(OH)3]=4.0×10-38)。
-
(5) 向滤液3中加入物质X,根据溶解度表判断X可能是: (填Na2CO3、NaOH或Nal)。
-
(6) 对沉淀3进行洗涤操作,应选择(选填“冷水”或“热水”)进行洗涤。
-
(7) 磷酸铁锂电池的工作原理为:LiFePO4+ 6C
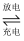 Li1-xFePO4 +LixC6 , 电池中的电解质可传导Li+。放电时正极的电极反应式为。
Li1-xFePO4 +LixC6 , 电池中的电解质可传导Li+。放电时正极的电极反应式为。
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 海带通过灼烧、水溶、过滤,在滤液中依次滴加稀硫酸、H2O2、淀粉溶液 | 溶液变蓝 | 海带含碘单质 |
| B | 向Ba(NO3)2溶液中通入SO2气体 | 产生白色沉淀 | SO2具有还原性 |
| C | 将盐酸滴入NaHCO3溶液 | 有气泡产生 | 氯的非金属性比碳强 |
| D | 将少量浓硝酸分多次加入盛有Cu和稀硫酸的试管中 | 管口产生红棕色气体 | 硝酸的还原产物是NO2 |
![]()
-
(1) 锌锰干电池的负极材料是(填化学式)。
-
(2) 第I步操作得滤渣的成分是;第II步在空气中灼烧的目的除了将MnOOH转化为MnO2外,另一作用是。
-
(3) 步骤I中制得MnSO4溶液,该反应的化学方程式为。用草酸(H2C2O4)而不用双氧水(H2O2)作还原剂的原因是。
-
(4) 已知:MnCO3难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解; Mn(OH)2开始沉淀时pH为7.7。
第IV步多步操作可按以下步骤进行:
操作l:加入NH4HCO3溶液调节溶液pH<7.7,充分反应直到不再有气泡产生;
操作2:过滤,用少量水洗涤沉淀2~3次;
操作3:检测滤液;
操作4:用少量无水乙醇洗涤2~3次;
操作5:低温烘干。
①操作1发生反应的离子方程式为;若溶液pH>7.7,会导致产品中混有(填化学式)。
②操作3中,检测MnCO3是否洗净的方法是。
③操作4用少量无水乙醇洗涤的作用是。
-
(1) 采用装置A,在高温下x克钢样中碳、硫转化为CO2、SO2。

①气体a的成分是。
②若钢样中硫以FeS形式存在,A中反应:3FeS+5 O2
 1+3。
1+3。 -
(2) 将气体a通入测硫酸装置中(如右图),采用滴定法测定硫的含量。
①H2O2氧化SO2的化学方程式:。
②用NaOH溶液滴定生成的H2SO4 , 消耗z mLNaOH溶液,若消耗1mLNaOH溶液相当于硫的质量为y克,则该钢样中硫的质量分数:。
-
(3) 将气体a通入测碳装置中(如下图),采用重量法测定碳的含量。


①气体a通过B和C的目的是。
②计算钢样中碳的质量分数,应测量的数据是。
| 实验目的 | 实验操作 | |
| A | 验证乙烯能被酸性高锰酸钾溶液氧化 | 将乙醇与浓硫酸加热到170度,反应生成的气体直接通入酸性高锰酸钾溶液,观察溶液是否褪色 |
| B | 除去溴水中的少量溴化钠 | 加入乙醇,振荡,静置,分液,取出上层液体 |
| C | 除去乙酸乙酯中混有的少量乙酸 | 加入足量饱和Na2CO3溶液,振荡,静置,分液,取出上层液体 |
| D | 检验蔗糖的水解产物 | 取少量蔗糖溶液,与稀硫酸共热后加入新制的Cu(OH)2悬浊液,观察是否出现红色沉淀 |
资料:①CH3COONH4溶液呈中性。
②Cl-对该反应几乎无影响。
|
实验 |
实验试剂 |
实验现象 |
|
1 |
5mL蒸馏水 |
反应缓慢,有少量气泡产生(经检验为H2) |
|
2 |
5mL 1.0 mol/L NH4Cl溶液(pH=4.6) |
剧烈反应,产生刺激性气味气体和灰白色难溶固体 |
-
(1) 经检验实验2中刺激性气味气体为NH3 , 检验方法是。用排水法收集一小试管产生的气体,经检验小试管中气体为H2。
-
(2) 已知灰白色沉淀中含有Mg2+、OH-。为研究固体成分,进行实验:将生成的灰白色固体洗涤数次,至洗涤液中滴加AgNO3溶液后无明显浑浊。将洗涤后固体溶于稀HNO3 , 再滴加AgNO3溶液,出现白色沉淀。推测沉淀中含有,灰白色固体可能是(填化学式)。
-
(3) 甲同学认为实验2比实验1反应剧烈的原因是NH4Cl溶液中c(H+)大,与Mg反应快。用化学用语解释NH4Cl溶液显酸性的原因是。
-
(4) 乙同学通过实验3证明甲同学的说法不合理。
实验
实验装置
3

①试剂X是 。
②由实验3获取的证据为 。
-
(5) 为进一步探究实验2反应剧烈的原因,进行实验4。
实验
实验试剂
实验现象
4
5 mL NH4Cl乙醇溶液
有无色无味气体产生(经检验为H2)
依据上述实验,可以得出Mg能与
 反应生成H2。乙同学认为该方案不严谨,需要补充的实验方案是。
反应生成H2。乙同学认为该方案不严谨,需要补充的实验方案是。 -
(6) 由以上实验可以得出的结论是。

-
(1) “操作1”的名称为。
-
(2)
 中
中 元素的化合价为。
元素的化合价为。
-
(3) “煅烧”得到
 的化学方程式为。
的化学方程式为。
-
(4) 物质
 的主要成分为(填化学式)。
的主要成分为(填化学式)。
-
(5) 预处理后的废旧电池质量为
 , 其中
, 其中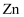 元素的质量分数为
元素的质量分数为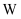 , 回收得到
, 回收得到 的质量为
的质量为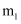 , 则
, 则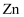 元素的回收率为(回收率
元素的回收率为(回收率 )。
)。
-
(6) 氢氧燃料电池选用
 溶液作为电解质溶液,负极的电极反应式为。
溶液作为电解质溶液,负极的电极反应式为。
选项 | 实验操作及现象 | 实验结论 |
A | 某溶液做焰色试验,若火焰颜色为黄色 | 该溶液中一定不含钾元素 |
B | 向某溶液中逐滴加入氢氧化钠溶液至过量,先无现象后产生白色沉淀,最后白色沉淀部分溶解 | 该溶液中可能含有Al3+ |
C | 向某溶液中滴入氯水无现象,再滴入KSCN溶液后溶液变红 | 该溶液中一定含有Fe2+ |
D | 向某溶液中加入盐酸酸化的BaCl2溶液,有白色沉淀生成 | 该溶液中 一定含有SO |
 溶液的试管中分别滴加相应的稀硝酸,后续实验操作及现象如下,以下相关说法不正确的是( )
溶液的试管中分别滴加相应的稀硝酸,后续实验操作及现象如下,以下相关说法不正确的是( )HNO3用量 | 少量稀硝酸 |
| 足量稀硝酸 | |||
分组 | 试管1 | 试管2 | 试管3 | 试管4 | 试管5 | 试管6 |
操作 | 加淀粉溶液 | 加KSCN溶液 | 加淀粉溶液 | 加KSCN溶液 | 加淀粉溶液 | 加KSCN溶液 |
现象 | 变蓝 | 未变红 | 变蓝 | 变红 | 变蓝 | 未变红 |
 B . 向
B . 向 溶液中滴加
溶液中滴加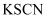 溶液,无明显现象,再滴加少量稀盐酸,溶液变红
C . 由上述实验可知:当
溶液,无明显现象,再滴加少量稀盐酸,溶液变红
C . 由上述实验可知:当 时,
时, 一定不参与反应
D . 试管6中溶液红色褪去的原因可能是稀硝酸氧化了
一定不参与反应
D . 试管6中溶液红色褪去的原因可能是稀硝酸氧化了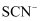
选项 | 目的 | 方案设计 | 现象和结论 |
A | 探究NO2能否支持燃烧 | 取少量浓硝酸加热分解,将产物先通入浓硫酸,后用集气瓶收集气体 | 将带火星的木条放置瓶内,木条复燃,说明NO2支持燃烧 |
B | 探究乙醇与浓硫酸反应是否生成了乙烯 | 将乙醇与浓硫酸混合加热,产生的气体通入酸性KMnO4溶液,观察颜色变化 | 溶液紫红色褪去,说明产生的气体中一定含有乙烯 |
C | 苯和液溴反应是否生成了HBr | 将少量铁粉、5mL苯和1mL液溴混合,产生的气体通入AgNO3溶液中 | 混合时液体剧烈沸腾,AgNO3溶液中产生淡黄色沉淀,苯和液溴发生反应生了HBr |
D | 探究维生素C的还原性 | 向盛有2mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化 | 黄色溶液变为浅绿色,说明生素C具有还原性 |
目的 | 方案设计 | |
A | 检验乙炔具有还原性 | 将饱和食盐水滴入盛有电石的锥形瓶中,将产生的气体导入酸性高锰酸钾溶液,观察溶液颜色变化 |
B | 比较HClO与 | 常温下,分别用玻璃棒蘸取 |
C | 除去粗苯甲酸样品中少量氯化钠和泥沙 | 取一定量样品加入适量的水,加热充分溶解,趁热过滤,冷却结晶,过滤,用少量蒸馏水洗涤所得晶体 |
D | 验证 | 向盛有 |
 与足量的10mol/L硫酸混合微热,产生下列现象:①有红色金属生成;②产生刺激性气味的气体;③溶液呈现蓝色。据此判断下列说法正确的是( )
与足量的10mol/L硫酸混合微热,产生下列现象:①有红色金属生成;②产生刺激性气味的气体;③溶液呈现蓝色。据此判断下列说法正确的是( )
 完全反应转移0.5 mol电子
完全反应转移0.5 mol电子
|
|
实验目的 |
仪器 |
试剂 |
|
A |
检验SO |
试管、胶头滴管 |
BaCl2溶液、稀硝酸、待检溶液 |
|
B |
检验Na+的存在 |
烧杯、酒精灯、洁净的铁丝、火柴 |
盐酸待检溶液 |
|
C |
MnO2在H2O2分解时作催化剂 |
酒精灯、漏斗、短导管、木条 |
MnO2、10%的H2O2 |
|
D |
验证苯环不是单双键交替结构 |
分液漏斗 、烧杯、铁圈、铁架台 |
苯、溴水、酸性高锰酸钾溶液 |
-
(1) I.制备O2
该小组同学设计了如下三套装置制备O2(部分夹持装置已省略)

甲装置中装3%H2O2溶液的仪器名称为。
-
(2) 使用乙装置制备氧气不合理的原因是。。
-
(3) 丙装置可用于制备较多O2 , 催化剂铂丝可上下移动。制备过程中如果体系内压强过大,安全管中的现象是,此时可以将铂丝抽离H2O2溶液。
-
(4) II.氧化C2H5OH
该小组同学最后选定了丙装置用于制备氧气,进一步设计氧化C2H5OH的装置如下图:

仪器b中发生反应的化学方程式为。
-
(5) C和E两个水浴作用不相同,其中C中热水的作用是。
-
(6) 在不断通入O2的情况下,熄灭酒精灯后反应仍能继续进行,说明乙醇催化氧化反应是反应(填“放热”或“吸热”)。
-
(7) III.检验产物
为检验上述实验收集到的产物,该小组同学进行了如下实验并得出相应结论。
实验序号
检验试剂和反应条件
现象
结论
①
酸性KMnO4溶液
紫红色褪去
产物含有乙醛
②
, 加热
生成砖红色沉淀
产物含有乙醛
③
微红色含酚酞的NaOH溶液
微红色褪去
产物可能含有乙酸
实验②中检验试剂是。实验①~③中的结论不合理的是(填序号),原因是。
|
|
实验目的 |
玻璃仪器 |
试剂 |
|
A |
精制含Ca2+、Mg2+、 |
胶头滴管、烧杯、试管、漏斗、玻璃棒 |
粗盐水、稀盐酸、氯化钡溶液、氢氧化钠溶液、碳酸钠溶液 |
|
B |
制备Fe(OH)3胶体 |
烧杯、酒精灯、胶头滴管 |
1mol/L氢氧化钠溶液、1mol/L氯化铁溶液 |
|
C |
确定FeCl3是否完全变质 |
试管、酒精灯、胶头滴管 |
稀硫酸、高锰酸钾溶液 |
|
D |
利用反萃取原理从碘的四氯化碳溶液中获取碘单质 |
漏斗、烧杯、玻璃棒、分液漏斗 |
稀硫酸、氢氧化钠溶液 |

-
(1) X的组成元素;X化学式。
-
(2)
 的离子方程式。
的离子方程式。
-
(3) 反应
 转化过程中,生成
转化过程中,生成 时消耗葡萄糖的质量至少g。
时消耗葡萄糖的质量至少g。
-
(4) 设计检验F溶液中溶质阴离子的实验方案。


 的酸性强弱
的酸性强弱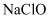 和
和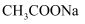 溶液点在pH试纸上,观察现象
溶液点在pH试纸上,观察现象
 溶液的试管中滴加4滴
溶液的试管中滴加4滴 溶液,振荡后,继续滴加4滴
溶液,振荡后,继续滴加4滴 溶液,观察现象
溶液,观察现象 的存在
的存在 的食盐水
的食盐水


