зҰ»еӯҗжҷ¶дҪ“ зҹҘиҜҶзӮ№
зҰ»еӯҗжҷ¶дҪ“пјҡ з”ұжӯЈгҖҒиҙҹзҰ»еӯҗжҲ–жӯЈгҖҒиҙҹзҰ»еӯҗйӣҶеӣўжҢүдёҖе®ҡжҜ”дҫӢйҖҡиҝҮзҰ»еӯҗй”®з»“еҗҲеҪўжҲҗзҡ„жҷ¶дҪ“з§°дҪңзҰ»еӯҗжҷ¶дҪ“пјҢзҰ»еӯҗжҷ¶дҪ“еұһдәҺзҰ»еӯҗеҢ–еҗҲзү©дёӯзҡ„дёҖз§Қзү№ж®ҠеҪўејҸпјҢдёҚиғҪз§°дёәеҲҶеӯҗгҖӮејәзўұгҖҒжҙ»жіјжҖ§йҮ‘еұһж°§еҢ–зү©е’ҢеӨ§еӨҡж•°зҡ„зӣҗзұ»еқҮдёәзҰ»еӯҗжҷ¶дҪ“гҖӮ
зҰ»еӯҗжҷ¶дҪ“ зҹҘиҜҶзӮ№йўҳеә“
е…ідәҺжҷ¶дҪ“зҡ„дёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲ пјү
A . еҲҶеӯҗжҷ¶дҪ“зҡ„зҶ”зӮ№дёҚдёҖе®ҡжҜ”йҮ‘еұһжҷ¶й’өзҶ”зӮ№дҪҺ
B . зҰ»еӯҗжҷ¶дҪ“дёӯдёҖе®ҡеҗ«йҮ‘еұһйҳізҰ»еӯҗ
C . еңЁе…ұд»·еҢ–еҗҲзү©еҲҶеӯҗдёӯеҗ„еҺҹеӯҗйғҪеҪўжҲҗ8з”өеӯҗз»“жһ„
D . еҸӘиҰҒеҗ«жңүйҮ‘еұһйҳізҰ»еӯҗзҡ„жҷ¶дҪ“е°ұдёҖе®ҡжҳҜзҰ»еӯҗжҷ¶дҪ“
д»…з”ұдёӢеҲ—еҗ„з»„е…ғзҙ жүҖз»„жҲҗзҡ„еҢ–еҗҲзү©,дёҚеҸҜиғҪеҪўжҲҗзҰ»еӯҗжҷ¶дҪ“зҡ„жҳҜ(гҖҖгҖҖ)
A . H O S
B . Na H O
C . K Cl O
D . H N Cl
дёӢйқўжңүе…іжҷ¶дҪ“зҡ„еҸҷиҝ°дёӯпјҢжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү
A . еңЁж°ҜеҢ–й’ жҷ¶дҪ“дёӯжҜҸдёӘNa+пјҲжҲ–Clп№Јпјүе‘ЁеӣҙйғҪзҙ§йӮ»8дёӘClп№ЈпјҲNa+пјү
B . еҺҹеӯҗжҷ¶дҪ“дёӯеҸӘеӯҳеңЁе…ұд»·й”®
C . зҰ»еӯҗжҷ¶дҪ“е’ҢеҲҶеӯҗжҷ¶дҪ“еңЁзҶ”еҢ–ж—¶пјҢеҢ–еӯҰй”®йғҪиў«з ҙеқҸ
D . зҶ”иһҚзҠ¶жҖҒдёӢиғҪеҜјз”өзҡ„жҷ¶дҪ“дёҖе®ҡжҳҜйҮ‘еұһжҷ¶дҪ“
е…ідәҺдёӢеҲ—еҮ з§ҚзҰ»еӯҗжҷ¶дҪ“пјҢиҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜпјҲВ В пјү
A . з”ұдәҺNaCl жҷ¶дҪ“е’ҢCsClжҷ¶дҪ“дёӯжӯЈиҙҹзҰ»еӯҗеҚҠеҫ„жҜ”пјҲ  пјүдёҚзӣёзӯүпјҢжүҖд»ҘдёӨжҷ¶дҪ“дёӯзҰ»еӯҗзҡ„й…ҚдҪҚж•°дёҚзӣёзӯү
B . CaF2жҷ¶дҪ“дёӯпјҢCa2+й…ҚдҪҚж•°дёә8пјҢFп№Јй…ҚдҪҚж•°дёә4дёҚзӣёзӯүпјҢдё»иҰҒжҳҜз”ұдәҺFп№ЈгҖҒCa2+з”өиҚ·пјҲз»қеҜ№еҖјпјүдёҚзӣёеҗҢ
C . MgOзҡ„зҶ”зӮ№жҜ”MgCl2й«ҳдё»иҰҒжҳҜеӣ дёәMgOзҡ„жҷ¶дҪ“иғҪжҜ”MgCl2еӨ§
D . MCO3дёӯM2+еҚҠеҫ„и¶ҠеӨ§пјҢMCO3зғӯеҲҶи§Јжё©еәҰи¶ҠдҪҺ
пјүдёҚзӣёзӯүпјҢжүҖд»ҘдёӨжҷ¶дҪ“дёӯзҰ»еӯҗзҡ„й…ҚдҪҚж•°дёҚзӣёзӯү
B . CaF2жҷ¶дҪ“дёӯпјҢCa2+й…ҚдҪҚж•°дёә8пјҢFп№Јй…ҚдҪҚж•°дёә4дёҚзӣёзӯүпјҢдё»иҰҒжҳҜз”ұдәҺFп№ЈгҖҒCa2+з”өиҚ·пјҲз»қеҜ№еҖјпјүдёҚзӣёеҗҢ
C . MgOзҡ„зҶ”зӮ№жҜ”MgCl2й«ҳдё»иҰҒжҳҜеӣ дёәMgOзҡ„жҷ¶дҪ“иғҪжҜ”MgCl2еӨ§
D . MCO3дёӯM2+еҚҠеҫ„и¶ҠеӨ§пјҢMCO3зғӯеҲҶи§Јжё©еәҰи¶ҠдҪҺ
 пјүдёҚзӣёзӯүпјҢжүҖд»ҘдёӨжҷ¶дҪ“дёӯзҰ»еӯҗзҡ„й…ҚдҪҚж•°дёҚзӣёзӯү
B . CaF2жҷ¶дҪ“дёӯпјҢCa2+й…ҚдҪҚж•°дёә8пјҢFп№Јй…ҚдҪҚж•°дёә4дёҚзӣёзӯүпјҢдё»иҰҒжҳҜз”ұдәҺFп№ЈгҖҒCa2+з”өиҚ·пјҲз»қеҜ№еҖјпјүдёҚзӣёеҗҢ
C . MgOзҡ„зҶ”зӮ№жҜ”MgCl2й«ҳдё»иҰҒжҳҜеӣ дёәMgOзҡ„жҷ¶дҪ“иғҪжҜ”MgCl2еӨ§
D . MCO3дёӯM2+еҚҠеҫ„и¶ҠеӨ§пјҢMCO3зғӯеҲҶи§Јжё©еәҰи¶ҠдҪҺ
пјүдёҚзӣёзӯүпјҢжүҖд»ҘдёӨжҷ¶дҪ“дёӯзҰ»еӯҗзҡ„й…ҚдҪҚж•°дёҚзӣёзӯү
B . CaF2жҷ¶дҪ“дёӯпјҢCa2+й…ҚдҪҚж•°дёә8пјҢFп№Јй…ҚдҪҚж•°дёә4дёҚзӣёзӯүпјҢдё»иҰҒжҳҜз”ұдәҺFп№ЈгҖҒCa2+з”өиҚ·пјҲз»қеҜ№еҖјпјүдёҚзӣёеҗҢ
C . MgOзҡ„зҶ”зӮ№жҜ”MgCl2й«ҳдё»иҰҒжҳҜеӣ дёәMgOзҡ„жҷ¶дҪ“иғҪжҜ”MgCl2еӨ§
D . MCO3дёӯM2+еҚҠеҫ„и¶ҠеӨ§пјҢMCO3зғӯеҲҶи§Јжё©еәҰи¶ҠдҪҺ
дёӢеҲ—жҷ¶дҪ“еҲҶзұ»дёӯжӯЈзЎ®зҡ„дёҖз»„жҳҜпјҲВ В пјү
йҖүйЎ№ | зҰ»еӯҗжҷ¶дҪ“ | еҺҹеӯҗжҷ¶дҪ“ | еҲҶеӯҗжҷ¶дҪ“ |
A | NaOH | Ar | SO2 |
B | K2SO4 | зҹіеўЁ | S |
C | CH3COONa | ж°ҙжҷ¶ |
|
D | BaпјҲOHпјү2 | йҮ‘еҲҡзҹі | зҺ»з’ғ |
A . AВ
B . BВ
C . CВ
D . D
еҮ з§Қжҷ¶дҪ“зҡ„жҷ¶иғһеҰӮеӣҫжүҖзӨәпјҡ

жүҖзӨәжҷ¶иғһд»Һе·ҰеҲ°еҸіеҲҶеҲ«иЎЁзӨәзҡ„зү©иҙЁжӯЈзЎ®зҡ„жҺ’еәҸжҳҜпјҲВ В пјү
A . зўҳгҖҒй”ҢгҖҒй’ гҖҒйҮ‘еҲҡзҹі
B . йҮ‘еҲҡзҹігҖҒй”ҢгҖҒзўҳгҖҒй’
C . й’ гҖҒй”ҢгҖҒзўҳгҖҒйҮ‘еҲҡзҹі
D . й”ҢгҖҒй’ гҖҒзўҳгҖҒйҮ‘еҲҡзҹі
дёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҡпјҲ пјү
в‘ NaClжҷ¶дҪ“дёӯдёҺжҜҸдёӘNa+и·қзҰ»зӣёзӯүдё”жңҖиҝ‘зҡ„Na+е…ұжңү12дёӘ
в‘Ўеҗ«жңүе…ұд»·й”®зҡ„жҷ¶дҪ“дёҖе®ҡе…·жңүй«ҳзҡ„зҶ”гҖҒжІёзӮ№еҸҠзЎ¬еәҰ
в‘ўsпјҚs Пғй”®дёҺsпјҚp Пғй”®зҡ„з”өеӯҗдә‘еҪўзҠ¶зӣёеҗҢ
в‘Јеҗ«жңүПҖй”®зҡ„еҢ–еҗҲзү©дёҺеҸӘеҗ«Пғй”®зҡ„еҢ–еҗҲзү©зҡ„еҢ–еӯҰжҖ§иҙЁдёҚеҗҢ
в‘ӨдёӯеҝғеҺҹеӯҗйҮҮеҸ–sp3жқӮеҢ–зҡ„еҲҶеӯҗпјҢе…¶з«ӢдҪ“жһ„еҪўдёҚдёҖе®ҡжҳҜжӯЈеӣӣйқўдҪ“
в‘Ҙй…ҚдҪҚй”®еңЁеҪўжҲҗж—¶пјҢжҳҜз”ұжҲҗй”®еҸҢж–№еҗ„жҸҗдҫӣдёҖдёӘз”өеӯҗеҪўжҲҗе…ұз”Ёз”өеӯҗеҜ№
A . в‘ в‘Ўв‘Ө
B . в‘ в‘Јв‘Ө
C . в‘Ўв‘ўв‘Ө
D . в‘Ўв‘ўв‘Ҙ
ж №жҚ®иЎЁдёӯз»ҷеҮәзү©иҙЁзҡ„зҶ”зӮ№ж•°жҚ®(AlCl3жІёзӮ№дёә260 в„ғ)пјҢеҲӨж–ӯдёӢеҲ—иҜҙжі•й”ҷиҜҜзҡ„жҳҜ(гҖҖгҖҖ)
жҷ¶дҪ“ | NaCl | MgO | SiCl4 | AlCl3 | жҷ¶дҪ“зЎј |
зҶ”зӮ№/в„ғ | 801 | 2 800 | -70 | 180 | 2 500 |
A . MgOдёӯзҡ„зҰ»еӯҗй”®жҜ”NaClдёӯзҡ„зҰ»еӯҗй”®ејә
B . SiCl4жҷ¶дҪ“жҳҜеҲҶеӯҗжҷ¶дҪ“
C . AlCl3жҷ¶дҪ“жҳҜзҰ»еӯҗжҷ¶дҪ“
D . жҷ¶дҪ“зЎјжҳҜеҺҹеӯҗжҷ¶дҪ“
дёӢеӣҫжҳҜCaF2жҷ¶иғһзҡ„з»“жһ„гҖӮдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜ (гҖҖгҖҖ)

A . дёҖдёӘCaF2жҷ¶иғһдёӯеҗ«жңү8дёӘCa2+
B . дёҖдёӘCaF2жҷ¶иғһдёӯеҗ«жңү8дёӘF-
C . еңЁCaF2жҷ¶иғһдёӯCa2+зҡ„й…ҚдҪҚж•°дёә4
D . еңЁCaF2жҷ¶иғһдёӯF-зҡ„й…ҚдҪҚж•°дёә8
й’ЎеңЁж°§ж°”дёӯзҮғзғ§ж—¶еҫ—еҲ°дёҖз§Қй’Ўзҡ„ж°§еҢ–зү©жҷ¶дҪ“пјҢз»“жһ„еҰӮеӣҫжүҖзӨәпјҢжңүе…іиҜҙжі•й”ҷиҜҜзҡ„жҳҜпјҲ пјү
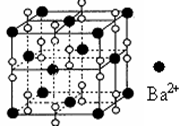
A . иҜҘжҷ¶дҪ“еұһдәҺзҰ»еӯҗжҷ¶дҪ“
B . жҷ¶дҪ“зҡ„еҢ–еӯҰејҸдёәBa2O2
C . иҜҘжҷ¶дҪ“жҷ¶иғһз»“жһ„дёҺNaClзӣёдјј
D . дёҺжҜҸдёӘBa2+и·қзҰ»зӣёзӯүдё”жңҖиҝ‘зҡ„Ba2+е…ұжңү12дёӘ
дёӢеҲ—жңүе…іжҷ¶дҪ“зҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲ пјү
A . еҲҶеӯҗжҷ¶дҪ“дёӯдёҖе®ҡдёҚеҗ«зҰ»еӯҗй”®
B . еҲҶеӯҗжҷ¶дҪ“дёӯдёҖе®ҡеҗ«жңүе…ұд»·й”®
C . зҰ»еӯҗжҷ¶дҪ“дёӯдёҖе®ҡеҸӘеҗ«зҰ»еӯҗй”®
D . зҰ»еӯҗжҷ¶дҪ“зҡ„зҶ”зӮ№дёҖе®ҡжҜ”е…ұд»·еҢ–еҗҲзү©й«ҳ
еҰӮеӣҫжҳҜд»ҺNaClе’ҢCsClжҷ¶дҪ“з»“жһ„дёӯеҲҶеүІеҮәжқҘзҡ„йғЁеҲҶз»“жһ„еӣҫпјҢе…¶дёӯеұһдәҺд»ҺNaClжҷ¶дҪ“дёӯеҲҶеүІеҮәжқҘзҡ„з»“жһ„еӣҫжҳҜпјҲ пјү
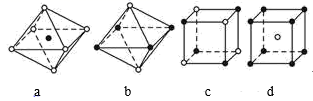
A . еҸӘжңүc
B . bе’Ңc
C . aе’Ңc
D . aе’Ңd
дёӢйқўзҡ„жҺ’еәҸй”ҷиҜҜзҡ„жҳҜпјҲ пјү
A . жІёзӮ№зҡ„й«ҳдҪҺпјҡд№ҷйҶҮпјһдёҷзғ·
B . зЎ¬еәҰз”ұеӨ§еҲ°е°ҸпјҡйҮ‘еҲҡзҹіпјһзўіеҢ–зЎ…>жҷ¶дҪ“зЎ…
C . зҶ”зӮ№з”ұй«ҳеҲ°дҪҺпјҡNa>Mg>Al
D . жҷ¶ж јиғҪз”ұеӨ§еҲ°е°ҸпјҡNaF>NaCl>NaBr>NaI
дёӢеҲ—еҸҷиҝ°й”ҷиҜҜзҡ„жҳҜ( )
A . жҹҗзү©иҙЁзҶ”иһҚзҠ¶жҖҒеҸҜеҜјз”өпјҢеӣәжҖҒеҸҜеҜјз”өпјҢе°Ҷе…¶жҠ•е…Ҙж°ҙдёӯжүҖеҪўжҲҗзҡ„ж°ҙжә¶ж¶Ід№ҹеҸҜеҜјз”өпјҢеҲҷеҸҜжҺЁжөӢиҜҘзү©иҙЁеҸӘеҸҜиғҪжҳҜйҮ‘еұһеҚ•иҙЁ
B . жҷ¶дҪ“дёӯеҸӘиҰҒжңүйҳҙзҰ»еӯҗпјҢе°ұдёҖе®ҡжңүйҳізҰ»еӯҗпјӣжңүйҳізҰ»еӯҗдёҚдёҖе®ҡжңүйҳҙзҰ»еӯҗ
C . MgOзҡ„зҶ”зӮ№жҜ”MgCl2й«ҳдё»иҰҒжҳҜеӣ дёәMgOзҡ„жҷ¶ж јиғҪжҜ”MgCl2еӨ§
D . зҰ»еӯҗжҷ¶дҪ“дёӯеҸӘеҸҜиғҪеӯҳеңЁйҳҙгҖҒйҳізҰ»еӯҗ
дёӢеҲ—жңүе…іж°ҜеҢ–й’ жҷ¶дҪ“зҡ„еҸҷиҝ°дёӯпјҢжӯЈзЎ®зҡ„жҳҜпјҲ пјү
A . ж°ҜеҢ–й’ жҷ¶дҪ“жҳҜз”ұй’ зҰ»еӯҗе’Ңж°ҜзҰ»еӯҗжһ„жҲҗзҡ„пјҢжүҖд»Ҙж°ҜеҢ–й’ жҷ¶дҪ“иғҪеҜјз”ө
B . й’ зҰ»еӯҗе’Ңж°ҜзҰ»еӯҗд№Ӣй—ҙеӣ йқҷз”өеҗёеј•иҖҢеҪўжҲҗж°ҜеҢ–й’ жҷ¶дҪ“
C . ж°ҜеҢ–й’ зҡ„еҲҶеӯҗејҸдёәNaCl
D . жҜҸдёӘй’ зҰ»еӯҗе‘Ёеӣҙеҗёеј•6дёӘж°ҜзҰ»еӯҗпјҢжҜҸдёӘж°ҜзҰ»еӯҗе‘ЁеӣҙеҗҢж ·еҗёеј•6дёӘй’ зҰ»еӯҗ
жңүе…іжҷ¶дҪ“зҡ„з»“жһ„еҰӮеӣҫжүҖзӨәпјҢдёӢеҲ—иҜҙжі•дёӯй”ҷиҜҜзҡ„жҳҜпјҲ пјү
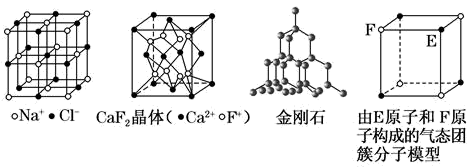
A . еңЁ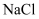 жҷ¶дҪ“дёӯпјҢи·қ
жҷ¶дҪ“дёӯпјҢи·қ жңҖиҝ‘зҡ„
жңҖиҝ‘зҡ„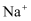 жңү6дёӘпјҢи·қ
жңү6дёӘпјҢи·қ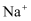 жңҖиҝ‘дё”зӯүи·қзҡ„
жңҖиҝ‘дё”зӯүи·қзҡ„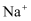 е…ұ12дёӘ
B . еңЁ
е…ұ12дёӘ
B . еңЁ жҷ¶дҪ“дёӯпјҢжҜҸдёӘжҷ¶иғһе№іеқҮеҚ жңү4дёӘ
жҷ¶дҪ“дёӯпјҢжҜҸдёӘжҷ¶иғһе№іеқҮеҚ жңү4дёӘ пјҢ
пјҢ 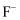 зҡ„й…ҚдҪҚж•°жҳҜ4
C . еңЁйҮ‘еҲҡзҹіжҷ¶дҪ“дёӯпјҢжҜҸдёӘзўіеҺҹеӯҗиў«12дёӘе…ӯе…ғзҺҜе…ұеҗҢеҚ жңүпјҢжҜҸдёӘе…ӯе…ғзҺҜжңҖеӨҡжңү4дёӘзўіеҺҹеӯҗе…ұйқў
D . иҜҘж°”жҖҒеӣўз°ҮеҲҶеӯҗзҡ„еҲҶеӯҗејҸдёә
зҡ„й…ҚдҪҚж•°жҳҜ4
C . еңЁйҮ‘еҲҡзҹіжҷ¶дҪ“дёӯпјҢжҜҸдёӘзўіеҺҹеӯҗиў«12дёӘе…ӯе…ғзҺҜе…ұеҗҢеҚ жңүпјҢжҜҸдёӘе…ӯе…ғзҺҜжңҖеӨҡжңү4дёӘзўіеҺҹеӯҗе…ұйқў
D . иҜҘж°”жҖҒеӣўз°ҮеҲҶеӯҗзҡ„еҲҶеӯҗејҸдёә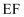 жҲ–
жҲ–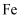 пјҢ е…¶жҷ¶дҪ“дёҚеҜјз”ө
пјҢ е…¶жҷ¶дҪ“дёҚеҜјз”ө
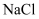 жҷ¶дҪ“дёӯпјҢи·қ
жҷ¶дҪ“дёӯпјҢи·қ жңҖиҝ‘зҡ„
жңҖиҝ‘зҡ„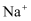 жңү6дёӘпјҢи·қ
жңү6дёӘпјҢи·қ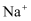 жңҖиҝ‘дё”зӯүи·қзҡ„
жңҖиҝ‘дё”зӯүи·қзҡ„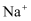 е…ұ12дёӘ
B . еңЁ
е…ұ12дёӘ
B . еңЁ жҷ¶дҪ“дёӯпјҢжҜҸдёӘжҷ¶иғһе№іеқҮеҚ жңү4дёӘ
жҷ¶дҪ“дёӯпјҢжҜҸдёӘжҷ¶иғһе№іеқҮеҚ жңү4дёӘ пјҢ
пјҢ 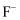 зҡ„й…ҚдҪҚж•°жҳҜ4
C . еңЁйҮ‘еҲҡзҹіжҷ¶дҪ“дёӯпјҢжҜҸдёӘзўіеҺҹеӯҗиў«12дёӘе…ӯе…ғзҺҜе…ұеҗҢеҚ жңүпјҢжҜҸдёӘе…ӯе…ғзҺҜжңҖеӨҡжңү4дёӘзўіеҺҹеӯҗе…ұйқў
D . иҜҘж°”жҖҒеӣўз°ҮеҲҶеӯҗзҡ„еҲҶеӯҗејҸдёә
зҡ„й…ҚдҪҚж•°жҳҜ4
C . еңЁйҮ‘еҲҡзҹіжҷ¶дҪ“дёӯпјҢжҜҸдёӘзўіеҺҹеӯҗиў«12дёӘе…ӯе…ғзҺҜе…ұеҗҢеҚ жңүпјҢжҜҸдёӘе…ӯе…ғзҺҜжңҖеӨҡжңү4дёӘзўіеҺҹеӯҗе…ұйқў
D . иҜҘж°”жҖҒеӣўз°ҮеҲҶеӯҗзҡ„еҲҶеӯҗејҸдёә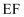 жҲ–
жҲ–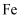 пјҢ е…¶жҷ¶дҪ“дёҚеҜјз”ө
пјҢ е…¶жҷ¶дҪ“дёҚеҜјз”ө
NH4Clзҡ„жҷ¶иғһдёәз«Ӣж–№дҪ“пјҢе…¶з»“жһ„еҰӮдёӢгҖӮдёӢеҲ—иҜҙжі•й”ҷиҜҜзҡ„жҳҜпјҲ пјү

A . NH4Clжҷ¶дҪ“еұһдәҺзҰ»еӯҗжҷ¶дҪ“
B . NH4Clжҷ¶иғһдёӯH-N-Hй”®и§’дёә90В°
C . NH4Clжҷ¶дҪ“дёӯж—ўжңүзҰ»еӯҗй”®еҸҲжңүе…ұд»·й”®
D . жҜҸдёӘCl-е‘ЁеӣҙдёҺе®ғжңҖиҝ‘дё”зӯүи·қзҰ»зҡ„  зҡ„ж•°зӣ®дёә8
зҡ„ж•°зӣ®дёә8
 зҡ„ж•°зӣ®дёә8
зҡ„ж•°зӣ®дёә8
жңүе…іжҷ¶дҪ“зҡ„з»“жһ„еҰӮеӣҫжүҖзӨәпјҢдёӢеҲ—иҜҙжі•дёӯй”ҷиҜҜзҡ„жҳҜпјҲ пјү

A . еңЁNaClжҷ¶дҪ“дёӯпјҢи·қNa+жңҖиҝ‘зҡ„Cl-еҪўжҲҗжӯЈе…«йқўдҪ“
B . еңЁCaF2жҷ¶дҪ“дёӯпјҢF-зҡ„й…ҚдҪҚж•°дёә8
C . еңЁйҮ‘еҲҡзҹіжҷ¶дҪ“дёӯпјҢзўіеҺҹеӯҗдёҺзўізўій”®дёӘж•°зҡ„жҜ”дёә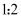 D . иҜҘж°”жҖҒеӣўз°ҮеҲҶеӯҗзҡ„еҲҶеӯҗејҸдёәEFжҲ–FE
D . иҜҘж°”жҖҒеӣўз°ҮеҲҶеӯҗзҡ„еҲҶеӯҗејҸдёәEFжҲ–FE
 D . иҜҘж°”жҖҒеӣўз°ҮеҲҶеӯҗзҡ„еҲҶеӯҗејҸдёәEFжҲ–FE
D . иҜҘж°”жҖҒеӣўз°ҮеҲҶеӯҗзҡ„еҲҶеӯҗејҸдёәEFжҲ–FE
й’ЎеңЁж°§ж°”дёӯзҮғзғ§ж—¶еҫ—еҲ°дёҖз§Қй’Ўзҡ„ж°§еҢ–зү©жҷ¶дҪ“пјҢе…¶жҷ¶иғһзҡ„з»“жһ„еҰӮеӣҫжүҖзӨәпјҢдёӢеҲ—жңүе…іиҜҙжі•дёӯй”ҷиҜҜзҡ„жҳҜпјҲ пјү

A . иҜҘжҷ¶дҪ“еұһдәҺзҰ»еӯҗжҷ¶дҪ“
B . иҜҘжҷ¶дҪ“зҡ„жҷ¶иғһз»“жһ„дёҺ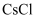 зӣёдјј
C . жҷ¶дҪ“зҡ„еҢ–еӯҰејҸдёә
зӣёдјј
C . жҷ¶дҪ“зҡ„еҢ–еӯҰејҸдёә D . жҷ¶дҪ“дёӯ
D . жҷ¶дҪ“дёӯ зҡ„й…ҚдҪҚж•°дёҺ
зҡ„й…ҚдҪҚж•°дёҺ зҡ„й…ҚдҪҚж•°д№ӢжҜ”дёә
зҡ„й…ҚдҪҚж•°д№ӢжҜ”дёә
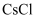 зӣёдјј
C . жҷ¶дҪ“зҡ„еҢ–еӯҰејҸдёә
зӣёдјј
C . жҷ¶дҪ“зҡ„еҢ–еӯҰејҸдёә D . жҷ¶дҪ“дёӯ
D . жҷ¶дҪ“дёӯ зҡ„й…ҚдҪҚж•°дёҺ
зҡ„й…ҚдҪҚж•°дёҺ зҡ„й…ҚдҪҚж•°д№ӢжҜ”дёә
зҡ„й…ҚдҪҚж•°д№ӢжҜ”дёә
дёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲ пјү
A . жҷ¶дҪ“еңЁеҸ—зғӯзҶ”еҢ–иҝҮзЁӢдёӯдёҖе®ҡеӯҳеңЁеҢ–еӯҰй”®зҡ„ж–ӯиЈӮ
B . еҺҹеӯҗжҷ¶дҪ“зҡ„еҺҹеӯҗй—ҙеҸӘеӯҳеңЁе…ұд»·й”®пјҢиҖҢеҲҶеӯҗжҷ¶дҪ“еҶ…еҸӘеӯҳеңЁиҢғеҫ·еҚҺеҠӣ
C . еҢәеҲҶжҷ¶дҪ“е’Ңйқһжҷ¶дҪ“жңҖ科еӯҰзҡ„ж–№жі•жҳҜеҜ№еӣәдҪ“иҝӣиЎҢXе°„зәҝиЎҚе°„е®һйӘҢ
D . йқһйҮ‘еұһе…ғзҙ зҡ„еҺҹеӯҗй—ҙеҸӘеҪўжҲҗе…ұд»·й”®пјҢйҮ‘еұһе…ғзҙ зҡ„еҺҹеӯҗдёҺйқһйҮ‘еұһе…ғзҙ зҡ„еҺҹеӯҗй—ҙеҸӘеҪўжҲҗзҰ»еӯҗй”®
жңҖиҝ‘жӣҙж–°



