吉林2018年高二化学上半期期末考试同步练习
| 1. 选择题 | 详细信息 |
|
下列说法正确的是 A. 物质发生化学变化都伴随着能量变化 B. 任何反应中的能量变化都表现为热量变化 C. 伴有能量变化的物质变化都是化学变化 D. 放热反应发生时不必加热 |
|
| 2. 选择题 | 详细信息 |
|
已知热化学方程式: SO2(g)+1/2O2(g) A. 196.64 kJ B. 196.64 kJ/mol C. <196.64 kJ D. >196.64 kJ |
|
| 3. 选择题 | 详细信息 |
|
下列变化中,属于吸热反应的是( ) ①液态水的汽化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释 ④KCl03分解制氧气 ⑤生石灰跟水反应生成熟石灰 ⑥CaCO3高温分解⑦CO2+C ⑧Ba(OH)2·8H2O与固体NH4Cl混合 ⑨C(s)+H2O(g) A. ②③④⑤⑥⑦⑧⑨ B.②④⑥⑦⑧⑨ C.②④⑥⑧ D.②③④⑧⑨ |
|
| 4. 选择题 | 详细信息 |
|
准确量取25.00mL KMnO4溶液,最好选用的仪器是 A. 25mL量筒 B. 25mL酸式滴定管 C. 25mL碱式滴定管 D. 有刻度的50mL烧杯 |
|
| 5. 选择题 | 详细信息 |
|
下列离子方程式中,属于水解反应的是( ) A.HCOOH+H2O B.CO2+H2O C.CO32- + H2O D.HS- + H2O |
|
| 6. 选择题 | 详细信息 |
|
物质的量浓度相同的下列溶液中,NH4+浓度最大的是 A. (NH4)2SO4 B. (NH4)2CO3 C. (NH4)2SO3 D. (NH4)2Fe(SO4)2 |
|
| 7. 选择题 | 详细信息 |
|
下列微粒在水溶液中显酸性的是 A. Cl— B. SO42— C. NH4+ D. CH3COO— |
|
| 8. 选择题 | 详细信息 |
|
在0.1mol/LCH3COOH溶液中存在如下电离平衡:CH3COOH A. 加入水时,平衡向逆反应方向移动 B. 加入少量NaOH固体,平衡向正反应方向移动 C. 加入少量0.1mol·L-1 HCl溶液,溶液中c(H+)减小 D. 加入少量CH3COONa固体,平衡向正反应方向移动 |
|
| 9. 选择题 | 详细信息 |
在容积不变的密闭容器中有如下反应:2SO2(g)+O2 (g)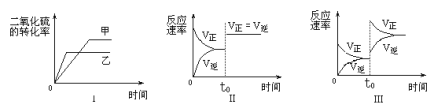 ①图Ⅰ研究的是温度对化学平衡的影响,且乙的温度较高 ②图Ⅱ研究的是催化剂对反应速率的影响,化学平衡不移动 ③图Ⅱ研究的是t0时刻通入氦气增大体系压强对反应速率的影响 ④图Ⅲ研究的是t0时刻增大O2的浓度对反应速率的影响 A. ①② B. ②③ C. ②④ D. ③④ |
|
| 10. 选择题 | 详细信息 |
下图表示一定条件下N2+3H2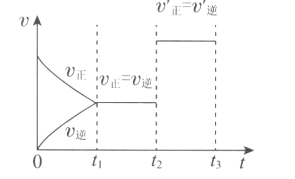 A.加压 B.升温 C.加入催化剂 D.增大反应物浓度 |
|
| 11. 选择题 | 详细信息 |
|
100 mL 浓度为2 mol·L-1的盐酸跟过量的锌片反应,为加快反应速率,又基本不影响生成氢气的总量,可采用的方法是( ) A. 加入适量的6 mol·L-1的盐酸 B. 加入数滴氯化铜溶液 C. 加入适量蒸馏水 D. 加入适量的氯化钠溶液 |
|
| 12. 选择题 | 详细信息 |
在一个容积为2 L的密闭容器中,加入0.8 mol的A2气体和0.6 mol B2气体,一定条件下发生如下反应:A2(g)+B2(g) A. 图中a点的值为0.15 B. 该反应的平衡常数K=0.03 C. 温度升高,平衡常数K值减小 D. 平衡时A2的转化率为62.5% |
|
| 13. 选择题 | 详细信息 |
|
在恒容密闭容器中,可逆反应C(s)+CO2(g) ①单位时间内生成n molCO2的同时生成n molC ②单位时间内生成n molCO2 的同时生成2n mol CO ③CO2 、CO的物质的量浓度之比为1: 2的状态 ④混合气体的密度不再改变的状态 ⑤混合气体的压强不再改变的状态 ⑥C的质量不再改变的状态 A. ①④⑤⑥ B. ②④⑤⑥ C. ②③⑤⑥ D. ①②③④ |
|
| 14. 选择题 | 详细信息 |
H2S2O3是一种弱酸,实验室欲用0.01 mol·L-1的Na2S2O3溶液滴定I2溶液,发生的反应为I2+2Na2S2O3=2NaI+Na2S4O6,下列说法合理的是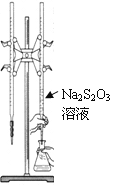 A. 该滴定可用甲基橙做指示剂 B. Na2S2O3是该反应的还原剂 C. 该滴定可选用右图所示装置 D. 该反应中每消耗2mol Na2S2O3,电子转移数为4mol |
|
| 15. 选择题 | 详细信息 |
|
下列各种离子一定能大量共存的是 A. 强碱性溶液中:Na+、K+、AlO2-、CO32— B. 含有大量Fe3+的溶液中:NH4+、SCN-、Cl-、K+ C. pH=7的溶液中:NH4+、Al3+、SO42—、CO32— D. c(OH-)=1×10-13mol/L的溶液中:K+、Fe2+、Cl-、NO3— |
|
| 16. 选择题 | 详细信息 |
|
已知温度T时水的离子积常数为KW,该温度下,将浓度为amol·L-1的一元酸HA与bmol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是 A. a=b B. 混合溶液的PH=7 C. 混合溶液中,c(H+)= D. 混合溶液中c(H+)+c(B+)=c(OH-)+C(A-) |
|
| 17. 选择题 | 详细信息 |
|
常温下体积相同的下列四种溶液:①pH=3的盐酸 ②pH=3的醋酸溶液 ③pH=11的氨水 ④pH=11的NaOH溶液。下列说法中,正确的是 A.②和④混合,所得混合溶液的pH大于7 B.将四种溶液分别稀释到体积为原的100倍,溶液pH大小顺序③>④>②>① C.③和④分别与足量稀硫酸中和,消耗硫酸的体积③=④ D.①和③混合,所得混合溶液中c(H+)+ c(NH4+)=c(Cl-)+c(OH-) |
|
| 18. 选择题 | 详细信息 |
|
1体积pH=2.5的盐酸与10体积某一元强碱溶液恰好完全反应,则该碱溶液的pH等于( ) A. 9.0 B. 9.5 C. 10.5 D. 11.0 |
|
| 19. 选择题 | 详细信息 |
|
现有三种溶液各25mL:①Na2CO3②NaHCO3③NaOH,下列说法正确的是 A.三者浓度相同时,pH大小顺序为③>②>① B.三者浓度相同时,稀释相同倍数,pH变化最大的为② C.三者的pH均为9时,物质的量浓度的大小关系为③>②>① D.三者浓度相同时,分别加入同体积同浓度的盐酸后,pH最大的是① |
|
| 20. 选择题 | 详细信息 |
|
用盐酸标准液来滴定NaOH待测液,下列操作可能会使测定结果偏低的是 A. 酸式滴定管只用水洗 B. 锥形瓶只用水洗 C. 使用甲基橙做指示剂 D. 第一次观察酸式滴定管的刻度时仰视 |
|
| 21. 选择题 | 详细信息 |
某温度下,相同pH的盐酸和醋酸分别加水稀释至平衡,pH随溶液体积变化的曲线如下图所 示。据图判断正确的是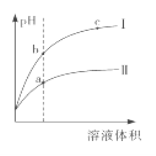 A. Ⅱ为盐酸稀释时的pH变化曲线 B. b点溶液的导电性比c点溶液的导电性强 C. a点KW的数值比c点KW的数值大 D. b点酸的总浓度大于a点酸的总浓度 |
|
| 22. 选择题 | 详细信息 |
|
下列叙述不正确的是 A. 金属腐蚀的本质是金属原子失去电子而被氧化 B. 钢铁吸氧腐蚀的正极反应是:O2+4e-+2H2O=4OH- C. 氢氧燃料电池中,氢气在负极发生氧化反应 D. 将地下钢管与直流电源的正极相连,用来保护钢管 |
|
| 23. 选择题 | 详细信息 |
|
电解饱和食盐水,当阴极附近有0.8molNaOH生成时,导线中通过电子的物质的量是( ) A. 0.16mol B. 0.2mol C. 0.4mol D. 0.8 mol |
|
| 24. 填空题 | 详细信息 | ||||||||||
|
滴定分析法又叫容量分析法,是一种重要的定量分析法。酸碱中和滴定是重要的滴定分析实验。 (1)现用已知浓度的NaOH溶液,用中和滴定法去测定未知浓度的CH3COOH溶液,实验步骤如下,请填写有关内容: ① 将酸式滴定管洗净后,每次用3~4 mL待测醋酸溶液润洗2~3次,然后加入待测醋酸至0刻度以上。把滴定管夹在滴定管夹上,转动活塞,放出少量溶液,使滴定管________,并使液面达到________,记录初始读数。 ② 用相似的方法在碱式滴定管中加入标准NaOH溶液,并调节好液面。 ③ 在酸式滴定管内取V mL的待测醋酸移到洗净的锥形瓶中,加2~3滴________作指示剂。 ④ 用标准NaOH溶液滴定待测醋酸。左手________,向锥形瓶中慢慢滴加NaOH溶液,右手轻轻摇动锥形瓶,两眼注视________,当溶液颜色由无色变为粉红色,且半分钟内不褪色,表示达到滴定终点,记录终点读数。 ⑤ 重复上述实验步骤。 (2) 指示剂的选择一般根据滴定突跃,其选择标准是________。 (3) 已知标准NaOH溶液的浓度为0.1000 mol·L-1,所取待测醋酸的体积V均为20.00 mL。实验过程记录的数据如下表,求待测醋酸的物质的量浓度________。
|
|||||||||||
| 25. 填空题 | 详细信息 | ||||||||
|
(1)一定条件下的密闭容器中,反应3H2(g)+3CO(g) a.升高温度 b.加入催化剂 c.减小CO2的浓度 d.增加CO的浓度 e.分离出二甲醚 (2)已知反应②2CH3OH(g)
①比较此时正、逆反应速率的大小:v(正) v(逆)(填“>”“<”或“=”)。 |
|||||||||
| 26. 填空题 | 详细信息 |
|
已知溶液中的化学反应大多是离子反应。根据要求回答下列问题。 (1)水存在如下平衡:H2O+H2O (2)向水中加NaHCO3固体,水的电离平衡向____(填“左”或“右”)移动,且所得溶液显____ 性。 (3)常温下,0.1 mol·L-1 CH3COONa溶液的pH为9,则由水电离出的c(H+)=________。 (4)若取pH、体积均相等的NaOH溶液和氨水分别加水稀释m倍、n倍后pH仍相等,则m____n ( 填“>”“<”或“=”)。 |
|
| 27. 填空题 | 详细信息 |
|
我国早在西汉成书的《淮南万毕术》里就有“曾青得铁则化为铜”的记载.曾青又有空青、白青、石胆、胆矾等名称,其实都是天然的硫酸铜. (1)写出“曾青得铁则化为铜”的离子方程式________. (2)理论上讲,任何自发的氧化还原反应都可以设计成原电池.若根据上述反应设计成原电池,则该电池的负极材料是________,发生________反应(选填“氧化”或“还原”),电解质溶液是________,正极上发生的电极反应为:________. (3)若导线上转移电子1mol,则生成铜________克. |
|
最近更新



