舒城中学网上考试练习
| 1. 选择题 | 详细信息 |
|
下列诗句或谚语可能与化学知识有关,其中说法不正确的是 A.“水乳交融,火上浇油”前者包含物理变化,而后者包含化学变化 B.“落汤螃蟹着红袍”肯定发生了化学变化 C.“滴水石穿,绳锯木断”不包含化学变化 D.“日照澄洲江雾开,淘金女伴满江隈”诗中包含了丁达尔效应 |
|
| 2. 选择题 | 详细信息 |
|
下列说法中正确的是 A.标准状况下,H2和N2的气体摩尔体积均为22.4 L B.1 mol·L-1 NaCl溶液的涵义是指此溶液中含有1 mol NaCl C.强氧化剂与强还原剂混合不一定能发生氧化还原反应 D.直径介于1~100 nm之间的微粒称为胶体 |
|
| 3. 选择题 | 详细信息 |
|
下列说法中正确的是 A.某元素的阳离子与同种阴离子可形成多种化合物 B.阳离子中肯定含有金属元素,但含有金属元素的离子不一定是阳离子 C.某物质经科学测定只含有一种元素,则可断定该物质一定是纯净物 D.1 molNa和1 molAl各自发生化学反应时钠失去的电子少,则钠单质的还原性弱于铝单质 |
|
| 4. 选择题 | 详细信息 |
|
设阿伏加德罗常数的值为NA,下列说法中正确的是 A.17 g OH-所含电子数为9NA B.等体积、等物质的量浓度的NaCl和KCl溶液中,阴、阳离子数目之和均为2NA C.23 gNa与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数为NA D.1 L 0.1 mol·L-1的硫酸溶液中含氧原子的数目为0.4NA |
|
| 5. 选择题 | 详细信息 |
|
下列离子方程式书写正确的是 A.醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑ B.向Ba(OH)2溶液中滴加等体积等浓度的NH4HSO4溶液:Ba2++2OH-+H++ C.向NaHCO3溶液中加入过量NaHSO4溶液: D.FeCl3溶液与Cu的反应:Cu+Fe3+=Cu2++Fe2+ |
|
| 6. 选择题 | 详细信息 |
|
铅的冶炼大致过程如下:①富集:将方铅矿(PbS)进行浮选;②焙烧:2PbS+3O2 A.浮选法富集方铅矿的过程,属于物理变化 B.将l molPbS冶炼成Pb,理论上至少需要6 g碳 C.方铅矿焙烧反应中,PbS是还原剂,还原产物只有PbO D.焙烧过程中,每生成l molPbO转移6 mol电子 |
|
| 7. 选择题 | 详细信息 | |||||||||||||||
下列各组离子能大量共存且满足相应要求的是
|
||||||||||||||||
| 8. 选择题 | 详细信息 |
在下图点滴板上进行四个溶液间反应的小实验,其对应反应的离子方程式书写正确的是( )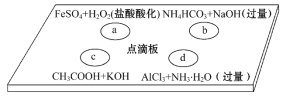 A. a反应:Fe2++2H++H2O2=Fe3++2H2O B. b反应:HCO3-+OH-=CO32-+H2O C. c反应:H++OH-=H2O D. d反应:Al3++3NH3·H2O=Al(OH)3↓+3NH4+ |
|
| 9. 选择题 | 详细信息 |
|
下列关于物质的量浓度表述中正确的是( ) A.0.3mol·L-1Na2SO4溶液中含有Na+和SO B.当1L水吸收22.4L氨气时所得氨水的浓度不是1mol·L-1,只有当22.4L氨气溶于水制得1L氨水时,其浓度才是1mol·L-1 C.在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO D.10℃时0.35mol·L-1的KCl饱和溶液100mL,蒸发掉5g水,冷却到10℃时其体积小于100mL,物质的量浓度仍为0.35mol·L-1 |
|
| 10. 选择题 | 详细信息 | ||||||||||||||
某研究性学习小组在国庆期间进行了研究膨松剂的蒸馒头实验。他们取一定量的面粉和水,和好面后分成六等份,按照下表加入对应物质后充分揉面,做成6个馒头放在同一个蒸锅里蒸制。实验完成后,他们比较6个馒头的大小和颜色,下列有关结论或解释不正确的是
|
|||||||||||||||
| 11. 选择题 | 详细信息 |
为了测定NaCl、Na2CO3·10H2O和NaHCO3的混合物中各组分的含量,某同学设计如下实验:取一定质量的混合物,通过测量反应前后②和③装置质量的变化,测定该混合物中各组分的质量分数。下列说法错误的是 A. ①、②、③中可以依次盛装碱石灰、无水CaCl2、碱石灰 B. 硬质玻璃管加热前,应关闭b,打开a,缓緩通入空气,直至a 处出来的空气不再使澄清石灰水变浑浊为止 C. 若将①装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量偏大 D. 实验过程中一直通入空气,停止加热后再停止通入空气 |
|
| 12. 选择题 | 详细信息 |
烧杯中盛有100 A.曲线a表示 B.曲线c表示 C.加入50mL D.加入 |
|
| 13. 选择题 | 详细信息 |
|
把一小块金属钠放入下列溶液中,说法正确的是 A.放入MgCl2溶液中:有氢气放出,有白色沉淀生成 B.放入稀CuSO4溶液中:有氢气放出,有紫红色铜析出 C.放入饱和NaOH溶液中:有氢气放出,恢复至室温后溶液的碱性增强 D.放入NH4NO3溶液中:有无色无味气体放出 |
|
| 14. 选择题 | 详细信息 |
|
某溶液中含有 A.CH3COO- B. |
|
| 15. 选择题 | 详细信息 |
A~F为常见化学物质,固体A在空气中易潮解,B和C能参与光合作用,B和D组成元素相同。它们相互转化的关系如图所示(“→”表示反应能一步实现,“-”表示相连物质间能发生反应,部分反应物、生成物和反应条件已省略)。下列说法错误的是( )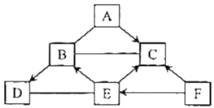 A.C和F组成元素可能相同 B.固体B可用于人工降雨 C.D和E在一定条件下反应生成B D.A~F属于酸、碱、盐、氧化物、单质中的四类物质 |
|
| 16. 选择题 | 详细信息 |
|
下列化合物中,不能由单质之间直接化合生成的是 A. Fe3O4 B. Na2O2 C. CuCl2 D. FeCl2 |
|
| 17. 选择题 | 详细信息 |
|
下列有关Na2O2的说法不正确的是 A.向包有Na2O2粉末的脱脂棉上滴加几滴水,脱脂棉剧烈燃烧起来,说明Na2O2与H2O反应放热且有氧气生成 B.Na2O2与CO2反应时有单质O2生成,该反应属于置换反应 C.Na2O2在空气中久置变白,最终产物为Na2CO3 D.Na2O2粉末加入Ca(HCO3)2溶液中,会产生气体和浑浊 |
|
| 18. 选择题 | 详细信息 |
一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左边充入 A.右边 B.右侧气体密度是相同条件下氢气密度的18倍 C.右侧 D.若充入相同组成的混合气体,其他条件不变,隔板处于距离右端1/6处,则前后两次压强之比为 |
|
| 19. | 详细信息 |
|
Ⅰ.(1)质量相同的 CO2、NH3、SO2、O3四种气体中,含有分子数目最多的是___________,在相同温度和相同压强条件下,体积最小的是____________。 (2)把2.0 mol·L-1 Na2SO4溶液和1.0 mol·L-1 H2SO4 溶液等体积混合(假设混合后溶液的体积等于混合前两种溶液的体积之和),则SO (3)已知:还原性:Fe2+>Br->Cl-。向100 mLFeBr2溶液中通入标准状况下的Cl2 3.36 L,Cl2全部被还原,测得溶液中c(Br–)=c(Cl–),则原FeBr2溶液的物质的量浓度是____________。 Ⅱ.物质的转化关系如图所示,其中A是固体金属单质,燃烧时火焰呈黄色。请回答下列问题:  (1)B物质的名称__________ (2)A→C反应的化学方程式并用双线桥表示电子转移的方向和数目:__________________。 (3)试写出C→D反应的化学方程式___________________________________________。 |
|
| 20. 实验题 | 详细信息 |
实验室需使用0.5 mol·L-1的稀硫酸480 mL,现欲用质量分数为98%的浓硫酸(密度为1.84 g·cm-3)进行配制。回答下列问题: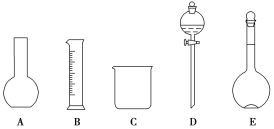 (1)如图所示的仪器中,配制溶液肯定不需要的是__________(填序号),配制上述溶液还需用到的玻璃仪器是__________(填仪器名称)。 (2)需用量筒量取98%的浓硫酸的体积为__________ mL。 (3)下列操作中正确的是__________(填序号,下同);若配制过程中的其他操作均准确,下列操作能使所配溶液浓度偏高的有________。 ①洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中 ②待稀释后的硫酸溶液冷至室温后,再将其转移到容量瓶中 ③将浓硫酸倒入烧杯中,再向烧杯中注入蒸馏水稀释浓硫酸 ④定容时,加蒸馏水超过刻度线,又用胶头滴管吸出 ⑤转移前,容量瓶中含有少量蒸馏水 ⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至刻度线 ⑦定容时,俯视刻度线 |
|
| 21. 填空题 | 详细信息 |
|
现有一混合溶液,只可能含有以下离子中的若干种:K+、NH 实验①:向第一份混合溶液中加入AgNO3溶液,有沉淀产生; 实验②:向第二份混合溶液中加入足量NaOH溶液,加热,收集到0.08mol气体; 实验③:向第三份混合溶液中加入足量BaCl2溶液后,得到干燥的沉淀12.54g,经足量稀盐酸洗涤、干燥后,沉淀质量为4.66g。 (已知:NH 根据上述实验,回答以下问题。 (1)由实验①推断该混合溶液___(填“一定”或“不一定”)含有Cl-。 (2)由实验②推断该混合溶液中应含有__(填离子符号),其物质的量浓度为__。 (3)由实验③可知12.54g沉淀的成分为___(填化学式)。 (4)综合上述实验,你认为以下结论正确的是__(填标号)。 A.该混合溶液中一定含有K+、NH B.该混合溶液中一定含有NH C.该混合溶液中一定含有NH D.该混合溶液中一定含有NH |
|
| 22. 实验题 | 详细信息 |
|
室温下,某同学进行CO2与Na2O2反应的探究实验,回答下列问题。 (1)用如图装置制备纯净的CO2  丙装置中盛放无水CaCl2的仪器名称是_______,乙装置中溶液的作用是_______。 (2)按照如图装置图进行实验(夹持装置略)。  ①先组装仪器,然后_______,再用注射器1抽取100mL纯净的CO2,将其连接在K1处,注射器2的活塞推到底后连接在K2处,具支U形管中装入足量的Na2O2粉末与玻璃珠。 ②打开止水夹K1、K2,向右推动注射器1的活塞,可观察到的现象是_______。 ③实验过程中,需缓慢推入CO2,反应的化学方程式为_______。 (3)实验结束后,当注射器1的活塞推到底时,测得注射器2中气体体积为70mL,则相同条件下反应消耗CO2的体积是_______。 |
|
最近更新



