贵溪市带答案与解析
| 1. 选择题 | 详细信息 |
|
生活是化学的源泉。下列叙述错误的是( ) A.75%浓度的酒精、含氯消毒剂均可以有效灭活新型冠状病毒 B.许多食品包装盒里用小袋包装的铁粉来防止食品氧化变质 C.生产宇航服所用的碳化硅陶瓷和碳纤维材料,是一种新型无机非金属材料 D.可溶性铜盐有毒,故人体内不存在铜元素 |
|
| 2. 选择题 | 详细信息 |
|
在实验室室中,对下列事故或药品的处理正确的是 A.有大量的氯气泄漏时,用肥皂水浸湿软布蒙面,并迅速离开现场 B.金属钠着火燃烧时,用泡沫灭火器灭火 C.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 D.漂白粉使用后,不需要再密封保存 |
|
| 3. 选择题 | 详细信息 |
|
下列关于硅酸的叙述,错误的是( ) A.硅酸是一种很弱的酸 B.硅酸的酸性比碳酸强 C.硅酸不稳定,加热脱水会生成二氧化硅 D.硅酸可以由可溶性硅酸盐与盐酸反应制得 |
|
| 4. 选择题 | 详细信息 |
|
下列说法中正确的是 A.氧化还原反应概念的发展,经历了拉瓦锡提出得氧失氧反应→汤姆生提出的得失电子(或电子对偏移)反应→弗兰克兰提出的化合价升降反应的过程 B.氯气能与铁发生化学反应,但液氯保存在钢瓶中 C.侯德榜是我国近代化学工业的奠基人之一,侯氏制碱法得到的纯碱是氢氧化钠 D.节日燃放的五彩缤纷的烟花,就是锂、钠、钾、锶、钡等金属化合物所呈现的各种艳丽的色彩,所以焰色试验是化学变化 |
|
| 5. 选择题 | 详细信息 |
|
1gNO2中含有氧原子a个,则阿伏加德罗常数可表示为( ) A. 23a B. 46a C. 46a/3 D. 16a |
|
| 6. 选择题 | 详细信息 |
|
用0.2mol·L-1某金属阳离子Rn+的盐溶液40mL,恰好将20mL0.4mol·L-1的Na2SO4中的硫酸根离子完全沉淀,则n值为( ) A.1 B.2 C.3 D.4 |
|
| 7. 选择题 | 详细信息 |
|
根据世界环保联盟的要求,广谱消毒剂ClO2将逐渐取代Cl2成为生产自来水的消毒剂。并且用于除甲醛。工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得,则反应后Na2SO3转化为( ) A.Na2SO4 B.SO2 C.S D.Na2S |
|
| 8. 选择题 | 详细信息 |
|
下列反应的离子方程式书写正确的是( ) A.Na2CO3溶液中加入少量盐酸: B.金属铝溶于氢氧化钠溶液:Al+2OH-+H2O= C.金属铝溶于稀盐酸:2Al+6H+=2Al3++3H2↑ D.氢氧化铝加入过量的氨水:Al(OH)3+OH-= |
|
| 9. 选择题 | 详细信息 |
|
下列离子方程式正确的是( ) A.浓硝酸中加入过量铁粉并加热:Fe+3 B.Ca(HCO3)2溶液与过量NaOH溶液反应 C.氢氧化铁溶于氢碘酸溶液:Fe(OH)3+3H+=Fe3++3H2O D.等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH-+ |
|
| 10. 选择题 | 详细信息 |
|
在一定量铁的氧化物中,加入 45mL 4 mol/L 硫酸溶液恰好完全反应,所得溶液中 Fe2+能恰好被标准状况下 672 mL 氯气氧化。则该固体中氧原子和铁原子的个数之比为( ) A. 9:7 B. 3:2 C. 6:5 D. 4:3 |
|
| 11. 选择题 | 详细信息 |
|
向500 mL 2 mol·L−1的CuSO4溶液中插入一铁片,反应片刻后取出铁片,洗涤、烘干,称其质量比原来增加2.0 g。下列说法错误的是(设反应后溶液的体积不变) A. 参加反应的铁的质量是14 g B. 析出的铜的物质的量是0.25 mol C. 反应后溶液中c(CuSO4)=1.5 mol·L−1 D. 反应后溶液中c(FeSO4)=1.5 mol·L−1 |
|
| 12. 选择题 | 详细信息 |
|
下列除去杂质的实验方法正确的是(括号里为少量杂质)( ) A.CO2( CO):用酒精灯点燃 B.K2CO3( NaHCO3):置于坩埚中加热 C.FeCl2( FeCl3):加入足量铜粉,过滤 D.Fe2O3(Al2O3):氢氧化钠溶液,过滤、洗涤 |
|
| 13. 选择题 | 详细信息 | ||||||||||||||||||||
下列各组物质中,满足如图物质一步转化关系的选项是
|
|||||||||||||||||||||
| 14. 选择题 | 详细信息 |
|
下列有关说法正确的是( ) A.硅酸钠溶液与醋酸混合的离子方程式为SiO B.向一定浓度的Na2SiO3溶液中通入适量CO2气体,出现白色沉淀,说明H2SiO3的酸性比H2CO3的酸性强 C.SiO2有导电性,所以SiO2可用于制备光导纤维 D.单质硅是将太阳能转变为电能的常用材料 |
|
| 15. 选择题 | 详细信息 |
|
下列物质不能通过相应的单质直接化合制取的是( ) A.HCl B.FeCl2 C.CuCl2 D.Na2O2 |
|
| 16. 选择题 | 详细信息 |
|
在离子浓度都为0.1mol/L的下列溶液中,加入(通入)某物质后,发生反应的先后顺序排列正确的是( ) A.在含 B.在含Fe3+、Br2的水溶液中滴加KI溶液:Fe3+、Br2 C.在含KI、NaBr的溶液中通入Cl2:KI、NaBr D.在含Ag+、Cu2+的溶液中加入Zn:Cu2+、Ag+ |
|
| 17. 填空题 | 详细信息 |
|
下列物质中:①Mg ②液态氯化氢 ③干冰 ④BaSO4 ⑤单质碘 ⑥熔融氢氧化钠 ⑦稀硫酸 ⑧乙醇。其中: (1)属于酸的是_________;属于碱的是__________;属于盐的是___________;属于氧化物的是____________; (2)属于电解质的是_________;属于非电解质的是___________; (3)能导电的是______________。 |
|
| 18. 填空题 | 详细信息 |
|
(1)实验室制取氯气反应的化学方程式为:_________; ①在该反应中,氧化剂与还原剂的物质的量之比是_________; ②若在反应中生成了标况下2.24L氯气,则电子转移的个数是________NA。 (2)氯酸钾和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O ①用双线桥表示上述反应中电子转移的方向和数目_________; ②浓盐酸在该反应中表现的性质是__________(填序号) A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性 ③该反应的还原产物是___________(填化学式); ④上述反应产生0.1molCl2时,转移电子的物质的量为___________。 |
|
| 19. 填空题 | 详细信息 |
|
铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。 (1)向沸水中逐滴滴加饱和FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是__nm。 (2)中国古代四大发明之一的指南针是由天然磁石制成的,其主要成分是______。 (3)Fe跟Cl2在一定条件下反应,所得产物的化学式是________。将该产物溶于水配成溶液,向其中一支试管中滴加KSCN溶液,则溶液变成_______色。 (4)若Fe2+溶液中存在Fe3+,除去的方法是:_____;该反应的离子方程式:_____。 (5)在FeCl2溶液中逐滴滴加NaOH溶液,实验现象是____;所发生的离子反应方程式为:___;____。 |
|
| 20. | 详细信息 |
A、B、C、D、E五种物质中均含有同一种非金属元素,它们能发生如图所示的转化关系。若该元素用R表示,则A为R的氧化物,D为R的单质,且D与NaOH溶液反应生成C和H2。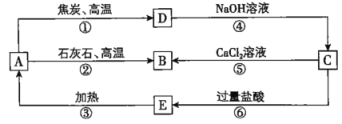 请回答下列问题。 (1)写出对应物质的化学式:A_______;C_______;E________。 (2)反应①的化学方程式为__________。 (3)反应④的离子方程式为__________。 (4)H2CO3的酸性强于E的酸性,请用离子方程式予以证明:________。 |
|
| 21. 计算题 | 详细信息 |
将一定质量的镁和铝的混合物投入100ml盐酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.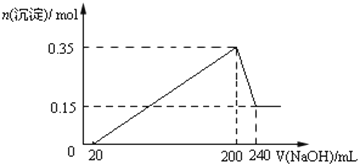 (1)原混合物中镁和铝的质量比为_______ (2)NaOH溶液的物质的量浓度为_______ mol•L﹣1 (3)生成的气体在标准状况下的体积为_______ L. |
|
最近更新



