2018年至2019年高二上册第一次月考化学在线测验完整版(甘肃省岷县一中)
| 1. 选择题 | 详细信息 |
|
下列各图所反映的措施中,目的是为了加快其化学反应速率的是 A.  B. B.  C.  D. D.  |
|
| 2. 选择题 | 详细信息 |
|
下列叙述中正确的是 A. 在稀溶液中,1 mol酸和1 mol碱完全反应所放出的热量,叫做中和热 B. 在101 kPa时,1 mol物质燃烧时所放出的热量叫做该物质的燃烧热 C. 热化学方程式中,各物质前的化学计量数不表示分子个数 D. 如果反应物所具有的总能量小于生成物所具有的总能量,则发生的反应是放热反应 |
|
| 3. 选择题 | 详细信息 |
|
下列反应既属于氧化还原反应,又属于放热反应的是 A. 铝片与稀盐酸的反应 B. Ba(OH)2·8H2O与NH4Cl晶体的反应 C. 灼热的炭与二氧化碳的反应 D. 碳酸氢钠受热分解 |
|
| 4. 选择题 | 详细信息 |
某实验小组学生用50 mL 0.50 mol·L−1盐酸与50 mL 0.55 mol·L−1 NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中放出的热量计算中和热。下列说法正确的是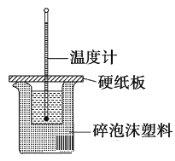 A. 实验过程中没有热量损失 B. 图中实验装置缺少环形玻璃搅拌棒 C. 烧杯间填满碎泡沫塑料的作用是固定小烧杯 D. 酸或碱的物质的量越大,所测中和热的数值越大 |
|
| 5. 选择题 | 详细信息 |
进行如下实验,在A锥形瓶中放入10g块状CaCO3,在B锥形瓶中放入5g粉末状CaCO3,分别加入50mL2mol/L盐酸。下图中能正确表示实验结果的是 |
|
| 6. 选择题 | 详细信息 |
|
已知450℃时,2SO2(g)+O2(g) A.Q2=Q1/2 B.Q2<Q1/2 C.Q2>Q1/2 D.不能确定 |
|
| 7. 选择题 | 详细信息 |
|
有两位同学在条件相同的情况下,测定可逆反应:A2(g)+3B2(g) A. 都正确 B. 都不正确 C. 甲正确,乙不正确 D. 甲不正确,乙正确 |
|
| 8. 选择题 | 详细信息 |
|
用CH4催化还原NOx可以消除氮氧化物的污染。例如: ①CH4(g)+4NO2(g) ②CH4(g)+4NO(g) 下列说法不正确的是 A. 由反应①可推知:CH4(g)+4NO2(g) B. 等物质的量的甲烷分别参加反应①、②,反应转移的电子数不同 C. 若用标准状况下4.48 L CH4还原NO2至N2,则放出的热量为173.4 kJ D. 若用标准状况下4.48 L CH4还原NO2至N2,则整个过程中转移的电子总物质的量为1.6 mol |
|
| 9. 选择题 | 详细信息 | ||||||||||||||||||||||||||||||||||||||||
已知:Na2S2O3+H2SO4===Na2SO4+SO2↑+S↓+H2O,下列各组实验中,反应速率最快的是
|
|||||||||||||||||||||||||||||||||||||||||
| 10. 选择题 | 详细信息 |
对于反应CH2=CH2+H2 → CH3CH3,反应过程的能量变化如图所示。下列说法正确的是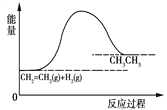 A. 此反应不属于氧化还原反应 B. 此反应的ΔH<0 C. 此反应中反应物的能量总和大于产物的能量总和 D. 1分子乙烯和1分子氢气的键能总和大于1分子乙烷的键能总和 |
|
| 11. 选择题 | 详细信息 |
下图表示可逆反应mA(g) +nB(s)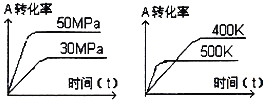 A. m>x,正反应为放热反应 B. m+n<x,正反应为吸热反应 C. m<x,正反应为放热反应 D. m>x,正反应为吸热反应 |
|
| 12. 选择题 | 详细信息 |
|
汽车尾气净化中的一个反应如下:NO(g)+CO(g) A.  B. B.  C. C.  D. D.  |
|
| 13. 选择题 | 详细信息 |
|
在恒温、体积为2 L的密闭容器中加入1 mol CO2和3 mol H2,发生如下的反应:CO2(g)+3H2(g) A. 容器中CO2、H2、CH3OH、H2O的物质的量之比为1∶3∶1∶1 B. v正(CO2)=v逆(H2O) C. 容器内混合气体密度保持不变 D. 3 mol H−H键断裂同时断裂3 mol H−O键 |
|
| 14. 选择题 | 详细信息 |
反应:L(s)+aG(g) 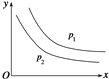 ①上述反应是放热反应 ②上述反应是吸热反应 ③a>b ④a<b A. ①③ B. ①④ C. ②③ D. ②④ |
|
| 15. 选择题 | 详细信息 |
|
在密闭容器中发生反应m A(g)+n B(g) A. m+n>p B. 平衡向逆反应方向移动 C. A的转化率提高 D. C的体积分数增加 |
|
| 16. 选择题 | 详细信息 |
在某一恒温、恒容的密闭容器中发生反应:3H2(g)+N2(g)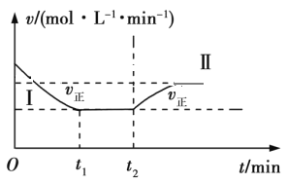 A. Ⅰ、Ⅱ两过程达到平衡时,平衡常数:KⅠ<KⅡ B. Ⅰ、Ⅱ两过程达到平衡时,NH3的体积分数:Ⅰ<Ⅱ C. Ⅰ、Ⅱ两过程达到平衡的标志:气体的平均密度不再发生变化 D. t2时刻改变的条件可以是向密闭容器中加H2和N2的混合气 |
|
| 17. 选择题 | 详细信息 |
一定条件下,在体积为3L的密闭容器中,发生反应:CO(g)+2H2(g)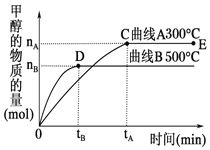 A. 平衡常数K(300 ℃)<K(500 ℃) B. 在其他条件不变时,压缩处于E点的体系体积,氢气浓度增大 C. 300 ℃,当容器内气体密度不变时说明反应已经达到平衡 D. 500 ℃,从反应开始到平衡,氢气的平均反应速率v(H2)= |
|
| 18. 填空题 | 详细信息 |
|
已知下列热化学方程式: ①H2(g)+1/2O2(g) ②H2(g)+1/2O2(g) ③C(s)+ 1/2O2(g) ④C(s)+O2(g) 回答下列各问题: (1)上述反应中属于放热反应的是_______________________。 (2)H2的燃烧热为________ (3)燃烧10 g H2生成液态水,放出的热量为________。 (4)CO的燃烧热为________;其热化学方程式为______________。 |
|
| 19. 解答题 | 详细信息 |
在2 L的密闭容器中发生反应后各物质的物质的量随时间变化的曲线如图所示。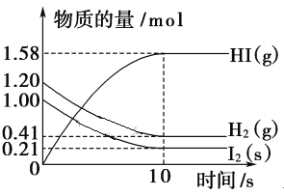 回答下列问题: (1)该反应的反应物和生成物分别是_______________,反应方程式为_______。 (2)0~10 s的平均反应速率v(H2)= ________v(HI)=____________________。 (3)根据上述反应速率数值,分析用不同物质表示同一化学反应在同一时间内,化学反应速率值是否必须相同?_________________________________________。 (4)能否用I2(s)表达该反应的反应速率,为什么?__________________________。 |
|
| 20. 解答题 | 详细信息 |
|
在一定温度下,在一体积固定的密闭容器中加入2 mol X和1 mol Y,发生如下反应:2X(g)+Y(g) (1)温度升高,平衡常数K的值是____________(填“增大”、“减小”或“不变”)。 (2)化学计量数a的值为____________。 (3)有同学认为,Q1一定小于Q,你认为该结论是否正确?________,其理由是___________________。 (4)维持温度不变,若起始时向容器中加入的物质的量如下列各项,则反应达到平衡后放出的热量仍为Q1 kJ的是____________(稀有气体不参与反应)。 A.2 mol X、1 mol Y、1 mol Ar B.a mol Z、1 mol W C.1 mol X、0.5 mol Y、0.5a mol Z、0.5 mol W D.2 mol X、1 mol Y、1 mol Z (5)X的转化率α=____________(用含Q、Q1的代数式表示)。 |
|
| 21. 解答题 | 详细信息 |
|
汽车排放的尾气是大气污染气体之一。如何减少污染气体的排放是科学家研究的热门课题。请回答下列问题: 使汽车排放的CO和NO在一定条件下发生反应:2NO(g)+2CO(g)  (1)该反应的化学平衡常数K=____。NO的平衡转化率=______。 (2)15 min时,若改变反应条件,导致CO浓度发生如图1所示的变化,则改变的条件可能是____(填标号)。 a.缩小容器体积 b.增加CO2的量 c.体积不变通入少量氩气 d.加入催化剂 (3)当NO与CO的起始浓度相等时,体系中NO的平衡转化率与温度、压强的关系如图2所示,则下列说法正确的是____(填标号)。 A.该反应ΔH<0 B.p1<p2<p3 C.升高温度正反应速率减小,逆反应速率增大 D.温度不变,增大压强,平衡常数增大 (4)以下说法中能判断反应2NO(g)+2CO(g) A.反应物和生成物的物质的量相等 B.单位时间内生成1 mol NO同时生成1 mol CO2 C.混合气体压强不再发生变化 D.NO的浓度不再变化 (5)向反应容器中再分别充入下列气体,能使NO转化率增大的是____(填标号)。 A.O2 B.N2 C.CO D.NO |
|
最近更新



