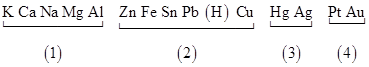高中化学2020-2021学年专题复习——金属通性(2)训练题【含详解】
| 1. | 详细信息 |
|
标准状况下,下列说法正确的是 A.等体积CH4和HF所含的电子数相同 B.pH=12的Na2CO3溶液中c(OH-)=10-2mol/L C.2.5gMg-Zn合金与足量的盐酸反应,放出的气体体积可能为2.24L D.由H2O2 制2.24LO2转移的电子数目为0.4NA
|
|
| 2. | 详细信息 |
|
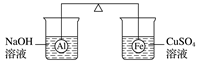
在杠杆的两端分别挂着质量相同的铝球和铁球,此时杠杆平衡。然后将两球分别浸没在溶液质量相等的稀烧碱溶液和硫酸铜溶液中一段时间,如图所示。下列说法正确的是( )
A.铝球表面有气泡产生,且有白色沉淀生成,杠杆不平衡 B.铝球表面有气泡产生,溶液澄清;铁球表面有红色物质析出,杠杆右边下沉 C.反应后去掉两烧杯,杠杆仍平衡 D.右边球上出现红色,左边溶液的c(OH-)增大
|
|
| 3. | 详细信息 |
|
下列有关物质的性质与用途具有对应关系的是 A.MgO具有高熔点,可用于制耐火材料 B.NaHCO3受热易分解,可用于治疗胃酸过多 C.金属铜具有金属光泽,可用作导电材料 D.浓硫酸具有脱水性,可用作干燥剂
|
|
| 4. | 详细信息 |
|
稀土金属铈(Ce)在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:①铈常见的化合价为+3价和+4价:②氧化性:Ce4+>Fe3+。下列说法不正确的是 A.工业上金属铈一般应低温密封保存 B.工业上不能采取用H2还原氧化铈的方法来治炼金属伂 C.工业上可以采取电解氯化铈水溶液的方法来获得铈单质 D.铈溶于氢碘酸的主要化学方程式可表示为2Ce+6HI===2CeI3+3H2↑
|
|
| 5. | 详细信息 |
|
下列金属单质中,能从CuSO4溶液中置换出Cu来的是( ) A.汞 B.银 C.钠 D.铁
|
|
| 6. | 详细信息 |
|
下列有关金属冶炼的说法中,不正确的是( ) A.用电解熔融氯化镁的方法冶炼金属镁 B.在加热情况下利用氢气还原三氧化二铝得到金属铝 C.用铝热法炼得熔点较高的金属铬 D.直接加热氧化汞得到金属汞
|
|
| 7. | 详细信息 |
|
将Mg、Al、Zn组成的混合物与足量的盐酸作用,放出H2的体积为2.8 L(标准状况下),则这三种金属的物质的量之和可能为 A.0.250 mol B.0.100 mol C.0.125 mol D.0.080 mol
|
|
| 8. | 详细信息 | ||||||
|
有关X、Y、Z、W四种金属的实验如下:
根据以上事实,下列判断或推测错误的是( ) A.Z的阳离子氧化性最强 B.Z放入CuSO4溶液中一定有Cu析出 C.W的还原性强于Y的还原性 D.用Y、Z和稀硝酸可构成原电池,且Y作负极
|
|||||||
| 9. | 详细信息 |
|
中美贸易战中,稀土是我国一张重要的牌。稀土金属铈(Ce)在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:①铈常见的化合价为+3价和+4价:②氧化性:Ce4+>Fe3+。下列说法不正确的是 A.工业上金属铈一般应低温密封保存 B.工业上可以采取用H2还原氧化铈的方法来治炼金属铈 C.工业上不可以采取电解氯化铈水溶液的方法来获得铈单质 D.铈溶于氢碘酸的主要化学方程式可表示为2Ce+6HI
|
|
| 10. | 详细信息 |
|
“垃圾是放错了位置的资源”,应该分类回收。生活中废弃的铁锅、铝制的易拉罐、铜导线等可以归为一类加以回收,它们属于( ) A.氧化物 B.盐 C.碱 D.金属或合金
|
|
| 11. | 详细信息 | |||||||||||||||
|
将金属与金属(或非金属)加热熔合在一起就能形成合金,根据下表中金属的熔点、沸点判断不能形成合金的是( )
A.Fe、Cu B.Al、Na C.Fe、Na D.Cu、Al
|
||||||||||||||||
| 12. | 详细信息 |
|
孔雀石的主要成分是Cu2(OH)2CO3。我国古人用孔雀石和焦炭混合共热的方法炼铜,其冶炼方法属于 A.热还原法 B.湿法炼铜 C.热分解法 D.电解冶炼法
|
|
| 13. | 详细信息 |
|
能通过置换反应得到金属铁的是( ) A.Na与FeSO4溶液反应 B.将CO通过灼热的Fe2O3 C.将H2通入FeSO4溶液 D.Al和Fe3O4混合加热至高温
|
|
| 14. | 详细信息 |
|
A、B、C、D、E代表五种金属,有以下化学反应: (1)水溶液中A+B2+=A2++B; (2)2C+2H2O(冷水)=2COH+H2↑; (3)D、E为电极,与E盐溶液组成原电池,D电极反应为D-2e-=D2+; (4)B可以溶于稀硫酸中,D不被稀硫酸氧化。 则这五种金属的活动性由弱到强的顺序是( ) A.D<E<B<A<C B.E<D<A<B<C C.E<D<B<A<C D.A<C<E<D<B
|
|
| 15. | 详细信息 |
|
类推是中学化学中重要的思维方法。下列类推结论正确的是 A.电解熔融NaCl制取Na,故电解熔融MgCl2也能制取Mg B.Fe与CuSO4溶液反应置换出Cu,故Na也能从CuSO4溶液中置换出Cu C.铝和硫加热得到Al2S3,故铁和硫加热得到Fe2S3 D.次氯酸钙溶液和CO2反应生成CaCO3和HClO,故次氯酸钙和SO2反应生CaSO3和HClO
|
|
| 16. | 详细信息 |
|
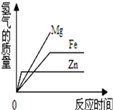
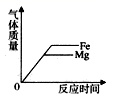
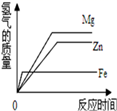
等质量的稀硫酸分别与足量的镁、铁、锌三种金属反应,下列图象能正确表示氢气质量与反应时间之间关系的是( ) A. C.
|
|
| 17. | 详细信息 |
|
现代建筑的门窗框架常用古铜色的硬铝制造,取硬铝样品作如下实验: ①取硬铝样品加入过量的盐酸,有气体生成,溶液中存有不溶物, ②过滤得到的残渣,加入过量的氢氧化钠溶液,有气体生成,溶液中仍存有不溶物。 (已知:硅不与盐酸反应,Si+2NaOH+H2O===Na2SiO3+2H2↑) 由此可推知,硬铝的组成可能为( ) A.Al Cu Mg Si B.Al Mg Si Zn C.Al Fe C Cu D.Al Mg Zn Fe
|
|
| 18. | 详细信息 |
|
下列冶炼金属的原理正确的是( ) A.电解食盐水制备金属钠 B.加热分解Cu2O制备金属铜 C.用A12O3与CO热还原法制备单质铝 D.湿法炼铜是用铁和硫酸铜溶液反应
|
|
| 19. | 详细信息 |
|
两种金属的混合物共15g,跟足量的盐酸反应时,恰好得到11.2L氢气(标况)。下列各组金属不可能构成上述条件的混合物的是 A.镁和银 B.铜和锌 C.铝和铁 D.镁和铁
|
|
| 20. | 详细信息 |
|
化学与生产、生活息息相关,下列叙述错误的是 A.“真金不怕火炼”说明有些金属(例如金)即使在高温下也不与氧气发生反应 B.中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 C.含重金属离子的电镀废液不能随意排放 D.铜的金属活泼性比铁弱,可在海轮外壳上装若干铜块以减缓其腐蚀
|
|
| 21. | 详细信息 |
|
a、b、c、d、e五种金属;将a与b用导线接起来,浸入电解质溶液中,a金属溶解;将a、d分别投入等浓度的盐酸中,d比a反应强烈;将铜浸入b的盐溶液里,无明显变化;把铜浸入c的盐溶液里,有c析出.金属阳离子氧化性:c<e;则活动性顺序由强到弱为 A.a>c>e>d>b B.d>a>b>c>e C.d>b>a>c>e D.e>d>a>b>c
|
|
| 22. | 详细信息 |
|
为探究Zn和Cu的金属活动性强弱,提供的试剂有Zn、Cu、H2SO4溶液、ZnSO4溶液、CuSO4溶液。下列说法正确的是 A.ZnSO4溶液中加入Cu不能探究金属活动性强弱 B.最多只能设计一种实验方案 C.根据Zn和Cu的硬度能判断金属活动性强弱 D.选用两种试剂可实现目的
|
|
| 23. | 详细信息 |
|
钠和钾化学性质相似的根本原因是( ) A.都是碱金属 B.都与酸反应 C.都与水反应生成碱 D.原子的最外层都只有一个电子
|
|
| 24. | 详细信息 |
|
“类推”这种思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实践的检验,才能决定其正确与否,下列几种类推结论中错误的是( ) ①钠与水反应生成NaOH和H2,所有金属与水反应都生成碱和H2 ②铁露置在空气中一段时间后就会生锈,性质更活泼的铝不能稳定存在于空气中 ③Al(OH)3、Cu(OH)2受热易分解,Fe(OH)3受热也易分解 ④不能用电解熔融的AlCl3来制取金属铝,也不能用电解熔融的MgCl2来制取金属镁 A.①④ B.②④ C.①②④ D.①②③④
|
|
| 25. | 详细信息 | ||||||||
|
金属Ti(钛)是一种具有许多优良性能的较为昂贵的金属,钛和钛合金被认为是21世纪的重要金属材料。某化学兴趣小组在实验室探究Ti、Mg、Cu的活动性顺序。他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积、等浓度的足量稀盐酸中,观察现象如下:
下列有关这三种金属的说法正确的是 A.用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径 B.若钛粉中混有Mg,提纯Ti时可用稀盐酸除去Mg C.Cu和稀盐酸不发生化学反应 D.三种金属的活泼性由强到弱的顺序是Ti、Mg、Cu
|
|||||||||
| 26. | 详细信息 |
|
若金属锰(Mn)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是( ) A.Mn+2HCl==MnCl2+H2↑ B.Mg+MnSO4==MgSO4+Mn C.Mn+Cu(NO3)2==Mn(NO3)2+Cu D.Fe+MnSO4==FeSO4+Mn
|
|
| 27. | 详细信息 |
|
有两种金属粉末的混合物15.6g,投入足量的稀硫酸中充分反应,产生5.6 L标准状况时的氢气,此混合物不可能是( ) A.Fe和Zn B.Al和Zn C.Fe和Cu D.Mg和Al
|
|
| 28. | 详细信息 |
|
从金属利用的历史来看,先是青铜器时代,而后是铁器时代,铝的利用是200来年的事。下列金属的性质和特点跟这个先后顺序有关的是( ) ①地壳中的含量 ②活动性顺序 ③导电性 ④冶炼的难易程度 ⑤延展性 A.①③ B.②⑤ C.③⑤ D.②④
|
|
| 29. | 详细信息 |
|
在CuC12和FeC12的混合溶液中,加入一定量的锌粉,充分反应后过滤,向滤渣中加稀盐酸,有气体生成,则滤渣中一定含有 A.Cu、Fe和Zn B.Cu和Fe C.Zn和Cu D.Fe和Zn
|
|
| 30. | 详细信息 |
|
下列金属的冶炼原理中,属于热分解法的是: A.2HgO C.Fe+CuSO4 =Cu+FeSO4 D.2NaCl(熔融)
|
|
| 31. | 详细信息 | ||||||||
|
合金的应用极大地促进了人类社会的发展。下列不属于合金的是
A.A B.B C.C D.D
|
|||||||||
| 32. | 详细信息 |
|
不法分子有时用铜锌合金制成假金币行骗。下列方法中,不能有效鉴别真假的是 A.在空气中灼烧看表面是否变黑 B.利用阿基米德原理测密度 C.用手掂量轻重 D.滴一滴硝酸在金币的表面,观察现象
|
|
| 33. | 详细信息 |
|
金属单质具有的通性是( ) A.硬度大 B.具有金属光泽、导电、导热和延展性 C.熔沸点高 D.质地柔软
|
|
| 34. | 详细信息 |
|
下列关于金属的叙述中正确的是( ) A.常温下所有的金属都是固态 B.金属具有导电、导热和延展性 C.地壳中含量最多的金属铁元素 D.金属元素大多数以游离态存在于自然界
|
|
| 35. | 详细信息 |
|
下列冶炼金属的方法错误的是 A.电解熔融氧化铝制铝 B.加热氧化银制银 C.CO还原铁矿石制铁 D.电解食盐水制钠
|
|
| 36. | 详细信息 |
|
下列关于非金属元素和金属元素特征的叙述不正确的是 ①非金属元素可能有还原性,也可能有氧化性 ②非金属元素只能形成共价化合物 ③金属阳离子被还原不一定得到金属单质 ④金属元素不可能存在于阴离子中 ⑤金属元素与非金属元素形成的化合物一定是离子化合物 A.①③ B.②③ C.③④⑤ D.②④⑤
|
|
| 37. | 详细信息 |
|
两种金属粉末的混合物15 g,投入足量的稀盐酸中,得到5.6 L氢气(标准状况),则这种混合物可能是 A.镁和铁 B.镁和铝 C.铁和锌 D.铜和锌
|
|
| 38. | 详细信息 |
|
下列金属中,通常采用热还原法冶炼的是 A.钠 B.铁 C.银 D.金
|
|
| 39. | 详细信息 |
|
利用金属的活泼性不同,冶炼镁、铁、汞分别应采用的方法是 A.热还原法、热分解法、电解法 B.电解法、热还原法、热分解法 C.热分解法、热还原法、电解法 D.电解法、热分解法、热还原法
|
|
| 40. | 详细信息 |
|
下列金属一般用电解熔融盐的方法冶炼的是( ) A.活动性强的金属 B.活动性弱的金属 C.人类较早使用的金属 D.明代作货币的金属
|
|
| 41. | 详细信息 |
|
要验证Mg、Fe、Cu三种金属的活动性顺序,可选用下列哪组物质进行实验 A.Cu、FeCl2溶液、MgCl2溶液 B.Fe、Cu、MgCl2溶液 C.Mg、CuO、FeSO4溶液 D.Fe、CuSO4溶液、MgCl2溶液
|
|
| 42. | 详细信息 |
|
铁在高温条件下与氧化铜反应:2Fe+3CuO ①甲中含有FeCl3;②甲中不含FeCl3;③若向固体丙加稀盐酸无明显现象,则滤液乙中一定含有ZnCl2、FeCl2,可能含有CuCl2;④若向固体丙加稀盐酸有气体产生,则滤液乙中可能含有ZnCl2、FeCl2,一定不含有CuCl2。 A.①③ B.②③ C.①④ D.②④
|
|
| 43. | 详细信息 |
|
下列说法不正确的是:( ) A.生物质能来源于植物及其加工产品所存贮的能量,绿色植物通过光合作用将化学能转化成生物质能 B.2015年8月国内油价再次迎来成品油最高零售价的下调,上演了年内首场“四连跌”,但油品从国Ⅳ汽油升级到Ⅴ汽油,有助于减少酸雨、雾霾,提高空气质量 C.我国已能利用3D打印技术,以钛合金粉末为原料,通过激光熔化逐层堆积,来制造飞机钛合金结构件,高温下可用金属钠还原四氯化钛来制取金属钛 D.在元素周期表过渡元素处可以寻找催化剂和耐高温、耐腐蚀的合金材料
|
|
| 44. | 详细信息 |
|
有a、b、c、d四种金属,最高价氧化物对应的水化物碱性a强于b。将a、d分别投入等浓度的盐酸中,d比a反应剧烈。将Cu浸入b的盐溶液里,无明显变化。如果把Cu浸入c的盐溶液里,有c的单质析出。据此判断它们的活动性由强到弱的顺序是 A.d、c、a、b B.d、a、b、c C.d、b、a、c D.b、a、d、c
|
|
| 45. | 详细信息 |
|
下列金属中,既属于有色金属又属于轻金属的是 A.铁 B.铬 C.钠 D.银
|
|
| 46. | 详细信息 |
|
Al、Fe、Cu都是重要而常见的金属,下列有关说法正确的是( ) A.生活中常用的是它们的合金材料 B.三者的单质放置在空气中均只生成氧化物 C.三者所对应的氢氧化物在水中都存在溶解平衡 D.工业上制备这三种金属的方法依次为电解法、热分解法和热还原法
|
|
| 47. | 详细信息 |
|
将铁片放入下列溶液中,一段时间后取出铁片,测得其质量减轻且反应过程中有无色气体产生的是 A.AgNO3溶液 B.稀盐酸 C.CuSO4溶液 D.Na2SO4溶液
|
|
| 48. | 详细信息 | |||||||||||||||
|
化学知识无处不在,我国优秀的传统文化中蕴含着众多的化学知识,下列对应的相关解释或说法不正确的是
A.A B.B C.C D.D
|
||||||||||||||||
| 49. | 详细信息 |
|
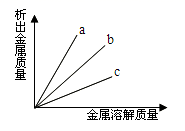
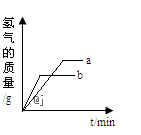
如图所示的是将铁、锌、铝、银分别插入足量的CuSO4溶液后,金属溶解的质量与析出金属的质量关系。图中直线a表示( )
A.铝 B.铁 C.锌 D.银
|
|
| 50. | 详细信息 |
|
下列金属单质,活泼性最强的是( ) A.Na B.Mg C.Al D.Fe
|
|
| 51. | 详细信息 |
|
下面有关金属的叙述正确的是( ) A.金属原子只有还原性而其阳离子只有氧化性 B.金属阳离子只存于化合物中且有相应的阴离子相配合 C.金属单质在氧化还原反应中只能做还原剂 D.若某单质具有延展性,则它一定是金属
|
|
| 52. | 详细信息 |
|
下列图象关系合理的是 A. B. C. D.
|
|
| 53. | 详细信息 |
|
自然界中只有极少数金属(如金和铂等)能以单质形式存在。它们应具备的性质是( ) A.不易被氧化 B.还原性较强 C.可与强酸反应放出氢气 D.可与空气中的氧气反应形成保护膜
|
|
| 54. | 详细信息 |
|
化学与生产、生活密切相关,下列说法不正确的是( ) A.开发太阳能、风能、地热能、潮汐能等新能源可以减少霾的产生 B.铝合金的大量使用归功于人们能使用焦炭从氧化铝中获得铝 C.还原铁粉可用作食品包装袋内的除氧剂 D.从诗句“千淘万漉虽辛苦,吹尽狂沙始得金”可知金的化学性质稳定,可用物理方法得到
|
|
| 55. | 详细信息 |
|
由钠、镁、铝、锌四种金属单质中的两种组成的合金l2g,跟足量的盐酸反应,产生5.6L标准状况下的氢气,那么此合金中一定含有的金属是( ) A.Na B.Mg C.Al D.Zn
|
|
| 56. | 详细信息 |
|
某化学兴趣小组在实验室中探究Ti、Mg、Cu的活泼性顺序。他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,现象如下:
下列有关三种金属的说法中正确的是( ) A.三种金属的活泼性由强到弱的顺序是Ti、Mg、Cu B.若钛粉中混有Mg,提纯Ti时可用稀盐酸除去Mg C.用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径 D.Cu和MgCl2溶液不发生化学反应
|
|
| 57. | 详细信息 |
|
能够说明金属锌的活动性比铁的活动性强的是( ) A.都能与盐酸反应产生氢气 B.都能与硫酸铜溶液反应生成铜 C.锌溶于氯化亚铁溶液并有铁生成 D.都能与氧气反应生成氧化物
|
|
| 58. | 详细信息 |
|
下列金属工业上通常用电解法冶炼,而不用热还原法冶炼的是( ) A.铁 B.铜 C.锌 D.钠
|
|
| 59. | 详细信息 |
|
有A、B、C、D四种金属。将A与B用导线连接起来,浸入稀硫酸溶液中,B极上有气泡。将A、D分别投入等浓度盐酸中,D比A反应剧烈。将铜浸入B的盐溶液里,无明显变化。如果把铜浸入C的盐溶液里,有金属C析出。据此判断它们的活动性由强到弱的顺序是( ) A.D>A>B>C B.D>C>A>B C.D>B>A>C D.B>A>D>C
|
|
| 60. | 详细信息 |
|
50g镁、锌、铝的混合物与适量的稀硫酸反应,得三种盐的混合溶液,然后加热、蒸发、结晶得三种盐的晶体共(不含结晶水)218g,则反应中生成H2的物质的量为( ) A.1.75mol B.1mol C.1.5mol D.0.75mol
|
|
| 61. | 详细信息 |
|
某化学活动小组欲制备一定量的氢气,下列方法不能达到目的的是 A.Cu和稀硝酸反应 B.Zn和稀盐酸反应 C.Fe和稀硫酸反应 D.A1和稀盐酸反应
|
|
| 62. | 详细信息 |
|
当足量的Cl2或盐酸分别与下列金属反应时,均有MCl2型化合物生成的是( ) A.Fe B.Mg C.Cu D.Ag
|
|
| 63. | 详细信息 |
|
下列关于金属的说法中正确的是( ) A.金属在常温下都能与氧气反应 B.常温下,与氧气反应的金属均可形成致密的氧化膜,阻止金属继续被氧化 C.铁能置换出CuSO4溶液中的铜,故银也能置换出CuSO4溶液中的铜 D.金属活动性顺序中,排在氢之前的金属与盐酸都能发生置换反应
|
|
| 64. | 详细信息 |
|
将下列四种金属分别投入水中,反应最剧烈的是 A.Al B.Fe C.Li D.Na
|
|
| 65. | 详细信息 |
|
下列几种类推结论中,错误的是( ) ①钠与水反应生成NaOH和H2;所有金属与水反应都生成碱和H2 ②铁露置在空气中一段时间后就会生锈;性质更活泼的铝不能稳定存在于空气中 ③化合物NaCl的焰色为黄色;Na2CO3的焰色也为黄色 A.②③ B.①③ C.①②③ D.①②
|
|
| 66. | 详细信息 |
|
金属活动性表:
以上四个区域通常采用热分解冶炼金属的是 A.(1) B.(2) C.(3) D.(4)
|
|
| 67. | 详细信息 |
|
下列金属单质,活泼性最强的是( ) A.Na B.K C.Cu D.Zn
|
|
| 68. | 详细信息 |
|
下列金属中,通常采用电解法冶炼的是( ) A.Na B.Cu C.Fe D.Ag
|
|
| 69. | 详细信息 |
|
人类的生活与生产离不开金属。下列对金属的利用不是由金属的活动性决定的是( ) A.用铁回收含银废液中的银 B.用锌与稀硫酸反应制取氢气 C.用金银制作具有保存价值的物品 D.用铝合金制作门窗框架
|
|
| 70. | 详细信息 | |||||||||||||||
|
下列金属在工业上的冶炼方法错误的是
|
||||||||||||||||
| 71. | 详细信息 |
|
历史上,铝、钛、铁、铜四种金属,最早使用的是 A.铜 B.铁 C.钛 D.铝
|
|
| 72. | 详细信息 |
|
下列叙述中可以说明金属甲的活动性比金属乙强的是 ( ) A.甲能跟稀盐酸反应而乙不能跟盐酸反应 B.同价态的阳离子,甲比乙的氧化性强 C.在氧化还原反应中,甲原子比乙原子失去的电子数多 D.将甲、乙作电极组成原电池时甲是正极
|
|
| 73. | 详细信息 |
|
现有铁与另一种金属组成的混合物1.2g,与足量稀硫酸反应生成H2 0.1g,则混合物中的另一种金属可能是( ) A.Mg B.Al C.Zn D.Cu
|
|
| 74. | 详细信息 |
|
下列说法不正确的是( )。 A.铝及其合金使用广泛,是因为铝比铁更耐酸、碱的腐蚀 B.通过红外光谱分析可以区分乙醇与乙酸乙酯 C.大部分金属的冶炼都是通过在高温下发生的氧化还原反应实现的 D.通常所说的三大合成材料是指塑料、合成橡胶和合成纤维
|
|
| 75. | 详细信息 |
|
将Na、Mg、Al各0.3mol分别放入足量的HCl中,同温同压下产生的气体的体积比是( ) A.1 : 2 : 3 B.6 : 3 : 2 C.3 : 1 : 1 D.1 : 1 : 1
|
|
| 76. | 详细信息 |
|
下列金属中,不能从硫酸铜溶液里置换出铜的是( ) A.Zn B.Fe C.Na D.Al
|
|
| 77. | 详细信息 |
|
下列说法不正确的是 A. B.铁锈的主要成分可表示为Fe2O3·nH2O C.钙单质可以从TiCl4中置换出Ti D.可用H2还原MgO制备单质Mg
|
|
| 78. | 详细信息 |
|
将两种金属单质组成的混合物11g,加到足量稀硫酸中,最终得到11.2L(标准状况下)的氢气,这两种金属可能是( ) A.Zn和Fe B.Ag和Mg C.Al和 Cu D.Mg和Zn
|
|
| 79. | 详细信息 |
|
我国有着悠久的历史传统文化。下列有关古诗词(句)中蕴含的化学知识分析正确的是 A.“千淘万漉虽辛苦,吹尽狂沙始到金”,说明金在自然界中以游离态存在,其化学性质稳定 B.“春蚕到死丝方尽,蜡炸成灰泪始干”,其中只有化学变化的过程 C.“纷纷灿烂如星陨,赫赫喧虺似火攻。 ”,灿烂的烟花是某些金属的焰色反应,属于化学变化 D.“粉身碎骨浑不怕,要留清白在人间”,其中发生的主要化学反应均为氧化还原反应
|
|
| 80. | 详细信息 |
|
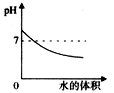
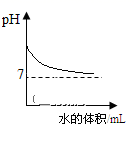
下列关系曲线不能正确反映其对应变化关系的是( ) A.加热KClO3和MnO2固体混合物 B.向Ca(OH)2溶液中通入CO2至过量(碳酸钙遇到溶有二氧化碳的水,能生成可溶性碳酸氢钙) C.向一定浓度的NaOH溶液中加水稀释 D.将等质量的Mg和Al分别与过量等浓度的盐酸反应,则a为Mg,b为Al
|
|
| 81. | 详细信息 |
|
由Na、Mg、Al、Fe四种金属单质中的两种组成的混合物共24克,跟足量盐酸反应,产生11.2LH2(标准状况下),由此可以判断混合物中必定含有( ) A.Fe B.Na C.Mg D.Al
|
|
| 82. | 详细信息 |
|
下列金属能跟酸反应生成氢气的是 A.Fe+H2SO4(稀) B.Al+H2SO4(浓) C.Ag+HCl(稀) D.Zn+HNO3(稀)
|
|
| 83. | 详细信息 |
|
对Al、Fe二种金属元素,下列说法正确的是 A.铝能够稳定存在于空气中,而铁很容易生锈,说明铁比铝活泼 B.等物质的量的Al、Fe分别与足量盐酸反应放出等质量的H2 C.二者的氢氧化物都不可以通过氧化物化合反应直接制备 D.二者的单质都能与强碱溶液反应生成H2
|
|
| 84. | 详细信息 |
|
两种金属混合物粉末15 g与足量的盐酸反应时生成标准状况下11.2 L氢气,符合上述情况的金属混合物 A.Mg、Fe B.Zn、Ag C.Zn、Fe D.Mg、Al
|
|
| 85. | 详细信息 |
|
已知三种二价金属的活动性顺序为X>Y>Z ,某同学设计了进行如下实验,请你从理论上分析肯定不能成功的实验是() A.实验一:X+YSO4→XSO4+Y B.实验二:Z+YSO4→ZSO4+Y C.实验三:X+H2SO4(稀)→XSO4+H2↑ D.实验四:Z+H2SO4(稀)→不反应
|
|
| 86. | 详细信息 |
|
下列金属中,工业上常用热分解法冶炼的是( ) A.镁 B.钾 C.铁 D.银
|
|
| 87. | 详细信息 |
|
下列金属的冶炼方法中,属于热还原法的是( ) A.2Ag2O =4Ag + O2↑ B.Fe + CuSO4 = FeSO4 + Cu C.Fe2O3 + 3CO
|
|
| 88. | 详细信息 |
|
某金属能与盐酸反应放出氢气,该金属与锌组成的原电池中,锌为原电池的负极,则金属可能是 A.铝 B.铜 C.铁 D.镁
|
|
| 89. | 详细信息 |
|
下列叙述正确的是( ) A.电解质在水溶液的电离需要通电 B.在化学反应中,得电子越多的氧化剂,其氧化性就越强 C.阳离子只能得到电子被还原,阴离子只能失去电子被氧化 D.含有最高价元素的化合物不一定具有很强的氧化性
|
|
| 90. | 详细信息 |
|
铊(Tl)是某超导材料的组成元素之一,与铝同族,位于周期表第六周期。Tl3+与银在酸性溶液中发生反应:Tl3++2Ag A.Tl+的最外层有1个电子 B.Tl能形成+3价和+1价的化合物 C.Tl3+氧化性比铝离子弱 D.Tl+的还原性比Ag强
|
|
| 91. | 详细信息 |
|
下列说法正确的是( ) A.有的复分解反应属于氧化还原反应 B.物质燃烧都属于氧化还原反应 C.生石灰、熟石灰都属于碱 D.金属在常温下都是固体
|
|
| 92. | 详细信息 |
|
已知钡的金属活动性处于钾和钠之间,下列反应可以实现的是 A.钡可以从氯化钾溶液中置换出钾 B.钡可以从冷水中置换出氢而得到氢气 C.钡可以从氯化钠溶液中置换出钠 D.钡不能置换出金属钠
|
|
| 93. | 详细信息 |
|
部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理:
下列说法正确的是 A.滤液A中的阳离子为Fe2+、Fe3+、H+ B.样品中Fe元素的质量为2.24 g C.样品中CuO的质量为4.0 g D.V=448
|
|
| 94. | 详细信息 |
|
两种金属混合粉末15g,与足量的盐酸反应时生成11.2L氢气(标准状况),符合上述情况的金属混合物的是 ( ) A.Mg和Al B.Mg和Ag C.Al和Zn D.Fe和Zn
|
|
| 95. | 详细信息 | ||||||||||||||||||||
|
以Al和不同的铜盐溶液间的反应为实验对象,探索Al与不同铜盐溶液反应的多样性。
(1)对实验Ⅰ进行研究 ①实验Ⅰ中生成红色物质的离子方程式为: __________________________________________ ②请写出60s后反应进一步加快可能的原因(写出一条)________________________________________________________________ (2)对实验Ⅱ进行研究 ①实验Ⅱ反应明显比实验Ⅰ缓慢,说明Al与不同的铜盐溶液反应呈现多样性,其原因可能有: ②假设一:SO 4 2-对Al与Cu 2+的置换反应存在一定的抑制作用。 ③假设二:________________________________________________ (3)为进一步研究上述假设,设计如下实验:
①实验Ⅵ的设计目的是:_______________________________________________ ②其中,实验Ⅰ与实验Ⅲ、Ⅳ做对比,结论为:______________________________ ③其中,实验Ⅱ与实验Ⅴ、Ⅵ做对比,结论为:________________________________
|
|||||||||||||||||||||
| 96. | 详细信息 |
|
冶炼金属常用以下几种方法: ①以C、CO或H2做还原剂的热还原法 ②利用铝热反应原理还原的铝热法 ③电解法 ④热分解法 下列金属各采用哪种方法还原最佳(用序号填写下列空白): (1)Fe、Zn、Cu等中等活泼金属________。 (2)Na、Mg、Al等活泼或较活泼金属________。 (3)Hg、Ag等不活泼金属________。 (4)V、Cr、Mn、W等高熔点金属________。
|
|
| 97. | 详细信息 |
|
已知氯气的氧化性很强,与金属发生反应一般生成高价态的金属氯化物。现有铜、铝、镁、铁、锌五种金属中的两种组成的混合物,取该混合物4g与足量的氯气反应后,固体质量增加7.1 g;等质量的该金属混合物投入足量的盐酸中,产生氢气0.2 g。金属混合物的组成情况可能有__种,分别为_____________ 。
|
|
| 98. | 详细信息 |
|
孔雀石的主要成分为CuCO3·Cu(OH)2,某同学设计从孔雀石中冶炼金属铜的方案如下: ①将孔雀石粉碎后加过量的稀硫酸; ②将反应后的混合物过滤; ③向滤液中加入一种金属粉末。 根据上述实验方案,试回答: (1)第①步反应中的现象为__。 (2)第③步加入的金属粉末是_,理由是__。 (3)若向滤液中加入过量生石灰后,过滤,将沉淀加热灼烧后再通入__气体,可制得较纯净的铜。
|
|
| 99. | 详细信息 |
|
Ⅰ、某校化学研究性学习小组欲设计实验验证Zn、Fe、Cu的金属活动性,他们提出了以下两种方案。请你帮助他们完成有关实验项目: (1)用三种金属与盐酸反应的现象来判断,实验中除选择大小相同的金属片外,还需要控制_____________、_____________相同;若选用一种盐溶液验证三种金属的活泼性,该试剂为___________。 (2)某小组同学采用Zn、Fe作为电极,只用一个原电池证明三种金属的活动性,则电解质溶液最好选用___________。 A.0.5mol·L-1氯化亚铁溶液 B.0.5mol·L-1氯化铜溶液 C.0.5mol·L-1盐酸 D.0.5mol·L-1氯化亚铁和0.5mol·L-1氯化铜混合溶液 Ⅱ、如图为甲烷燃料电池原理示意图。
(3)甲烷通入的一极为电源的____________极,该电极反应式:____________ (4)当电路中累计有2mol电子通过时,消耗的氧气体积在标准状况下____________L。
|
|
| 100. | 详细信息 |
|
在Cu(NO3)2和AgNO3的混合溶液中加入一定量的锌粉,使之充分反应后,有下列情况: (1)若反应后锌有剩余,则溶液中所含溶质是___________。 (2)若反应后过滤,向所得固体物质加盐酸没有气体产生。则溶液中一定有________,可能有_______________。 (3)若反应后过滤,向滤液中滴加NaCl溶液,有不溶于稀硝酸的白色沉淀生成,则此时溶液中含有的溶质为___________。
|
|
 B
B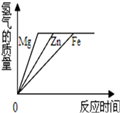
 D
D