2020人教版(2019)高中化学月考试卷
| 1. | 详细信息 |
|
25 ℃、101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ·mol-1,辛烷的燃烧热为5 518 kJ·mol-1。下列热化学方程式书写正确的是( ) A.2H+(aq)+SO B.KOH(aq)+ C.C8H18(l)+ D.2C8H18(g)+25O2(g)===16CO2(g)+18H2O(l) ΔH=-5 518 kJ·mol-1
|
|
| 2. | 详细信息 |
|
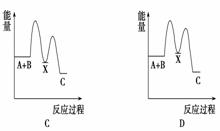
反应A+B—→C(ΔH<0)分两步进行:①A+B—→X(ΔH>0),②X—→C(ΔH<0)。下列示意图中,能正确表示总反应过程中能量变化的是( )
|
|
| 3. | 详细信息 |
|
我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程表示意图如下。
下列说法不正确的是( ) A.生成CH3COOH总反应的原子利用率为100% B.CH4→CH3COOH过程中,有C—H键发生断裂 C.①→②放出能量并形成了C—C键 D.该催化剂可有效提高反应物的平衡转化率
|
|
| 4. | 详细信息 | ||||||||
|
已知:①1 mol晶体硅中含有2 mol Si—Si键。 ②Si(s)+O2(g)===SiO2(g) ΔH,其反应过程与能量变化如图所示。 ③
下列说法中正确的是( ) A.晶体硅光伏发电是将化学能转化为电能 B.二氧化硅稳定性小于硅的稳定性 C.ΔH=-988 kJ·mol-1 D.ΔH=(a-c)kJ·mol-1
|
|||||||||
| 5. | 详细信息 |
|
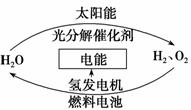
未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的是( ) ①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能 A.①②③④ B.③④⑤⑥⑦⑧ C.③⑤⑥⑦⑧ D.⑤⑥⑦⑧
|
|
| 6. | 详细信息 |
|
下列说法正确的是( ) A.H2O的分解反应是放热反应 B.氢能源已被普遍使用 C.2 mol H2O具有的总能量低于2 mol H2和1 mol O2的能量 D.氢气不易贮存和运输,无开发利用价值
|
|
| 7. | 详细信息 |
|
已知①H2(g)+ ②2H2(g)+O2(g)===2H2O(g) ΔH2=b kJ/mol ③H2(g)+ ④2H2(g)+O2(g)===2H2O(l) ΔH4=d kJ/mol 下列关系式正确的是( ) A.a<c<0 B.b>d>0 C.2a=b<0 D.2c=d>0
|
|
| 8. | 详细信息 |
|
室温下,将1 mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为ΔH1,将1 mol的CuSO4(s)溶于水会使溶液温度升高,热效应为ΔH2;CuSO4·5H2O受热分解的化学方程式为CuSO4·5H2O(s) A.ΔH2>ΔH3 B.ΔH1<ΔH3 C.ΔH1+ΔH3=ΔH2 D.ΔH1+ΔH2>ΔH3
|
|
| 9. | 详细信息 |
|
在25 ℃、101 kPa时,C(s)、H2(g)、CH3COOH(l)的燃烧热分别为393.5 kJ·mol-1、285.8 kJ·mol-1、870.3 kJ·mol-1,则2C(s)+2H2(g)+O2(g)===CH3COOH(l)的反应热为( ) A.-488.3 kJ·mol-1 B.+488.3 kJ·mol-1 C.-191 kJ·mol-1 D.+191 kJ·mol-1
|
|
| 10. | 详细信息 |
|
已知丙烷的燃烧热ΔH=-2 215 kJ·mol-1。若一定量的丙烷完全燃烧后生成1.8 g水,则放出的热量约为( ) A.55 kJ B.220 kJ C.550 kJ D.1 108 kJ
|
|
| 11. | 详细信息 | ||||||||||||
|
常温下,1 mol化学键分解成气态原子所需要的能量用E表示。结合表中信息判断下列说法不正确的是( )
A.432 kJ·mol-1>E(H—Br)>298 kJ·mol-1 B.表中最稳定的共价键是H—F键 C.H2(g)—→2H(g) ΔH=+436 kJ·mol-1 D.H2(g)+F2(g)===2HF(g) ΔH=-25 kJ·mol-1
|
|||||||||||||
| 12. | 详细信息 |
|
常温下,0.01 mol·L-1MOH溶液的pH为10。已知:2MOH(aq)+H2SO4(aq)===M2SO4(aq)+2H2O(l) ΔH1=-24.2 kJ·mol-1;H+(aq)+OH-(aq)===H2O(l) ΔH2=-57.3 kJ·mol-1。 则MOH在水溶液中电离的ΔH为( ) A.+33.1 kJ·mol-1 B.+45.2 kJ·mol-1 C.-81.5 kJ·mol-1 D.-33.1 kJ·mol-1
|
|
| 13. | 详细信息 |
|
在四个不同的容器中,在不同的条件下进行合成氨反应:N2(g)+3H2(g)2NH3(g)。根据在相同时间内测定的结果判断,生成氨的速率最快的是( ) A.v(H2)=0.01 mol·L-1·s-1 B.v(N2)=0.3 mol·L-1·min-1 C.v(NH3)=0.15 mol·L-1·min-1 D.v(H2)=0.3 mol·L-1·min-1
|
|
| 14. | 详细信息 | |||||||||||||||||||||||||
|
为探究NaHCO3、Na2CO3分别与1 mol·L-1盐酸反应(设两反应分别是反应Ⅰ、反应Ⅱ)过程中的热效应,进行实验并测得如下数据:
下列有关说法正确的是( ) A.仅通过实验③即可判断反应Ⅰ是吸热反应
C.通过实验可判断出反应Ⅰ、Ⅱ分别是吸热反应、放热反应 D.通过实验可判断出反应Ⅰ、Ⅱ分别是放热反应、吸热反应
|
||||||||||||||||||||||||||
| 15. | 详细信息 |
|
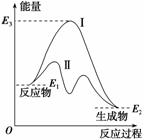
如图表示某反应的能量变化,按要求回答下列问题: (1)该反应是 (填“放热”或“吸热”)反应。 (2)该反应的ΔH=_ 。 (3)使用催化剂 (填“能”或“不能”)影响该反应的反应热。 (4)逆反应的活化能可表示为 。
|
|
| 16. | 详细信息 |
|
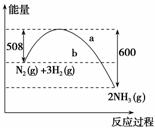
(1)如图是298 K、101 kPa时,N2与H2反应过程中能量变化的曲线图。该反应的热化学方程式为___________________________________________________________________。
(2)化学反应N2+3H22NH3的能量变化如图所示(假设该反应反应完全) 试写出N2(g)和H2(g)反应生成NH3(l)的热化学方程式: ________________________________________________________________________。
|
|
| 17. | 详细信息 | |||||||||
|
把温度为20 ℃,浓度为1.0 mol/L的H2SO4溶液和2.2 mol/L的碱溶液各50 mL混合[溶液密度均为1 g/mL,比热容为4.18 kJ/(kg·℃)]轻轻搅动,测得酸碱混合液的温度变化数据如下:
(1)反应NH3·H2O(aq)NH (2)计算上述两组实验测出的中和热:ΔH1=______________ kJ/mol;ΔH2=________ kJ/mol。 (3)由本题结论可预测将第1组中的1 mol/L的H2SO4溶液换成2 mol/L的CH3COOH溶液进行实验,测得的中和热数值________(填“大于”“小于”或“等于”)56.848。
|
||||||||||
| 18. | 详细信息 |
|
碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题: (1)有机物M经过太阳光光照可转化成N,转化过程如下:
ΔH=+88.6 kJ·mol-1。则M、N相比,较稳定的是________。 (2)已知CH3OH(l)的燃烧热ΔH=-726.5 kJ·mol-1,CH3OH(l)+ (3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:_________________________________________。 (4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可做耐高温材料,4Al(s)+3TiO2(s)+3C(s)===2Al2O3(s)+3TiC(s) ΔH=-1 176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为________。
|
|
| 19. | 详细信息 | ||||||||||
|
氢气是一种清洁能源,氢气的制取是氢能源利用领域的研究热点;氢气也是重要的化工原料。 (1)纳米级的Cu2O可作为太阳光分解水的催化剂。一定温度下,在2 L密闭容器中加入纳米级Cu2O并通入0.10 mol水蒸气发生反应:2H2O(g)
上述反应过程中能量转化形式为光能转化为________能,达平衡过程中至少需要吸收光能________kJ(保留三位小数)。 (2)氢气是合成氨工业的原料,合成塔中每产生2 mol NH3,放出92.2 kJ热量。已知:
则1 mol N—H键断裂吸收的能量约等于________。
|
|||||||||||
| 20. | 详细信息 | ||||||||||||||||||||||||||||
|
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题: (1)硫酸铜溶液可以加快氢气生成速率的原因是________________________________ ________________________________________________________________________; (2)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入六个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
①请完成此实验设计,其中:V1=____________,V6=____________,V9=____________; ②该同学最后得出的结论为当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:_______________________________________________________________________。
|
|||||||||||||||||||||||||||||