2017з”ҳиӮғй«ҳдёҖдёҠеӯҰжңҹдәәж•ҷзүҲй«ҳдёӯеҢ–еӯҰжңҹжң«иҖғиҜ•
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
еңЁдёӢеҲ—зү©иҙЁеҲҶзұ»дёӯпјҢеүҚиҖ…еҢ…еҗ«еҗҺиҖ…зҡ„жҳҜпјҲВ пјүгҖӮ A. ж°§еҢ–зү©гҖҒеҢ–еҗҲзү©В В В В В В В В В В В В В В В В В В В В В В B. еҢ–еҗҲзү©гҖҒз”өи§ЈиҙЁ C. жә¶ж¶ІгҖҒиғ¶дҪ“В В В В В В В В В В В В В В В В В В В В В В В В В В D. жә¶ж¶ІгҖҒеҲҶж•Јзі» |
|
| 2. | иҜҰз»ҶдҝЎжҒҜ |
|
е…үзәӨйҖҡдҝЎжҳҜдёҖз§ҚзҺ°д»ЈеҢ–зҡ„йҖҡдҝЎжүӢж®өпјҢеҲ¶йҖ е…үеҜјзәӨз»ҙзҡ„дё»иҰҒеҺҹж–ҷжҳҜпјҲВ пјүгҖӮ A. CaCO3В В В В В В В В В В В B. CaOВ В В В В В В В C. SiO2 В В В В В В В В В В D. Na2CO3 |
|
| 3. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҲҶж•Јзі»дёӯзҡ„еҲҶж•ЈиҙЁзҡ„зІ’еӯҗеӨ§е°ҸеұһдәҺзәізұізә§пјҲ1пҪһ100 nmпјүзҡ„жҳҜпјҲ В В В пјүгҖӮ A. Fe(OH)3иғ¶дҪ“В В В В В В В В В В В В В В В В В В В В В В В В B. Fe(OH)3жІүж·Җ C. FeCl3жә¶ж¶ІВ В В В В В В В В В В В В В В В В В В В В В В В В В D. зўҳж°ҙдёҺCCl4жә¶ж¶ІжҢҜиҚЎеҗҺзҡ„ж··еҗҲж¶І |
|
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
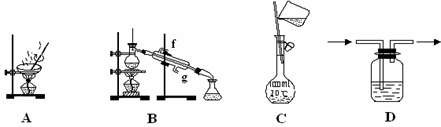
д»ҘдёӢе®һйӘҢиЈ…зҪ®дёҖиҲ¬дёҚз”ЁдәҺеҲҶзҰ»зү©иҙЁзҡ„жҳҜпјҲВ В В пјүгҖӮ
|
|
| 5. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зү©иҙЁдёӯеҗҢж—¶еҗ«жңүж°ҜеҲҶеӯҗе’Ңж°ҜзҰ»еӯҗзҡ„жҳҜпјҲ В В В пјүгҖӮ A. ж¶Іж°ҜВ В В В В В В В В В В В B. ж–°еҲ¶ж°Ҝж°ҙВ В В В В В В В В В C. CaCl2жә¶ж¶ІВ В В В В В D. ж¬Ўж°Ҝй…ё |
|
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
еҢәеҲ«дәҢж°§еҢ–зЎ«е’ҢдәҢж°§еҢ–зўіж°”дҪ“зҡ„жңҖдҪіж–№жі•жҳҜпјҲ В В пјүгҖӮ A. йҖҡе…Ҙжҫ„жё…зҹізҒ°ж°ҙВ В В В В В В В В В В В В В В В В В В В В В B. з”Ёж№ҝж¶Ұзҡ„и“қиүІзҹіи•ҠиҜ•зәё C. з”Ёе“Ғзәўжә¶ж¶ІВ В В В В В В В В В В В В В В В В В В В В В В В В В D. ж №жҚ®жңүж— жҜ’жҖ§ |
|
| 7. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҸҚеә”дёӯпјҢж°ҙеҸӘдҪңиҝҳеҺҹеүӮзҡ„жҳҜпјҲ В В В пјүгҖӮ A. CaO+H2O===Ca(OH)2В В В В В В В В В В В В В В В В В В B. C+H2O===CO+H2 В C. 2F2+2H2O===4HF+O2В В В В В В В В В В В В В В В В В В D. 3NO2+H2O===2HNO3+NO |
|
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
еңЁдёӢеҲ—еҸҚеә”дёӯпјҢзЎ«е…ғзҙ иЎЁзҺ°еҮәж°§еҢ–жҖ§зҡ„жҳҜпјҲВ В пјүгҖӮ A. зЁҖзЎ«й…ёдёҺй”ҢзІ’еҸҚеә”В В В В В В В В В В В В В В В В В В В В B. жө“зЎ«й…ёдёҺй“ңзүҮеҸҚеә” C. дәҢж°§еҢ–зЎ«дёҺж°§ж°”еҸҚеә”В В В В В В В В В В В В В В В В В В D. дёүж°§еҢ–зЎ«дёҺж°ҙзҡ„еҸҚеә” |
|
| 9. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зү©иҙЁз»„еҗҲдёӯпјҢж—ўиғҪе’Ңй…ёеҸҚеә”еҸҲиғҪе’ҢзўұеҸҚеә”зҡ„еҢ–еҗҲзү©жҳҜпјҲВ В В пјүгҖӮ в‘ Al В В В В В В В В В в‘ЎAl2O3 В В В В В В В в‘ўAl(OH)3 В В В В В В в‘ЈNaHCO3 A. в‘ в‘Ўв‘ўв‘ЈВ В В В В В В В B. в‘Ўв‘ўв‘ЈВ В В В В В C. в‘ в‘ўв‘ЈВ В В В В В В D. в‘ в‘Ўв‘Ј |
|
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
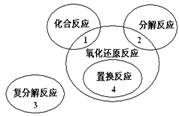
ж°§еҢ–иҝҳеҺҹеҸҚеә”дёҺеӣӣз§Қеҹәжң¬зұ»еһӢеҸҚеә”зҡ„е…ізі»еҰӮеҸіеӣҫжүҖзӨәпјҢеҲҷдёӢеҲ—еҢ–еӯҰеҸҚеә”еұһдәҺ3еҢәзҡ„жҳҜпјҲВ В пјүгҖӮ
A. Cl2+2KBr===Br2+2KClВ В В В В В В В В В В В В В В В B. 2NaHCO3====Na2CO3+H2O+CO2 C. 4Fe(OH)2+O2+2H2O===4Fe(OH)3 В В В В В В В В D. 2Na2O2+2CO2===2Na2CO3+O2 |
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
еҗ‘50 mL 18 molВ·L-1 H2SO4жә¶ж¶ІдёӯеҠ е…Ҙи¶ійҮҸзҡ„й“ңзүҮ并еҠ зғӯгҖӮе……еҲҶеҸҚеә”еҗҺпјҢиў«иҝҳеҺҹзҡ„H2SO4зҡ„зү©иҙЁзҡ„йҮҸжҳҜпјҲ пјүгҖӮ A. е°ҸдәҺ0.45В molВ В В В В В В В В В В В В В В В В В В В В В B. зӯүдәҺ0.45 mol C. еңЁ0.45 mol е’Ң0.9 molВ В В В В В В В В В В В В В В В D. еӨ§дәҺ0.9 molВ В
|
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зҰ»еӯҗеңЁжә¶ж¶ІдёӯиғҪеӨ§йҮҸе…ұеӯҳзҡ„жҳҜпјҲ пјүгҖӮ A. Na+гҖҒCO32вҖ”гҖҒSO42вҖ”гҖҒH+ В В В В В В В В В В В В В В В B. K+гҖҒAlO2вҖ”гҖҒH+гҖҒClвҖ” C. Fe3+гҖҒK+гҖҒOHвҖ”гҖҒNO3вҖ”В В В В В В В В В В В В В В В В D. Al3+гҖҒH+гҖҒNO3вҖ”гҖҒSO42вҖ” |
|
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зҰ»еӯҗж–№зЁӢејҸжӯЈзЎ®зҡ„жҳҜпјҲ пјүгҖӮ A. й“ҒдёҺзЁҖзЎ«й…ёеҸҚеә”В В В В В В В В В В В В Fe+2H+===Fe3++H2вҶ‘В В В B. ж°ўж°§еҢ–й“қдёҺи¶ійҮҸзӣҗй…ёеҸҚеә”В В В В Al(OH)3+3H+===Al3++3H2O C. й’ е’ҢеҶ·ж°ҙеҸҚеә”В В В В В В В В В В В В В В Na+2H2O===Na++H2вҶ‘+OHвҖ” D. й“ңзүҮдёҺзЁҖзЎқй…ёеҸҚеә”В В В В В В В В В Cu+NO3вҖ”+4H+===Cu2++NOвҶ‘+2H2O |
|
| 14. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—жә¶ж¶Ідёӯc(ClвҖ”)дёҺ50 mL 1 molВ·L-1AlCl3жә¶ж¶Ідёӯc(ClвҖ”)зӣёзӯүзҡ„жҳҜпјҲ пјүгҖӮ A. 150 mL 1 molВ·L-1зҡ„NaClжә¶ж¶ІВ В В В В В В В В В B. 75 mL 2 molВ·L-1NH4Clжә¶ж¶І C. 150 mL 2 molВ·L-1зҡ„KClжә¶ж¶ІВ В В В В В В В В В В D. 75 mL 1 molВ·L-1FeCl3жә¶ж¶І |
|
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
жҠҠ7.4 g Na2CO3В·10H2Oе’ҢNaHCO3з»„жҲҗзҡ„еӣәдҪ“ж··еҗҲзү©жә¶дәҺж°ҙй…ҚжҲҗ100 mLжә¶ж¶ІпјҢе…¶дёӯc(Na+)==0.6 molВ·L-1гҖӮиӢҘжҠҠзӯүиҙЁйҮҸзҡ„еӣәдҪ“ж··еҗҲзү©еҠ зғӯиҮіжҒ’йҮҚпјҢж®Ӣз•ҷеӣәдҪ“зҡ„иҙЁйҮҸжҳҜпјҲ пјүгҖӮ A. 3.18 gВ В В В В В В В В В B. 2.12 gВ В В В В В В В В C. 4.22 gВ В В В В В В В В D. 5.28 g В В |
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
|
з©әж°”жҳҜдәәзұ»з”ҹеӯҳжүҖеҝ…йңҖзҡ„йҮҚиҰҒиө„жәҗпјҢдёәж”№е–„з©әж°”иҙЁйҮҸиҖҢеҗҜеҠЁзҡ„вҖңи“қеӨ©е·ҘзЁӢвҖқеҫ—еҲ°дәҶе…Ёж°‘ж”ҜжҢҒгҖӮдёӢеҲ—жҺӘж–ҪдёҚеҲ©дәҺвҖңи“қеӨ©е·ҘзЁӢвҖқе»әи®ҫзҡ„жҳҜпјҲВ пјүгҖӮ A. жҺЁе№ҝдҪҝз”ЁзҮғз…Өи„ұзЎ«жҠҖжңҜпјҢйҳІжІ»SO2жұЎжҹ“ B. е®һж–Ҫз»ҝеҢ–е·ҘзЁӢпјҢйҳІжІ»жү¬е°ҳжұЎжҹ“ C. з ”еҲ¶ејҖеҸ‘зҮғж–ҷз”өжұ жұҪиҪҰпјҢж¶ҲйҷӨжңәеҠЁиҪҰе°ҫж°”жұЎжҹ“ D. еҠ еӨ§зҹіжІ№пјҢз…ӨзӮӯзҡ„ејҖйҮҮйҖҹеәҰпјҢеўһеҠ еҢ–зҹіеҺҹж–ҷдҫӣеә”йҮҸ |
|
| 17. | иҜҰз»ҶдҝЎжҒҜ |
|
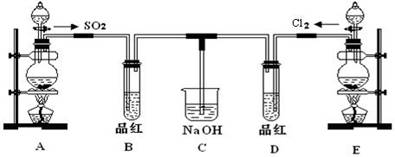
жҹҗеҢ–еӯҰе®һйӘҢе°Ҹз»„зҡ„еҗҢеӯҰдёәжҺўз©¶е’ҢжҜ”иҫғSO2е’Ңж°Ҝж°ҙзҡ„жјӮзҷҪжҖ§пјҢи®ҫи®ЎдәҶеҰӮдёӢзҡ„е®һйӘҢиЈ…зҪ®гҖӮ
пјҲ1пјүе®һйӘҢе®Өз”ЁиЈ…зҪ®AеҲ¶еӨҮSO2гҖӮжҹҗеҗҢеӯҰеңЁе®һйӘҢж—¶еҸ‘зҺ°жү“ејҖAзҡ„еҲҶж¶ІжјҸж–—жҙ»еЎһеҗҺпјҢжјҸж–—дёӯж¶ІдҪ“жңӘжөҒдёӢпјҢдҪ и®ӨдёәеҺҹеӣ еҸҜиғҪжҳҜпјҡ________________________________________________________пјӣ пјҲ2пјүе®һйӘҢе®Өз”ЁиЈ…зҪ®EеҲ¶еӨҮCl2пјҢе…¶еҸҚеә”зҡ„еҢ–еӯҰеҢ–еӯҰж–№зЁӢејҸдёәпјҡMnO2+4HClпјҲжө“пјү пјҲ3пјүв‘ еҸҚеә”ејҖе§ӢдёҖж®өж—¶й—ҙеҗҺпјҢи§ӮеҜҹеҲ°BгҖҒDдёӨдёӘиҜ•з®Ўдёӯзҡ„е“Ғзәўжә¶ж¶ІеҮәзҺ°зҡ„зҺ°иұЎжҳҜпјҡ В В В В В В В В Bпјҡ_________________________пјҢDпјҡ________________________гҖӮ В В В В в‘ЎеҒңжӯўйҖҡж°”еҗҺ,еҶҚз»ҷBгҖҒDдёӨдёӘиҜ•з®ЎеҲҶеҲ«еҠ зғӯпјҢдёӨдёӘиҜ•з®Ўдёӯзҡ„зҺ°иұЎеҲҶеҲ«дёә В В В В В В В В Bпјҡ_________________________пјҢDпјҡ________________________гҖӮ пјҲ4пјүеҸҰдёҖдёӘе®һйӘҢе°Ҹз»„зҡ„еҗҢеӯҰи®ӨдёәSO2е’Ңж°Ҝж°ҙйғҪжңүжјӮзҷҪжҖ§пјҢдәҢиҖ…ж··еҗҲеҗҺзҡ„жјӮзҷҪжҖ§иӮҜе®ҡдјҡжӣҙејәгҖӮ他们е°ҶеҲ¶еҫ—зҡ„SO2е’ҢCl2жҢү1пјҡ1еҗҢж—¶йҖҡе…ҘеҲ°е“Ғзәўжә¶ж¶ІдёӯпјҢз»“жһңеҸ‘зҺ°иӨӘиүІж•Ҳжһң并дёҚеғҸжғіиұЎзҡ„йӮЈж ·гҖӮиҜ·дҪ еҲҶжһҗиҜҘзҺ°иұЎзҡ„еҺҹеӣ пјҲз”ЁеҢ–еӯҰж–№зЁӢејҸиЎЁзӨәпјү_____________________________________гҖӮ |
|
| 18. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҗ„еҸҚеә”дёӯпјҢйҖҡе…Ҙзҡ„ж°”дҪ“еҸҚеә”зү©еҗ„иө·д»Җд№ҲдҪңз”ЁпјҹиҜ·йҖүжӢ©дёӢеҲ—еәҸеҸ·еЎ«з©әпјҡ A. еҸӘеҒҡж°§еҢ–еүӮВ В В В В В В В В В В В В В В В В В В В В В В В В В В В B. еҸӘеҒҡиҝҳеҺҹеүӮ C. ж—ўеҒҡж°§еҢ–еүӮеҸҲеҒҡиҝҳеҺҹеүӮВ В В В В В В В В В В В В В В В В В D. ж—ўдёҚеҒҡж°§еҢ–еүӮеҸҲдёҚеҒҡиҝҳеҺҹеүӮ пјҲ1пјүж°Ҝж°”йҖҡе…Ҙж°ҙдёӯпјҡCl2+H2O===HCl+HClO______________________ пјҲ2пјүдәҢж°§еҢ–ж°®йҖҡе…Ҙж°ҙдёӯпјҡ3NO2+H2O===2HNO3+NO__________________ пјҲ3пјүдәҢж°§еҢ–зўіж°”дҪ“йҖҡе…Ҙж°ўж°§еҢ–й’ҫжә¶ж¶ІдёӯпјҡCO2+2KOH===K2CO3+H2O____________ пјҲ4пјүдәҢж°§еҢ–зЎ«ж°”дҪ“йҖҡе…Ҙж°ўзЎ«й…ёдёӯпјҡSO2+2H2S===3S +2H2O_____________________ |
|
| 19. | иҜҰз»ҶдҝЎжҒҜ |
|
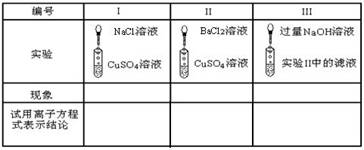
д»ҘдёӢиЎЁж јдёӯзҡ„е®һйӘҢжҳҜд»ҘCuSO4дёәдҫӢпјҢеҲҶжһҗз”өи§ЈиҙЁеңЁжә¶ж¶ІйҮҢжүҖиө·еҸҚеә”зҡ„е®һиҙЁ
|
|
| 20. | иҜҰз»ҶдҝЎжҒҜ |
|
з”ІгҖҒд№ҷгҖҒдёҷдёүз§Қзү©иҙЁд№Ӣй—ҙжңүеҰӮдёӢиҪ¬еҢ–е…ізі»пјҡ
пјҲ1пјүиӢҘз”ІжҳҜдёҚжә¶дәҺж°ҙзҡ„зҷҪиүІеӣәдҪ“зү©иҙЁпјҢж—ўиғҪжә¶дәҺзӣҗй…ёеҸҲиғҪжә¶дәҺж°ўж°§еҢ–й’ жә¶ж¶ІпјҢеҲҷз”ІжҳҜ _______________ пјӣеҶҷеҮә д№ҷвҶ’дёҷиҪ¬еҢ–зҡ„еҢ–еӯҰж–№зЁӢејҸ пјҡ___________________________гҖӮ (2)иӢҘд№ҷжә¶ж¶ІдёӯеҠ е…ҘKSCNжә¶ж¶ІпјҢжңүзәўиүІеҮәзҺ°,еҲҷз”Ізү©иҙЁжҳҜ__________________________пјӣ еҶҷеҮә з”ІвҶ’д№ҷиҪ¬еҢ–зҡ„зҰ»еӯҗж–№зЁӢејҸ_________________________________________гҖӮ |
|
| 21. | иҜҰз»ҶдҝЎжҒҜ |
|
е°Ҷ100 mL В 5 molВ·L-1 NaOH(aq)зЁҖйҮҠеҲ°500 mL пјҢзЁҖйҮҠеҗҺжә¶ж¶ІдёӯNaOHзҡ„зү©иҙЁзҡ„йҮҸжө“еәҰдёә______________пјӣ е°Ҷж°Ҝж°”йҖҡе…ҘжӯӨжә¶ж¶Іе……еҲҶеҸҚеә”пјҢеҸҜеҲ¶еҫ—жјӮзҷҪж¶ІпјҢе…¶дёӯеҗ«жңүж•ҲжҲҗеҲҶзҡ„зү©иҙЁзҡ„йҮҸжңҖеӨҡдёә_________________гҖӮ |
|
| 22. | иҜҰз»ҶдҝЎжҒҜ |
|
жңүдёүз§ҚйҮ‘еұһеҚ•иҙЁAгҖҒBгҖҒCпјҢе…¶дёӯAзҡ„з„°иүІеҸҚеә”дёәй»„иүІпјҢBгҖҒCжҳҜеёёи§ҒйҮ‘еұһгҖӮдёүз§ҚйҮ‘еұһеҚ•иҙЁAгҖҒBгҖҒCиғҪдёҺж°”дҪ“з”ІгҖҒд№ҷгҖҒдёҷеҸҠзү©иҙЁDгҖҒEгҖҒFгҖҒGгҖҒHд№Ӣй—ҙеҸ‘з”ҹеҰӮдёӢиҪ¬еҢ–е…ізі»пјҲеӣҫдёӯжңүдәӣеҸҚеә”зҡ„дә§зү©е’ҢеҸҚеә”зҡ„жқЎд»¶жІЎжңүж ҮеҮәпјүгҖӮ
иҜ·ж №жҚ®д»ҘдёҠдҝЎжҒҜеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ пјҲ1пјүеҶҷеҮәдёӢеҲ—зү©иҙЁзҡ„еҢ–еӯҰејҸпјҡ A_____________пјӣH ______________пјӣ G___________пјӣд№ҷ____________гҖӮ пјҲ2пјүеҶҷеҮәдёӢеҲ—еҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸпјҡ еҸҚеә”в‘ ___________________________________________________________пјӣ еҸҚеә”в‘Ў___________________________________________________________гҖӮ |
|
| 23. | иҜҰз»ҶдҝЎжҒҜ |
|
200в„ғж—¶,11.6 g CO2е’Ңж°ҙи’ёж°”зҡ„ж··еҗҲж°”дҪ“дёҺи¶ійҮҸзҡ„Na2O2е……еҲҶеҸҚеә”еҗҺеӣәдҪ“зҡ„иҙЁйҮҸеўһеҠ дәҶ3.6 g ,жұӮеҺҹж··еҗҲж°”дҪ“дёӯCO2е’Ңж°ҙи’ёж°”зҡ„иҙЁйҮҸжҜ”пјҹ |
|
- 2017-2018е№ҙй«ҳдәҢдёҠеӯҰжңҹ第дәҢж¬ЎжңҲиҖғеҢ–еӯҰиҜ•еҚ·пјҲиҙөе·һзңҒйҒөд№үеёӮ第еӣӣдёӯеӯҰпјү
- 2018еұҠй«ҳдёү12жңҲжңҲиҖғеҢ–еӯҰеңЁзәҝжөӢйӘҢпјҲж№–еҚ—зңҒеІійҳіеёӮ第дёҖдёӯеӯҰпјү
- 2017-2018е№ҙй«ҳдәҢдёҠеӯҰжңҹйҳ¶ж®өжөӢиҜ•еҢ–еӯҰиҖғиҜ•йўҳпјҲжұҹиӢҸзңҒеҰӮдёңй«ҳзә§дёӯеӯҰпјү
- 2016-2017е№ҙй«ҳдёҖдёҠжңҹеҢ–еӯҰжңҹдёӯиҖғиҜ•еңЁзәҝжөӢйӘҢпјҲе№ҝдёңзңҒе№ҝе·һеёӮжү§дҝЎдёӯеӯҰпјү
- 2018е№ҙй«ҳиҖғеҢ–еӯҰдәҢиҪ®дё“йўҳеӨҚд№ дё“йўҳеҚҒдәҢпјҡжңүжңәеҢ–еҗҲзү©пјҲеӨҮиҖғпјү
- 2016-2017е№ҙй«ҳдәҢдёҠеҶҢеҢ–еӯҰжңҹдёӯиҖғиҜ•иҜ•еҚ·пјҲе№ҝдёңзңҒжұ•еӨҙеёӮжҫ„жө·дёӯеӯҰпјү
- 2017-2018е№ҙй«ҳдёҖдёҠеҶҢеҢ–еӯҰжңҹжң«иҖғиҜ•дё“йўҳи®ӯз»ғпјҲж№–еҢ—зңҒй•ҝйҳідёӯеӯҰпјү
- 2016-2017е№ҙй«ҳдёҖдёҠеӯҰжңҹжңҹжң«иҖғиҜ•е®һйӘҢе°ҸзҸӯеҠ иҜ•зҗҶ科综еҗҲеҢ–еӯҰиҜ•еҚ·пјҲеӣӣе·қзңҒе°„жҙӘеҺҝпјү