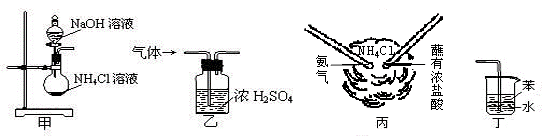2019甘肃高一下学期人教版(2019)高中化学期末考试
| 1. | 详细信息 |
|
短周期主族元素X、Y、Z、W原子序数依次增大,X原子的最外层有6个电子,Y是迄今发现的非金属性最强的元素,在周期表中Z位于I A族,W与X属于同一主族。下列说法正确的是 A. 元素X、W的简单阴离子具有相同的电子层结构 B. 由Y、Z两种元素组成的化合物是离子化合物 C. W的简单气态氢化物的热稳定性比Y的强 D. 原子半径:r(X)<r(Y)<r(Z)<r(W)
|
|
| 2. | 详细信息 |
|
不符合ⅦA族元素性质特征的是 A. 从上到下原子半径逐渐减小 B. 易形成-1价离子 C. 最高价氧化物的水化物显酸性 D. 从上到下氢化物的稳定性依次减弱
|
|
| 3. | 详细信息 |
|
下列有关化学用语使用正确的是( ) A. 硫原子的原子结构示意图: B. NH4Cl的电子式为: C. 原子核内有10个中子的氧原子: D. HBr
|
|
| 4. | 详细信息 |
|
下列各组物质中化学键的类型相同的是( ) A. HCl MgCl2 NH4Cl B. H2O Na2O CO2 C. CaCl2 NaOH H2O D. NH3 H2O CO2
|
|
| 5. | 详细信息 |
|
同一周期的X、Y、Z三种元素,已知最高价氧化物对应水化物的酸性顺序为HXO4>H2YO4>H3ZO4,则下列判断错误的是 A. 原子半径:X>Y>Z B. 气态氢化物的稳定性:HX>H2Y>ZH3 C. 元素原子得电子能力:X>Y>Z D. 阴离子的还原性:Z3->Y2->X-
|
|
| 6. | 详细信息 |
|
下列有关化学用语表示正确的是( ) A. H2O2的电子式:H+[ C. 原子核中有10个中子的氧离子:188O2— D. HClO的结构式H-Cl-O
|
|
| 7. | 详细信息 |
|
反应A(g)+3B(g) A. v(C)=0.04mol·(L·s)-1 B. v(B)=0.06mol·(L·min)-1 C. v(A)=0.15mol·(L·min)-1 D. v(D)=0.01mol·(L·s)-1
|
|
| 8. | 详细信息 |
|
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水” 电池在海水中放电时的有关说法正确的是( ) A. 正极反应式:Ag+Cl--e-=AgCl B. 每生成1 mol Na2Mn5O10转移2 mol电子 C. Na+不断向“水”电池的负极移动 D. AgCl是还原产物
|
|
| 9. | 详细信息 |
|
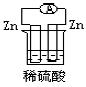
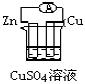
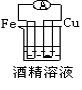
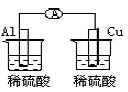
下列图各个装置中能组成原电池的是 ( ) A. B. C. D.
|
|
| 10. | 详细信息 |
|
下列各组的电极材料和电解液,不能组成原电池的是( ) A. 铜片、石墨棒,蔗糖溶液 B. 锌片、石墨棒,硫酸铜溶液 C. 锌片、铜片,稀盐酸 D. 铜片、银片,硝酸银溶液
|
|
| 11. | 详细信息 |
|
复印机工作时,空气中的氧气可以转化为臭氧:3O2=2O3,下列有关说法正确的是 A. 该变化属于物理变化 B. 1mol 臭氧比 1mol 氧气的能量高 C. 空气中臭氧比氧气更稳定 D. 氧分子中的化学键断裂会放出能量
|
|
| 12. | 详细信息 |
|
有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于CH4在O2中燃烧,则下列说法正确的是 ①每消耗1molCH4可以向外电路提供8mole- ②负极上CH4失去电子,电极反应式CH4+10OH--8e-=CO32-+7H2O ③负极上是O2获得电子,电极反应式为 O2+2H2O+4e-=4OH- ④电池放电后,溶液pH不断升高 A. ①② B. ①③ C. ①④ D. ③④
|
|
| 13. | 详细信息 |
|
下列关于甲烷的叙述错误的是( ) A. 天然气的主要成分 B. 最简单的有机物 C. 含碳质量分数最大的有机物 D. 与氯气在光照条件下能发生取代反应
|
|
| 14. | 详细信息 |
|
某校学生用化学知识解决生活中的问题,下列家庭小实验中不合理的是 ( ) A. 用高度白酒进行皮肤消毒 B. 用米汤(含淀粉)检验加碘盐中的碘酸钾(KIO3) C. 用食用碱(Na2CO3溶液)洗涤餐具上的油污 D. 用灼烧并闻气味的方法区别纯棉织物和纯毛织物
|
|
| 15. | 详细信息 |
|
下列有机分子中,所有的原子不可能处于同一平面的是
|
|
| 16. | 详细信息 |
|
在实验室中,下列除去杂质的方法不正确的是( ) A. 溴苯中混有溴,加稀NaOH溶液反复洗涤、分液 B. 乙烷中混有乙烯,将混合气体通过高锰酸钾 C. 硝基苯中混有浓硝酸和浓硫酸,将其倒入NaOH溶液中,静置,分液 D. 乙烯中混有SO2和CO2,将其通过NaOH溶液洗气
|
|
| 17. | 详细信息 |
|
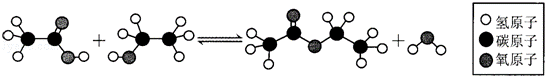
如图所示的某有机反应,其反应类型为( )
A. 取代反应 B. 加成反应 C. 水解反应 D. 氧化反应
|
|
| 18. | 详细信息 |
|
下列物质中,不能和氯气发生取代反应的是 A. CH3Cl B. CCl4 C. CH2Cl2 D. CH4
|
|
| 19. | 详细信息 |
|
下列关于有机物 A. 分子式为C9H9O2 B. 能使Br2的CCl4溶液褪色 C. 能发生酯化反应 D. 能发生加成反应
|
|
| 20. | 详细信息 |
|
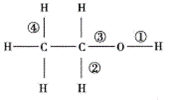
乙醇分子中的化学键如图所示,则乙醇在催化氧化时,化学键断裂的位置是( )
A. ②③ B. ①② C. ③④ D. ①③
|
|
| 21. | 详细信息 |
|
利用下列实验装置完成相应的实验,能达到实验目的的是 A. 浓硫酸稀释
|
|
| 22. | 详细信息 |
|
下列反应的离子方程式书写正确的是( ) A. 氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu B. 稀H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ C. 氢氧化钡溶液与稀H2SO4反应:Ba2++ D. 碳酸钙与盐酸反应:
|
|
| 23. | 详细信息 |
|
下列关于Cl2性质的说法正确的是 A. 密度比空气小 B. 是无色无味的气体 C. 能使干燥的有色布条褪色 D. 可与NaOH溶液反应
|
|
| 24. | 详细信息 |
|
下列装置适用于实验室制氨气并验证氨气
A. 用装置甲制取氨气 B. 用装置乙除去氨气中的水蒸气 C. 用装置丙检验氨气 D. 用装置丁吸收尾气
|
|
| 25. | 详细信息 |
|
下列说法错误的是
A. 石油主要是由烃组成的混合物 B. ①主要发生物理变化 C. ②包括裂化、裂解等过程 D. ③是加成反应,产物名称是二溴乙烷
|
|
| 26. | 详细信息 |
|
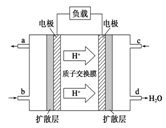
人们利用原电池原理制作了多种电池,以满足日常生活、生产和科学技术等方面的需要。请根据题中提供的信息,回答下列问题。 (1)铅蓄电池在放电时的电池反应为 (2) (3)已知甲醇燃料电池的工作原理如图所示。该电池工作时,b口通入的物质为___,该电池正极上的电极反应式为__;当6.4g甲醇(
|
|
| 27. | 详细信息 | ||||||
|
四种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。
请回答下列问题: (1)元素Z位于周期表中第_______周期,_______族; (2)这些元素的氢化物中,水溶液碱性最强的是_____________(写化学式); (3)XW2的电子式为________________________; (4)Y的最高价氧化物的化学式为_________________。
|
|||||||
| 28. | 详细信息 |
|
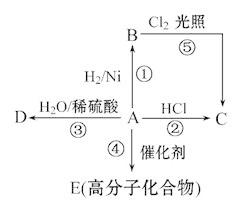
某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型。
根据图示回答下列问题: (1)写出A、B、C、D、E的结构简式: A ,B ,C ,D ,E ; (2)写出②、⑤两步反应的化学方程式,并注明反应类型: ② ,反应类型 ; ⑤ ,反应类型 。
|
|
| 29. | 详细信息 |
|
.为了验证木炭可被浓硫酸氧化成CO2,选用如图所示装置(内含物质)进行实验。
(1)如按气流由左向右的流向,连接如图所示装置的正确顺序是_______(填字母) (2)若实验检验出有CO2生成,则装置乙、丙中的现象分别为装置乙中______,装置丙中________。 (3)装置丁中酸性KMnO4溶液的作用是________。 (4)写出装置甲中所发生反应的化学方程式:________。
|
|
| 30. | 详细信息 |
|
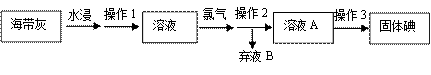
下图为从海带中提碘生产的实验室模拟流程。试回答下列问题:
(1)实验操作中所用玻璃仪器为酒精灯、烧杯、普通漏斗、牛角管、锥形瓶、蒸馏烧瓶等。若要完成操作1,还缺少的玻璃仪器有 ,该仪器的作用为 ;操作2的名称为 ;若要完成操作3,还缺少的玻璃仪器有 。 (2)实验室用二氧化锰制氯气的化学方程式为 。 (3)弃液B中滴入淀粉液,溶液呈蓝色,但通入二氧化硫后蓝色褪去,写出该过程中发生反应的化学方程式并用双线桥标明电子转移的方向和数目 。
|
|
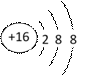

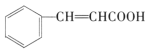
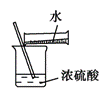 B.
B. 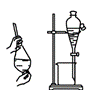 C.
C. 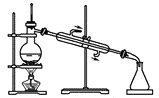 D.
D.