2019福建高一上学期人教版(2019)高中化学月考试卷
| 1. | 详细信息 |
|
下列说法不正确的是( ) A.假说经过反复验证和修正,才能发展成为科学的理论 B.模型一般可分为物体模型和思维模型 C.研究物质的性质常用观察、实验、分类、比较等方法 D.科学实验能解决化学学科的所有问题
|
|
| 2. | 详细信息 | ||||||||||||||||||||||||||||||
|
下列物质的分类正确的是( )
|
|||||||||||||||||||||||||||||||
| 3. | 详细信息 |
|
容量瓶上需标有以下五项中的①温度;②浓度;③容量;④压强;⑤刻度线( ) A.①③⑤ B.②③⑤ C.①②③ D.②③④
|
|
| 4. | 详细信息 |
|
下列说法中,正确的是( ) A.摩尔是一种国际基本物理量 B.OH-的摩尔质量是17 g·mol-1 C.O2的气体摩尔体积是22.4L·mol-1 D.2mol H2O的摩尔质量是1mol H2O的两倍
|
|
| 5. | 详细信息 |
|
钠与水反应时的现象与下列钠的性质无关的是( ) A.熔点低 B.硬度小 C.密度小 D.很活泼
|
|
| 6. | 详细信息 |
|
下列关于金属钠的叙述中正确的是( ) A.金属钠切开一段时间后,可以观察到钠是灰色的固体 B.钠钾合金可用做原子反应堆的导热剂 C.火灾现场有钠存放时,必须用泡沫灭火器灭火 D.金属钠投入CuSO4溶液中可观察到有红色物质析出
|
|
| 7. | 详细信息 |
|
制备氯化物时,常用两种方法:①用金属与氯气直接化合制得;②用金属与盐酸反应制得。用以上两种方法都可制得的氯化物是( ) A.MgCl2 B.FeCl3 C.FeCl2 D.CuCl2
|
|
| 8. | 详细信息 |
|
下列物质间发生反应, 在不同条件下可制得不同产物的是( ) A.氢气与氯气 B.碳与二氧化碳 C.钠与氧气 D.钠与盐酸溶液
|
|
| 9. | 详细信息 |
|
下列物质的保存方法正确的是( ) A.白磷可露置于空气中保存 B.漂白粉必须避光密封保存 C.新制氯水保存在无色试剂瓶中 D.过氧化钠必须保存在水中
|
|
| 10. | 详细信息 |
|
下列说法中不正确的是( ) A.氢气在氯气中燃烧,火焰呈苍白色 B.光照新制氯水有气泡逸出,该气体是氧气 C.氯气车间液氯泄漏时,应往地势高的地方逃离 D.液氯能使干燥的蓝色石蕊试纸先变红后褪色
|
|
| 11. | 详细信息 |
|
氯水中存在多种物质,它们在不同反应中表现出不同性质。下列结论正确的是( ) A.加入有色布条,片刻后有色布条褪色,说明有Cl2存在 B.滴入酚酞试剂,酚酞变红,说明有H+存在 C.加入AgNO3溶液,生成白色沉淀,说明有Cl-存在 D.加入NaOH溶液,氯水的浅黄绿色消失,说明有HClO存在
|
|
| 12. | 详细信息 |
|
若NA代表阿伏加德罗常数,下列说法正确的是( ) A.20℃,1个标准大气压时11.2LN2含有的分子数为0.5NA B.标况下,23g钠的体积为22.4L C.常温常压下,30gNO含有的原子数为2NA D.0℃、1.01×104 Pa时,11.2L氧气所含的原子数目为NA
|
|
| 13. | 详细信息 |
|
下列做法能达到目的的是( ) A.将0.1mol Na2CO3溶于1L水中,可得0.1mol/L的Na2CO3溶液 B.可使用 250 m L容量瓶分两次完成 490 m L某浓度的BaCl2溶液的配制 C.将 62 g Na2O溶于水配成1 L溶液,可得到浓度为1mol/L的NaOH溶液 D.将25.0g胆矾(CuSO4﹒5H2O)溶于水后配成100mL溶液所得溶液浓度为1mol/L
|
|
| 14. | 详细信息 |
|
把1L含有MgSO4和Na2SO4的混合溶液分成两等份,一份加入含8g NaOH的溶液,恰好使镁离子完全沉淀;另一份加入0. 2mol/L、1L的BaCl2溶液,恰好使硫酸根离子完全沉淀,则原混合溶液中钠离子的物质的量浓度为( ) A.0.4 mol/L B.0.2mol/L C.0.8mol/L D.0.6mol/L
|
|
| 15. | 详细信息 |
|
下列各溶液中,K+物质的量浓度最大的是( ) A.4 L 0.5 mol/L KCl溶液 B.5 L 0. 4 mol/L KOH溶液 C.1 L 0.3 mol/L K2SO4溶液 D.2 L 0.15 mol/L K3PO4溶液
|
|
| 16. | 详细信息 |
|
下列有关实验用品的使用或操作的叙述中,正确的是( ) A.配制稀硫酸时,先向烧杯中注入浓硫酸,再加水稀释 B.用托盘天平称量20.22g氯化钠固体 C.称量NaOH固体时,将NaOH直接放在托盘上的纸上 D.容量瓶只能用于配制准确浓度的溶液,不能作为反应容器使用
|
|
| 17. | 详细信息 |
|
填写下列空白: (1) 含有6.02×1023个H的H2SO4,其物质的量是_____,与____mol NaOH恰好完全中和。 (2) 9gH2O中含有的氧原子数是 ,标况下 LCO2中含有的氧原子数与之相等。 (3) 1L 1 mol·L -1的Al2(SO4)3溶液,其中含有 个Al3+,SO42-浓度为 。 (4) 标准状况下,aL的NH3溶于水形成bml溶液,计算氨水浓度的表达式为_______。
|
|
| 18. | 详细信息 |
|
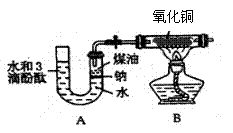
实验是学习化学的一个重要途径。
① A装置中钠块反应的化学方程式: 。 ② U形管中溶液的颜色 。 ③ 氧化铜的变化现象 。 (2) 图2是实验室利用高锰酸钾和浓盐酸制备氯气 (2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O)、验证氯气是否具有漂白性并制备氯化铁的装置, 装置B中盛装饱和食盐水用以除去A中挥发的氯化氢气体。
① 下列关于装置B中长颈漏斗的说法正确的是 A.长颈漏斗可以用于添加饱和食盐水 B.长颈漏斗起到平衡内外压强的作用 C.气体会从长颈漏斗逸出污染环境 ② 装置C中II处放入的是干燥剂,该装置的实验目的是验证氯气是否具有漂白性,湿润 的有色布条应放置在_________处(填“I”或“Ⅲ”)。 ③ 装置 D中发生反应的现象是 , 化学方程式是____ 。 ④ 为防止氯气污染空气,E中盛放的是 。 ⑤ 工业上用氯气和石灰乳制备漂白粉,漂白粉的有效成分是 , 制备反应的方程式是: 。
|
|
| 19. | 详细信息 | |
|
已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
(1) 该“84消毒液”的物质的量浓度约为____________ mol·L-1。 (2) 取用任意体积的该NaClO溶液时,下列物理量中不随所取体积 多少而变化的是____________(填选项字母)。 A.溶液中NaClO的物质的量 B.溶液的浓度 C.溶液中ClO- 的数目 D.溶液的密度 (3) 该同学参阅该“84消毒液”的配方,欲用NaClO固体配制500mL该浓度的溶液。 ① 配制该溶液时使用的仪器除托盘天平、药匙、烧杯、玻璃棒外,还必须用到的仪器有_______________、_______________。 ② 写出整个实验简单的操作过程:计算→_________ →溶解→移液→洗涤→______ →摇匀→装瓶→贴标签。 ③ 定容时的正确操作是:待容量瓶中的液体液面距离容量瓶的刻度线 1~2 cm 时,改用 ____________滴加,并且目光要平视刻度线,至___________ ,定容完成。 (4) 下列操作对溶液的浓度有偏小的是 ( ) A.没有洗涤烧杯和玻璃棒。 B.使用前容量瓶用蒸馏水洗涤,且没有干燥。 C.定容时俯视液面。 D.摇匀后发现液面低于刻度线,又滴加蒸馏水。
|
||
| 20. | 详细信息 |
|
列式计算 把6.5 g Zn放入500mL稀盐酸中,Zn与盐酸都恰好完全反应。计算: (1) 生成的气体在标准状况下的体积; (2) 原稀盐酸的物质的量浓度。
|
|