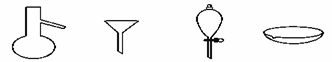2020四川高一上学期人教版(2019)高中化学期末考试
| 1. | 详细信息 |
|
引起环境污染的原因不正确的是 A. 重金属、农药和难分解有机物、含N、P的污水等会造成水体污染 B. 装饰材料中的甲醛、芳香烃及氡等会造成居室污染 C. SO2、NO2和CO2都会导致酸雨的形成 D. CO2的大量排放会造成温室效应的加剧
|
|
| 2. | 详细信息 |
|
下图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是
A. 蒸馏、蒸发、萃取、过滤 B. 蒸馏、过滤、萃取、蒸发 C. 萃取、过滤、蒸馏、蒸发 D. 过滤、蒸发、萃取、蒸馏
|
|
| 3. | 详细信息 |
|
下列物质中属于纯净物的是 A、液氨 B、漂白粉 C、氯水 D、盐酸
|
|
| 4. | 详细信息 |
|
下列各组物质,按酸、碱、盐、非电解质的顺序排列的是 A. 硫酸、胆矾、氯化镁、二氧化碳 B. 硝酸、烧碱、干冰、苏打水 C. 醋酸、消石灰、明矾、铜 D. 氯化氢、苛性钠、NaHCO3、氨气
|
|
| 5. | 详细信息 |
|
硅及其化合物在材料领域中应用广泛。下列叙述中,正确的是 A. 晶体硅是良好的半导体材料 B. 硅是地壳中含量最多的元素 C. SiO2和酸,碱都可以反应,故为两性氧化物 D. 硅是生产光导纤维的主要原料
|
|
| 6. | 详细信息 |
|
下列说法不正确的是 A. 钠在氧气中燃烧生成的淡黄色的固体Na2O2,可做为呼吸面具的供氧剂 B. 将足量CO2气体通入饱和碳酸钠溶液中,会析出固体 C. 保存硫酸亚铁溶液时应加入一定量的铁粉 D. 向过氧化钠中滴入紫色石蕊试液,溶液先变红后褪色
|
|
| 7. | 详细信息 |
|
下列反应的离子方程式正确的是 A. 铝粉投入到NaOH溶液中:2Al + 2OH- = 2AlO2- + H2↑ B. 小苏打与足量澄清石灰水反应:2HCO3- + Ca2+ + 2OH- =CaCO3↓ + CO32- + 2H2O C. AlCl3溶液中加入足量的氨水:Al3+ + 4NH3·H2O = AlO2- + 4NH4+ + 2H2O D. FeCl2溶液中加入氯水:Cl2 +2Fe2+ =2Fe3+ + 2Cl-
|
|
| 8. | 详细信息 |
|
己知在碱性溶液中可发生如下反应:2R(OH)3+3C1O-+4OH-=2RO4n-+3Cl-+5H2O。则 RO4n-中 R 的化合价是 A. +7 B. +6 C. +5 D. +4
|
|
| 9. | 详细信息 |
|
设NA为阿伏伽德罗常数的值。下列说法正确的是 A. 5NH4NO3 B. 室温下,0.2mol·L-1的Na2SO4溶液中含Na+数目为0.4NA C. 标准状况下,NA个HF分子所占的体积约为22.4L D. 高温下,0.2molFe与足量水蒸气反应,生成的H2分子数目为0.3NA
|
|
| 10. | 详细信息 |
|
下列离子在酸性溶液中能大量共存的是 A. Fe3+、NH4+、SCN-、Cl- B. Na+、Mg2+、NO C. Al3+、Fe2+、NO
|
|
| 11. | 详细信息 |
|
吸入人体內的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体內的活性氧,由此推断Na2SeO3的作用是 A. 作还原剂 B. 作氧化剂 C. 既作氧化剂又作还原剂 D. 既不作氧化剂又不作还原剂
|
|
| 12. | 详细信息 |
|
将一定量的Na2CO3与NaHCO3的混合物充分加热,可收集到标况下 A.
|
|
| 13. | 详细信息 |
|
盐酸广泛应用在稀有金属的湿法冶金、漂染工业、金属加工、无机药品及有机药物的生产等领域中。HCl 极易溶于水,工业上用 HCl 气体溶于水的方法制取盐酸。 (1)用 12.0mol/L 浓盐酸配置 230mL 0.3mol/L 的稀盐酸,需要量取浓盐酸的体积为___mL; (2)溶液稀释过程中需要的玻璃仪器有烧杯、玻璃棒、量筒、____________、___________; (3)溶液稀释过程中有以下操作: a.量取浓盐酸和一定体积的水,在烧杯中稀释 b.计算所需浓盐酸的体积 c.上下颠倒摇匀 d.加蒸馏水至刻度线 1-2cm 地方,改用胶头滴管加蒸馏水至凹液面与刻度线相切 e.将稀释液转移入容量瓶,洗涤烧杯和玻璃棒,并将洗涤液转移入容量瓶,振荡 以上正确的操作顺序为____________________________________________(填序号); (4)实验过程中的以下操作会导致最终所配溶液浓度(填“偏大”、“偏小”或“不变”) a.量取浓盐酸时俯视:______________________; b.量取浓盐酸后,清洗了量筒并将洗涤液转移入容量瓶:______________________; c.实验前,容量瓶中有少量残留蒸馏水:______________________; (5)标准状况,1L 水中通入 aL HCl 气体,忽略盐酸溶液中 HCl 的挥发,得到的盐酸溶液密度为 b g/mL,物质的量浓度为 ______________________mol/L。
|
|
| 14. | 详细信息 |
|
某溶液只可能含有K+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、CO32-、SO42-中的若干种离子。某同学取100 mL的溶液分成两等份进行如下实验: ①第一份加过量的氢氧化钠溶液后加热,收集到0.05 mol有刺激性气味的气体,同时得到澄清溶液甲。 ②向溶液甲中通入过量的二氧化碳气体,生成白色沉淀,沉淀经过滤,洗涤灼烧后,得到1.02 g固体。 ③第二份加足量的氯化钡溶液后,生成白色沉淀,加入足量盐酸,沉淀并不溶解,过滤沉淀,充分洗涤,干燥,得到11.65 g固体。 (1)在原溶液中一定存在的离子有_________________________________;一定不存在的离子有_____________________;不能确定是否存在的离子有___________。 (2)为了确定不能确定的离子是否存在,可以采取的方法为__________________________________。 (3)由操作②确定的离子在溶液中的浓度为___________。
|
|
| 15. | 详细信息 |
|
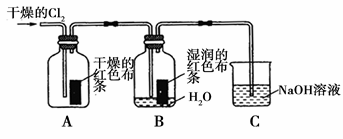
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。某化学兴趣小组同学对氯气的性质进行如下探究: (1)兴趣小组同学按下图装置进行实验,探究Cl2的漂白性。
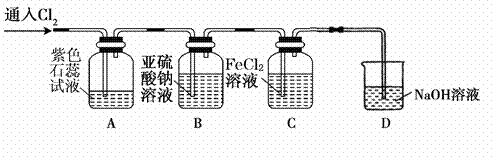
①通入Cl2 后,观察到的现象是 根据现象可得出的结论是 。 ②集气瓶B发生反应的离子方程式是 。 ③C装置的作用是 ,若有2.24L(标准状况下)Cl2被NaOH溶液完全吸收,则反应过程中转移的电子为 mol。 (2)兴趣小组同学按下图装置进行实验,探究Cl2的氧化性。
①实验开始后,观察装置A 中的现象是 。 ②装置C中发生反应的离子方程式是 。 ③停止通入氯气,取装置B中少量溶液于洁净的试管中,向其中滴加足量稀盐酸,再向其中滴加氯化钡溶液,有白色沉淀生成。则通入Cl2时装置B中发生反应的离子方程式是 。
|
|
| 16. | 详细信息 |
|
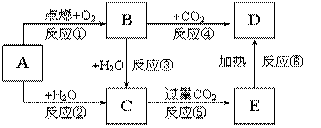
下边图示中,A为一种常见的单质,B、C、D 、E是含有A元素的常见化合物。它们的焰色反应均为黄色。 (1)写出下列物质的化学式: B___________ E___________ (2)以上反应中属于氧化还原反应的有__________________(填写编号) (3)写出B→C反应的离子方程式并用单线桥标出电子转移方向和数目 _______________ E→D的化学方程式 ________________________________________________ (4)加热5.00g D和E的固体混合物,使E完全分解,固体混合物的质量减少了0. 31g,则原混合物中D的质量为_________。 |
|