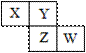2019广东高一下学期人教版(2019)高中化学期末考试
| 1. | 详细信息 |
|
中国科学技术名词审定委员会已确定第116号元素Lv的名称为鉝.关于293116Lv的叙述错误的是 A. 原子序数116 B. 中子数177 C. 在第ⅥA族 D. 核电荷数293
|
|
| 2. | 详细信息 |
|
下列物质中,属于含有共价键的离子化合物是 A. Ba(OH)2 B. CaCl2 C. H2SO4 D. NH3
|
|
| 3. | 详细信息 |
|
下列化学用语的书写正确的是 A. F原子结构示意图: C. 乙烯的结构简式: C2H4 D. 苯的分子式:C6H6
|
|
| 4. | 详细信息 |
|
适宜用分液漏斗进行分离的一组混合物是 A. 乙醇和乙酸乙酯 B. 水和氯化钠 C. 水和花生油 D. 四氯化碳和碘
|
|
| 5. | 详细信息 | ||||||||
|
.下列我国科研成果所涉及材料中,主要成分为同主族元素形成的无机非金属材料的是
A. A B. B C. C D. D
|
|||||||||
| 6. | 详细信息 |
|
下列各种金属冶炼方法中,不能制得相应金属的是 A. 加热氧化汞 B. 氧化铁和铝粉高温共热 C. 电解熔融氯化钠 D. 高温煅烧碳酸钙
|
|
| 7. | 详细信息 |
|
海水是一个巨大的化学资源库,下列有关海水综合利用的说法正确的是( ) A. 海水中含有钾元素,只需经过物理变化能得到钾单质 B. 海水蒸发制海盐的过程中只发生了化学变化 C. 从海水中可以得到NaCl,电解熔融NaCl可制备Na D. 利用潮汐发电是将化学能转化为电能
|
|
| 8. | 详细信息 |
|
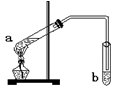
“酒是陈的香”,是因为酒在储存过程中生成了有香味的乙酸乙酯。在实验室我们可以用如图所示的装置来制取乙酸乙酯。关于该实验的说法不正确的是
A. a试管中发生的反应是酯化反应,原理是乙酸脱去羟基、乙醇脱氢 B. b试管中所盛的试剂是NaOH C. 反应后b中可以看到明显 D. 试管b中的导管要在液面的稍上方,不能插入液面以下,是为了防止倒吸
|
|
| 9. | 详细信息 |
|
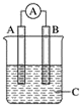
如图所示装置,电流表指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的( )
A. A是Zn,B是Cu,C为稀硫酸 B. A是Cu,B是Zn,C为稀硫酸 C. A是Fe,B是Ag,C为稀AgNO3溶液 D. A是Ag,B是Fe,C为稀AgNO3溶液
|
|
| 10. | 详细信息 |
|
下列说法正确的是 A. 甲烷、汽油、酒精都是可燃性烃,都可作燃料 B. 可食用植物油含有的高级脂肪酸甘油酯是人体的营养物质 C. 淀粉、蛋白质、葡萄糖都是高分子化合物 D. 石油的分馏、煤的液化和气化都是物理变化,石油的裂化、裂解都是化学变化
|
|
| 11. | 详细信息 |
|
.以下是反应A(g) + 3B(g) ⇌2C(g) + 2D(g) 在四种不同情况下的反应速率,反应速率最大的是 A. υ(A)=0.45mol·L-1·s-1 B. υ(B)=0.6mol·L-1·s-1 C. υ(C)=0.4mol·L-1·s-1 D. υ(D)=0.45mol·L-1·s-1
|
|
| 12. | 详细信息 |
|
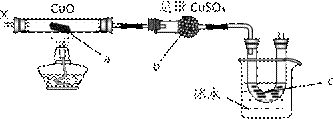
按如图装置,持续通入X气体,可以看到a处有红色物质生成,b处变蓝,c处得到液体,则X气体是( )
A. (CH3)3COH (气) B. NH3 C. CH3CH2CH2OH(气) D. CO和H2
|
|
| 13. | 详细信息 |
|
下列有关电池的说法不正确的是( ) A. 手机上用的锂离子电池属于二次电池 B. 锌锰干电池中,锌电极是负极 C. 氢氧燃料电池可把化学能转化为电能 D. 铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
|
|
| 14. | 详细信息 |
|
下列反应中,属于加成反应 A. CH3CH=CH2+Br2 C. CH3COOH+CH3OH
|
|
| 15. | 详细信息 |
|
工业制硫酸中的一步重要反应是SO2的催化氧化:2SO2+O2⇌2SO3(正反应放热),下列有关说法正确的是 A. 升高温度只提高逆反应速率 B. 降低温度可提高正反应速率 C. 使用催化剂能显著增大反应速率 D. 达到化学平衡时正、逆反应速率相等且等于0
|
|
| 16. | 详细信息 |
|
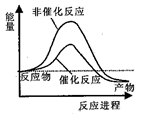
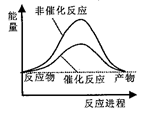
据报道,科学家开发出了利用太阳能分解水的新型催化剂。下列有关水分解过程的能量变化示意图正确的是 A. C.
|
|
| 17. | 详细信息 |
|
某有机物A的结构为 A. 1 mol A能跟2 mol NaOH溶液反应 B. 能发生加聚反应 C. 不能发生分子内酯化反应 D. A分子中所有原子在同一平面上
|
|
| 18. | 详细信息 |
|
X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示。Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是
A. 原子半径:Z > Y > X B. 氢化物稳定性:X > Y C. 氢化物沸点:Z > Y D. 最高价氧化物对应的水化物酸性:W > Z
|
|
| 19. | 详细信息 |
|
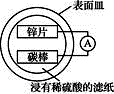
有一种可做融雪剂的盐,其主要成分的化学式为XY2 , X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1mol XY2含有54mol电子。 (1)该融雪剂的化学式是_________;用电子式表示XY2的形成过程__________________。 (2)主族元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻, 则D的离子结构示意图是_________;D与E能形成一种类似于CO2的三原子分子,且每个原子均达到了8e−稳定结构,该分子的化学键类型为_________(填“离子键”或“共价键”)。 (3)用化学式回答: ①D与Y的氢化物稳定性________>________; ②D与Y的最高价氧化物对应水化物酸性________>________。 (4)某兴趣小组设计的简易原电池装置如下图所示。回答下列问题:
①锌片为_____极(填“正”或“负”)。 ②电池正极的现象是_________________,其电极反应式为_____________________。 ③电流由_______经导线流向______(填“锌片”或“碳棒”)。
|
|
| 20. | 详细信息 | ||||||||||||
|
化学反应速率与限度与生产、生活密切相关 (1)某学生为了探究锌与盐酸反应过程中的速率变化,他在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
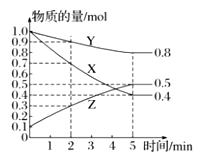
①哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大___________。 ②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率______________。(设溶液体积不变) (2)另一学生也做同样的实验,由于反应太快,不好控制测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是_________。 A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液 (3)某温度下在4L密闭容器中,3种气态物质X、Y、Z的物质的量随时间变化曲线如图。
①该反应的化学方程式是__________________________。 ②在5min时,该反应达到了平衡状态,下列可作为判断反应已达到该状态的是_______。 A.X、Y、Z的反应速率相等 B.容器内气体压强保持不变 C.X、Y的反应速率比为3:1 D.生成1mol Y的同时生成2mol Z ③2min内X的转化率为_____________________。
|
|||||||||||||
| 21. | 详细信息 | ||||||||||||||||
|
.溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
按下列合成步骤回答问题: (1)在a中加入15mL无水苯和少量铁屑。在b中小心加入4.0mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了______气体。该反应为_______(填“吸热”或“放热”)反应,冷却水流向是_____________(填“上进下出”或“下进上出”),继续滴加至液溴滴完。其中仪器c的名称是________,其作用是:__________________________________。装置d的作用是:_____________________________________________________;烧瓶中发生的有机反应的方程式为:_______________________________________________。 (2)液溴滴完后,经过下列步骤分离提纯: ①向a中加入10mL水,然后过滤除去未反应的铁屑; ②滤液依次用10mL水、8mL 10%的NaOH溶液、10mL水洗涤。洗涤、分离有机和无机试剂,需要用到的仪器是:_____________。第一次水洗除去大部分的HBr;用NaOH溶液洗涤的作用是______________;第二次水洗的目的是:____________;每一次洗涤,有机层从_________(填“下口放出”或“上口倒出”),棕黄色的溴苯经过提纯后恢复为无色。 ③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是_____________。 (3)经以上分离操作后,粗溴苯中还含有的主要杂质苯,要进一步提纯,下列操作中必须的是____(填入正确选项前的字母)。 A.蒸馏 B.渗析 C.分液 D.萃取
|
|||||||||||||||||
 B. 四氯化碳的电子式:
B. 四氯化碳的电子式: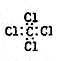




 B.
B. 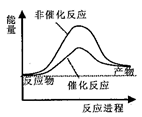
 D.
D. 
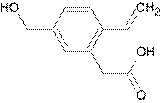 , 下列有关说法正确的是
, 下列有关说法正确的是