2020е№ҝиҘҝй«ҳдәҢдёӢеӯҰжңҹдәәж•ҷзүҲ(2019)й«ҳдёӯеҢ–еӯҰжңҲиҖғиҜ•еҚ·
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
ж №жҚ®еӣҫзӨәеЎ«з©ә
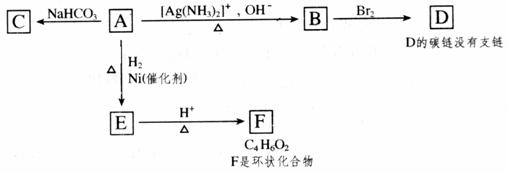
пјҲ1пјүеҢ–еҗҲзү© A еҗ«жңүзҡ„е®ҳиғҪеӣўжҳҜ____________________________ пјҲ2пјү1mol A дёҺ2mol H2 еҸ‘з”ҹеҸҚеә”з”ҹжҲҗ 1mol EпјҢе…¶еҸҚеә”ж–№зЁӢејҸжҳҜ____________________________________________________________ пјҲ3пјүдёҺ A е…·жңүзӣёеҗҢе®ҳиғҪеӣўзҡ„ A зҡ„еҗҢеҲҶејӮжһ„дҪ“зҡ„з»“жһ„з®ҖејҸжҳҜ_____________________________________________________________ пјҲ4пјүB еңЁй…ёжҖ§жқЎд»¶дёӢдёҺ Br2 еҸҚеә”еҫ—еҲ° DпјҢD зҡ„з»“жһ„з®ҖејҸжҳҜ________________________________ пјҲ5пјүF зҡ„з»“жһ„з®ҖејҸжҳҜ____________________;з”ұ E з”ҹжҲҗ F зҡ„еҸҚеә”зұ»еһӢжҳҜ______________гҖӮ
|
|
| 2. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||
|
жҹҗз ”з©¶жҖ§еӯҰд№ е°Ҹз»„зҡ„еӯҰз”ҹз”Ёж ҮеҮҶжө“еәҰзҡ„ж°ўж°§еҢ–й’ жә¶ж¶ІжөӢе®ҡжңӘзҹҘжө“еәҰзҡ„зӣҗй…ёжә¶ж¶ІпјҺ
пјҲ1пјүиҜҘеӯҰз”ҹжҢҮзӨәеүӮе’ҢиЈ…ж ҮеҮҶж¶Ізҡ„д»ӘеҷЁйҖүз”ЁжӯЈзЎ®зҡ„дёҖз»„жҳҜ ________пјҲеҶҷзј–еҸ·пјү пјҲ2пјүе®һйӘҢдёӯз”Ёе·ҰжүӢжҺ§еҲ¶ж»ҙе®ҡз®ЎдёҠж©Ўиғ¶з®ЎеҶ…зҡ„зҺ»з’ғзҸ пјҢзңјзқӣжіЁи§Ҷй”ҘеҪўз“¶дёӯжә¶ж¶Ізҡ„йўңиүІеҸҳеҢ–пјҢзӣҙиҮіж»ҙе®ҡз»ҲзӮ№пјҺеҲӨж–ӯеҲ°иҫҫз»ҲзӮ№зҡ„зҺ°иұЎпјҡ____________________________________________________________ пјҲ3пјүе·ІзҹҘж»ҙе®ҡз®ЎдёӯиЈ…жңүжө“еәҰдёә0.1000mol/Lзҡ„ж°ўж°§еҢ–й’ пјҺйҖҗж»ҙеҠ е…ҘеҲ°иЈ…жңүзӣҗй…ёжә¶ж¶Ізҡ„й”ҘеҪўз“¶дёӯпјҺејҖе§Ӣж—¶иҜ»ж•°еҸҠжҒ°еҘҪеҸҚеә”ж—¶ж°ўж°§еҢ–й’ жә¶ж¶Ізҡ„иҜ»ж•°и§ҒдёӢиЎЁпјҺ
иҜ·и®Ўз®—еҫ…жөӢзҡ„зӣҗй…ёзҡ„зү©иҙЁзҡ„йҮҸжө“еәҰ ________В mol/L пјҲ4пјүдёӢйқўж“ҚдҪңдјҡеҜјиҮҙеҫ…жөӢзӣҗй…ёзҡ„жө“еәҰеҒҸеӨ§зҡ„жҳҜВ ___________пјҲеҶҷзј–еҸ·пјү
|
|||||||||||||||||
| 3. | иҜҰз»ҶдҝЎжҒҜ |
|
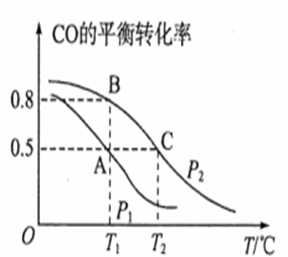
з”ІйҶҮжҳҜдёҖз§ҚйҮҚиҰҒзҡ„еҢ–е·ҘеҺҹж–ҷпјҢеҸҲжҳҜдёҖз§ҚеҸҜеҶҚз”ҹиғҪжәҗпјҢе…·жңүејҖеҸ‘е’Ңеә”з”Ёзҡ„е№ҝйҳ”еүҚжҷҜгҖӮ пјҲ1пјүВ В В еңЁдёҖе®№з§Ҝдёә2Lзҡ„еҜҶй—ӯе®№еҷЁеҶ…пјҢе……е…Ҙ0.2mol COдёҺ0.4mol H2еҸ‘з”ҹеҸҚеә”еҰӮдёӢпјҡ CO(g)+2H2(g)
в‘ В В В В AгҖҒBдёӨзӮ№еҜ№еә”зҡ„еҺӢејәеӨ§е°Ҹе…ізі»жҳҜPA________PBпјҲеЎ«вҖң>гҖҒ<гҖҒ=вҖқпјүгҖӮ в‘ЎВ В В В AгҖҒBгҖҒCдёүзӮ№зҡ„е№іиЎЎеёёж•°KAпјҢKBпјҢKC зҡ„еӨ§е°Ҹе…ізі»жҳҜ__________________гҖӮ в‘ўдёӢеҲ—еҸҷиҝ°иғҪиҜҙжҳҺдёҠиҝ°еҸҚеә”иғҪиҫҫеҲ°еҢ–еӯҰ е№іиЎЎзҠ¶жҖҒзҡ„жҳҜ __________________(еЎ«д»ЈеҸ·) гҖӮ aпјҺH2зҡ„ж¶ҲиҖ—йҖҹзҺҮжҳҜCH3OHз”ҹжҲҗйҖҹзҺҮзҡ„2еҖҚВ В В В В В В bпјҺCH3OHзҡ„дҪ“з§ҜеҲҶж•°дёҚеҶҚж”№еҸҳ cпјҺж··еҗҲж°”дҪ“зҡ„еҜҶеәҰдёҚеҶҚж”№еҸҳВ В В В В В В В В В В В В В В В В dпјҺCOе’ҢCH3OHзҡ„зү©иҙЁзҡ„йҮҸд№Ӣе’ҢдҝқжҢҒдёҚеҸҳ пјҲ2пјүеңЁP1еҺӢејәгҖҒT1в„ғж—¶пјҢиҜҘеҸҚеә”зҡ„е№іиЎЎеёёж•°K=__________________пјҢеҶҚеҠ е…Ҙ1.0mol COеҗҺйҮҚж–°еҲ°иҫҫе№іиЎЎпјҢеҲҷCOзҡ„иҪ¬еҢ–зҺҮ___________пјҲеЎ«вҖңеўһеӨ§пјҢдёҚеҸҳжҲ–еҮҸе°ҸвҖқпјүгҖӮ
|
|
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
еңЁзҒ«з®ӯжҺЁиҝӣеҷЁдёӯиЈ…жңүејәиҝҳеҺҹеүӮиӮј(N2H4)е’Ңејәж°§еҢ–еүӮ(H2O2)пјҢеҪ“е®ғ们混еҗҲж—¶пјҢеҚідә§з”ҹN2е’Ңж°ҙи’ёж°”пјҢ并ж”ҫеҮәеӨ§йҮҸзғӯгҖӮе·ІзҹҘ0.4molж¶ІжҖҒиӮје’Ңи¶ійҮҸH2O2еҸҚеә”пјҢз”ҹжҲҗж°®ж°”е’Ңж°ҙи’ёж°”пјҢж”ҫеҮә256kJзҡ„зғӯйҮҸгҖӮ пјҲ1пјүеҶҷеҮәиҜҘеҸҚеә”зҡ„зғӯеҢ–еӯҰж–№зЁӢејҸ__________________________________________гҖӮ пјҲ2пјүдёҠиҝ°еҸҚеә”еә”з”ЁдәҺзҒ«з®ӯжҺЁиҝӣеүӮпјҢйҷӨйҮҠж”ҫеӨ§йҮҸзҡ„зғӯе’Ңеҝ«йҖҹдә§з”ҹеӨ§йҮҸж°”дҪ“еӨ–пјҢиҝҳжңүдёҖдёӘеҫҲзӘҒеҮәзҡ„дјҳзӮ№жҳҜ______________________________________ пјҲ3пјүе·ҘдёҡдёҠз”ЁCO2е’ҢH2еҸҚеә”еҗҲжҲҗдәҢз”ІйҶҡгҖӮе·ІзҹҘпјҡ CO2(g)пјӢ3H2(g) === CH3OH(g)пјӢH2O(g)В В О”H1пјқпјҚ53.7kJВ·molпјҚ1 CH3OCH3(g)пјӢH2O(g) === 2CH3OH(g)В В О”H2пјқпјӢ23.4kJВ·molпјҚ1 еҲҷ2CO2(g)пјӢ6H2(g) === CH3OCH3(g)пјӢ3H2O(g)гҖҖО”H3пјқ________kJВ·mol пјҲ4пјүз”ЁзҰ»еӯҗж–№зЁӢејҸиЎЁзӨәзўій…ёй’ жә¶ж¶ІжҳҫзўұжҖ§зҡ„еҺҹеӣ пјҡ___________________В В В В В В В гҖӮ
|
|
| 5. | иҜҰз»ҶдҝЎжҒҜ |
|
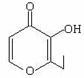
еӨ®и§Ҷз„ҰзӮ№и®ҝи°ҲиҠӮзӣ®жӣҫжҠҘйҒ“пјҢдҝ—з§°вҖңдёҖж»ҙйҰҷвҖқзҡ„жңүжҜ’зү©иҙЁиў«дәәйЈҹз”ЁеҗҺдјҡжҚҹдјӨиӮқи„ҸпјҢиҝҳиғҪиҮҙзҷҢгҖӮвҖңдёҖж»ҙйҰҷвҖқзҡ„еҲҶеӯҗз»“жһ„еҰӮеҸідёӢеӣҫжүҖзӨәпјҢдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜ В (В В В В )
AпјҺиҜҘжңүжңәзү©зҡ„еҲҶеӯҗејҸдёәC7H6O3 BпјҺ1 molиҜҘжңүжңәзү©жңҖеӨҡиғҪдёҺ2 mol H2еҸ‘з”ҹеҠ жҲҗеҸҚеә” CпјҺиҜҘжңүжңәзү©зҡ„дёҖз§ҚиҠійҰҷж—ҸеҗҢеҲҶејӮжһ„дҪ“иғҪеҸ‘з”ҹ银й•ңеҸҚеә” DпјҺиҜҘжңүжңәзү©иғҪеҸ‘з”ҹеҸ–д»ЈгҖҒеҠ жҲҗгҖҒж°§еҢ–е’ҢиҝҳеҺҹеҸҚеә”
|
|
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
е®Өжё©ж—¶пјҢе°Ҷжө“еәҰе’ҢдҪ“з§ҜеҲҶеҲ«дёәC1гҖҒV1зҡ„NaOHжә¶ж¶Іе’ҢC2гҖҒV2зҡ„CH3COOHжә¶ж¶Ізӣёж··еҗҲпјҢдёӢеҲ—е…ідәҺиҜҘж··еҗҲжә¶ж¶Ізҡ„еҸҷиҝ°й”ҷиҜҜзҡ„жҳҜпјҲВ В пјү AпјҺиӢҘpHпјһ7пјҢеҲҷдёҖе®ҡжҳҜC1V1пјқC2V2В В В В В В В В В В В В В В В В В В В В BпјҺеңЁд»»дҪ•жғ…еҶөдёӢйғҪжҳҜC(Na+)пјӢC(H+)пјқC(CH3COO-)пјӢC(OH-) CпјҺеҪ“pH=7ж—¶пјҢиӢҘV1пјқV2пјҢдёҖе®ҡжҳҜC2пјһC1В В В В В В В В DпјҺиӢҘV1пјқV2пјҢC1пјқC2пјҢеҲҷC(CH3COO-)пјӢC(CH3COOH)=C(Na+)
|
|
| 7. | иҜҰз»ҶдҝЎжҒҜ |
|
еҜ№ж»ҙжңүй…ҡй…һиҜ•ж¶Ізҡ„Na2CO3жә¶ж¶ІпјҢдёӢеҲ—ж“ҚдҪңеҗҺзәўиүІдјҡеҠ ж·ұзҡ„жҳҜВ (В В В В ) AпјҺйҷҚжё© В В В BпјҺйҖҡе…ҘCO2ж°”дҪ“В В В CпјҺеҠ е…Ҙе°‘йҮҸCaCl2еӣәдҪ“ В В В В DпјҺеҠ е…Ҙе°‘йҮҸNaOHеӣәдҪ“
|
|
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜВ В (В В В В ) A. 50в„ғж—¶пјҢж°ҙеңЁ0.1mol/Lзӣҗй…ёдёӯдёҺеңЁ0.1mol/LNaOHжә¶ж¶Ідёӯзҡ„з”өзҰ»зЁӢеәҰзӣёеҗҢ B. pHзӯүдәҺ7зҡ„жә¶ж¶ІдёҖе®ҡе‘ҲдёӯжҖ§ C. ж°ҙзҡ„зҰ»еӯҗз§ҜиЎЁзӨәеңЁж°ҙжә¶ж¶Ідёӯз”ұж°ҙз”өзҰ»еҮәзҡ„H+е’ҢOH-жө“еәҰз¬ҰеҗҲKw = cпјҲH+пјүВ·cпјҲOH-пјү D. е°Ҷ0.06 molВ·L-1ж°ўж°§еҢ–й’Ўжә¶ж¶ІдёҺ0.1 molВ·L-1зӣҗй…ёжә¶ж¶ІзӯүдҪ“з§Ҝж··еҗҲпјҢиҜҘж··еҗҲжә¶ж¶Ізҡ„pHзӯүдәҺ13пјҲеҝҪз•Ҙж··еҗҲиҝҮзЁӢдёӯжә¶ж¶ІдҪ“з§ҜеҸҳеҢ–пјү
|
|
| 9. | иҜҰз»ҶдҝЎжҒҜ |
|
дёәдәҶдҪҝй…ҚеҲ¶зҡ„NH4Clжә¶ж¶Ідёӯ AпјҺHClВ В В В В В В В В В В В В BпјҺNaClВ В В В В В В В В В В В CпјҺж°Ёж°ҙВ В В В В В В В В В В В DпјҺNaOH
|
|
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
дёҚиғҪиҜҒжҳҺд№ҷй…ёжҳҜејұй…ёзҡ„е®һйӘҢдәӢе®һжҳҜ В (В В В ) AпјҺ pH=1зҡ„CH3COOHжә¶ж¶ІеҠ ж°ҙзЁҖйҮҠеҲ°10еҖҚпјҢжөӢеҫ—pHпјң2 BпјҺеёёжё©дёӢ0.1 mol/L CH3COOHжә¶ж¶Ізҡ„pH=3 CпјҺ CH3COOHжә¶ж¶ІдёӯеҠ е…Ҙе°‘йҮҸйҶӢй…ёй’ еӣәдҪ“пјҢжә¶ж¶ІpHеўһеӨ§ DпјҺ 0.1 mol/L CH3COOHжә¶ж¶ІеҸҜдҪҝзҙ«иүІзҹіи•ҠеҸҳзәў
|
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
еёёжё©дёӢпјҢеҸ–жө“еәҰзӣёеҗҢзҡ„NaOHе’ҢHClжә¶ж¶ІпјҢд»Ҙ3вҲ¶2дҪ“з§ҜжҜ”зӣёж··еҗҲпјҢжүҖеҫ—жә¶ж¶Ізҡ„pHзӯүдәҺ12пјҢеҲҷеҺҹжә¶ж¶Ізҡ„жө“еәҰдёә пјҲВ В В пјү AпјҺ0.01molВ·LпјҚ1 В В В BпјҺ0.017molВ·LпјҚ1 В В CпјҺ0.05molВ·LпјҚ1 DпјҺ0.50molВ·LпјҚ1
|
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
йҶӢй…ёзҡ„з”өзҰ»ж–№зЁӢејҸдёәCH3COOH(aq)вҮҢHпјӢ(aq)+CH3COOпјҚ(aq) В О”Hпјһ0пјҢ25в„ғж—¶пјҢ0.1mol/LйҶӢй…ёжә¶ж¶ІKa=1.75Г—10-5 (Ka иЎЁзӨәй…ёзҡ„з”өзҰ»еёёж•°)гҖӮдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲ В В В пјү AпјҺеҚҮй«ҳжё©еәҰпјҢc(HпјӢ)еўһеӨ§пјҢKaеҸҳеӨ§ BпјҺиҜҘжә¶ж¶ІдёӯеҠ е°‘йҮҸCH3COONaеӣәдҪ“пјҢе№іиЎЎжӯЈеҗ‘移еҠЁ CпјҺиҜҘжё©еәҰдёӢ0.01mol/LйҶӢй…ёжә¶ж¶ІKaпјң1.75Г—10-5 DпјҺеҗ‘иҜҘжә¶ж¶Ідёӯж»ҙеҠ еҮ ж»ҙжө“зӣҗй…ёпјҢе№іиЎЎйҖҶеҗ‘移еҠЁпјҢc(HпјӢ)еҮҸе°Ҹ
|
|
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
зӣҗзұ»ж°ҙи§ЈеңЁе·ҘеҶңдёҡз”ҹдә§е’Ңж—Ҙеёёз”ҹжҙ»дёӯжңүзқҖе№ҝжіӣзҡ„еә”з”ЁпјҢжңүе…іеә”з”ЁжҲ–иҜҙжі•дёҺзӣҗзұ»ж°ҙи§Јж— е…ізҡ„жҳҜпјҲВ В пјү В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В AпјҺз”Ёзғӯзҡ„зәҜзўұжә¶ж¶Іжҙ—ж¶ӨйӨҗе…·дёҠзҡ„жІ№жұЎ В В В В В В BпјҺз”ҹжҙ»дёӯеёёз”ЁжҳҺзҹҫеҮҖж°ҙ CпјҺз”ЁзЁҖзЎ«й…ёжҲ–жө“ж°Ёж°ҙйҷӨеҺ»й“ңеҷЁиЎЁйқўзҡ„й“ңз»ҝ DпјҺй•ҝжңҹдҪҝз”ЁзЎ«й…ёй“өеҢ–иӮҘзҡ„еңҹеЈӨпјҢжҳ“еҸҳй…ёжҖ§пјҢеҸҜж–Ҫз”ЁйҖӮйҮҸзҡ„зҶҹзҹізҒ°
|
|
| 14. | иҜҰз»ҶдҝЎжҒҜ |
|
иӢҘжә¶ж¶Ідёӯз”ұж°ҙз”өзҰ»дә§з”ҹзҡ„ гҖҖгҖҖ
|
|
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зү©иҙЁзҡ„ж°ҙжә¶ж¶Із»ҸеҠ зғӯжө“зј©пјҢи’ёе№ІзҒјзғ§д»ҚиғҪеҫ—еҲ°еҺҹзү©иҙЁзҡ„жҳҜпјҲВ В В В пјү AпјҺFeCl3В В В В В В BпјҺCa(HCO3)2В В В В В В В В CпјҺNaAlO2В В В В В В В В В DпјҺNa2SO3
|
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
|
жө…з»ҝиүІзҡ„Fe(NO3)2жә¶ж¶ІдёӯпјҢеӯҳеңЁж°ҙи§Је№іиЎЎпјҡFe2++2H2O AпјҺжө…з»ҝиүІз•ҘеҸҳж·ұВ В В В В В В В В В В В В В В В В В В В В В В В BпјҺйўңиүІеҹәжң¬дёҚеҸҳ В В В В CпјҺеҸҳй»„В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В DпјҺеҸҳдёәзәўиӨҗиүІ.
|
|
| 17. | иҜҰз»ҶдҝЎжҒҜ |
|
еңЁдёҖжҒ’жё©жҒ’еҺӢзҡ„еҜҶй—ӯе®№еҷЁдёӯпјҢN2дёҺH2зҡ„еҸҚеә”д»Ҙиҫҫе№іиЎЎпјҢиӢҘеҶҚеҗ‘дҪ“зі»дёӯе……е…Ҙж°©ж°”е№іиЎЎе°Ҷ В (В В В ) В В AпјҺеҗ‘е·Ұ移еҠЁВ В В В В В BпјҺеҗ‘еҸіз§»еҠЁВ В В В В В В CпјҺдёҚ移еҠЁВ В В В В В В В DпјҺ移еҠЁж–№еҗ‘дёҚе®ҡ
|
|
| 18. | иҜҰз»ҶдҝЎжҒҜ |
|
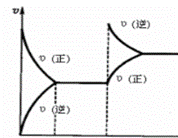
еңЁеҜҶй—ӯе®№еҷЁпјҢдёҖе®ҡжқЎд»¶дёӢиҝӣиЎҢеҸҚеә”пјҡmA(g)+nB(g)В
В AпјҺm+nпјңp+qВ В В В В В В В В В В В BпјҺйҖҶеҸҚеә”жҳҜж”ҫзғӯеҸҚеә” В CпјҺm+nпјһp+qВ В В В В В В В В В В В DпјҺжӯЈеҸҚеә”жҳҜеҗёзғӯеҸҚеә”
|
|
| 19. | иҜҰз»ҶдҝЎжҒҜ |
|
еңЁдёҖе®ҡжқЎд»¶дёӢпјҢеҸҚеә”N2+3H2==2NH3пјҢеңЁ2LеҜҶй—ӯе®№еҷЁдёӯиҝӣиЎҢпјҢ5minеҶ…ж°Ёзҡ„иҙЁйҮҸеўһеҠ дәҶ1.7gпјҢеҲҷеҸҚеә”йҖҹзҺҮдёә В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В (В В В В ) В В В AпјҺV(H2)=0.03mol/LВ·minгҖҖгҖҖВ В BпјҺV(N2)=0.02mol/LВ·min В В В CпјҺV(NH3)=0.17mol/LВ·minгҖҖ В В В DпјҺV(NH3)=0.01mol/LВ·min
|
|
| 20. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҢ–еӯҰеҸҚеә”еұһдәҺеҗёзғӯеҸҚеә”зҡ„жҳҜ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В (В В В В ) AпјҺзўҳзҡ„еҚҮеҚҺВ В В В В В В В В В В В В В В В В В В В В В В В В BпјҺж°ўж°§еҢ–й’ҷдёҺж°ҜеҢ–й“өжҷ¶дҪ“ж··еҗҲ CпјҺй•ҒдёҺзЁҖзӣҗй…ёеҸҚеә”В В В В В В В В В В В В В В В В В В В DпјҺз”ҹзҹізҒ°жә¶дәҺж°ҙ
|
|
- йҷ•иҘҝй«ҳдёҖеҢ–еӯҰ2018е№ҙдёҠжңҹжңҹдёӯиҖғиҜ•еёҰеҸӮиҖғзӯ”жЎҲдёҺи§Јжһҗ
- 2019еұҠй«ҳдёүдёӢеҚҠжңҹй«ҳиҖғжЁЎжӢҹеҢ–еӯҰпјҲеӨ©жҙҘеёӮд№қж ЎиҒ”иҖғпјү
- е№ҝе·һеёӮй«ҳдёүеҢ–еӯҰдёҠеҶҢдё“йўҳз»ғд№ еҗҢжӯҘиҖғиҜ•жЈҖжөӢ
- иҘҝи—ҸиҮӘжІ»еҢәжһ—иҠқеёӮ第дәҢй«ҳзә§дёӯеӯҰ2020еұҠй«ҳдёүдёҠеҚҠе№ҙ第дёҖж¬ЎжңҲиҖғзҗҶ科综еҗҲеҢ–еӯҰиҜ•еҚ·еёҰеҸӮиҖғзӯ”жЎҲе’Ңи§Јжһҗ
- е№ҝдёң2020е№ҙй«ҳдёүдёҠжңҹеҢ–еӯҰж— зәёиҜ•еҚ·
- жӯҰжұүеёӮй«ҳдёҖеҢ–еӯҰдёҠеҶҢжңҹжң«иҖғиҜ•е…Қиҙ№иҜ•еҚ·е®Ңж•ҙзүҲ
- дёҠжө·еёӮй«ҳдёүеҢ–еӯҰдёҠеҶҢжңҲиҖғиҜ•еҚ·еңЁзәҝжөӢйӘҢе®Ңж•ҙзүҲ
- й«ҳдёҖеҢ–еӯҰдёӢеҶҢеҚ•е…ғжөӢиҜ•еҗҢжӯҘиҖғиҜ•жЈҖжөӢ