2018еҗүжһ—й«ҳдёүдёҠеӯҰжңҹдәәж•ҷзүҲй«ҳдёӯеҢ–еӯҰжңҲиҖғиҜ•еҚ·
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
еҢ–еӯҰдёҺз”ҹжҙ»еҸҠзӨҫдјҡеҸ‘еұ•жҒҜжҒҜзӣёе…іпјҢдёӢеҲ—жңүе…іиҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜпјҲВ В В В В пјү AпјҺвҖңйқ’и’ҝдёҖжҸЎпјҢд»Ҙж°ҙдәҢеҚҮжёҚпјҢз»һеҸ–жұҒвҖқпјҢеұ е‘Ұе‘ҰеҜ№йқ’и’ҝзҙ зҡ„жҸҗеҸ–еұһдәҺеҢ–еӯҰеҸҳеҢ– BпјҺвҖңйңҫе°ҳз§ҜиҒҡйҡҫи§Ғи·ҜдәәвҖқпјҢйӣҫйңҫжүҖеҪўжҲҗзҡ„ж°”жә¶иғ¶жңүдёҒиҫҫе°”ж•Ҳеә” CпјҺвҖңзҶ¬иғҶзҹҫй“ҒйҮңпјҢд№…д№ӢдәҰеҢ–дёәй“ңвҖқпјҢиҜҘиҝҮзЁӢеҸ‘з”ҹдәҶзҪ®жҚўеҸҚеә” DпјҺеҗ‘иұҶжөҶдёӯеҠ е…ҘзӣҗеҚӨеҸҜеҲ¶дҪңиұҶи…җпјҢеҲ©з”ЁдәҶиғ¶дҪ“иҒҡжІүзҡ„жҖ§иҙЁ
|
|
| 2. | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||
|
д»…з”ЁдёӢиЎЁжҸҗдҫӣзҡ„зҺ»з’ғд»ӘеҷЁпјҲйқһзҺ»з’ғд»ӘеҷЁд»»йҖүпјүе°ұиғҪе®һзҺ°зӣёеә”е®һйӘҢзӣ®зҡ„зҡ„жҳҜпјҲВ В В В В пјү
|
||||||||||||||||
| 3. | иҜҰз»ҶдҝЎжҒҜ | ||||
|
дёӢеҲ—жңүе…ійҮ‘еұһзҡ„иҜҙжі•дёӯпјҢжӯЈзЎ®зҡ„жҳҜпјҲВ В В В В пјү в‘ зәҜй“Ғиҫғз”ҹй“ҒдёҚжҳ“з”ҹй”ҲВ В В В В В В В В В В В В В В В В в‘ЎеҶ¶зӮјй“қе’Ңй’ йғҪеҸҜд»Ҙз”Ёз”өи§Јжі• в‘ўKSCNжә¶ж¶ІеҸҜд»ҘжЈҖйӘҢFe3+зҰ»еӯҗВ В В В В В В в‘Јзјәй’ҷдјҡеј•иө·йӘЁиҙЁз–ҸжқҫпјҢзјәй“Ғдјҡеј•иө·иҙ«иЎҖ в‘Өйқ’й“ңгҖҒдёҚй”Ҳй’ўгҖҒзЎ¬й“қйғҪжҳҜеҗҲйҮ‘В В В В В В В в‘Ҙй“ңдёҺзЎ«еҸҚеә”пјҢз”ҹжҲҗй»‘иүІзҡ„CuS
|
|||||
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
и®ҫNAдёәйҳҝдјҸдјҪеҫ·зҪ—еёёж•°зҡ„еҖјгҖӮдёӢеҲ—жңүе…іеҸҷиҝ°жӯЈзЎ®зҡ„жҳҜпјҲВ В В В В пјү AпјҺж ҮеҶөдёӢпјҢ11.2LВ ж°ҹеҢ–ж°ўдёӯеҗ«жңүзҡ„еҲҶеӯҗж•°зӣ®дёә0.5NA BпјҺе®Өжё©дёӢпјҢ21.0gд№ҷзғҜе’ҢдёҒзғҜзҡ„ж··еҗҲж°”дҪ“дёӯжүҖеҗ«зҡ„зўіеҺҹеӯҗж•°зӣ®жҳҜNA CпјҺе®Өжё©дёӢпјҢ2L 0.05mol/LВ зҡ„NH4NO3жә¶ж¶ІдёӯжүҖеҗ«жңүзҡ„ж°®еҺҹеӯҗж•°зӣ®жҳҜ0.2NA DпјҺ22.4L Cl2В дёҺи¶ійҮҸNaOHжә¶ж¶ІеҸҚеә”ж—¶иҪ¬з§»зҡ„з”өеӯҗж•°дёәNA
|
|
| 5. | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||||||||||||||||||||||||||||||||
|
жүҖи°“еҗҲйҮ‘пјҢе°ұжҳҜдёҚеҗҢз§ҚйҮ‘еұһ(д№ҹеҢ…жӢ¬дёҖдәӣйқһйҮ‘еұһ)еңЁзҶ”иһҚзҠ¶жҖҒдёӢеҪўжҲҗзҡ„дёҖз§ҚзҶ”еҗҲзү©пјҢдёӢиЎЁдёәеӣӣз§ҚйҮ‘еұһзҡ„зҶ”гҖҒжІёзӮ№пјҢж №жҚ®д»ҘдёӢж•°жҚ®еҲӨж–ӯе…¶дёӯдёҚиғҪеҪўжҲҗеҗҲйҮ‘зҡ„жҳҜпјҲВ В В В В пјү
|
||||||||||||||||||||||||||||||||||||||||||||||
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—иҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜпјҲВ В В В В пјү AпјҺиғ¶дҪ“дёҺе…¶е®ғеҲҶж•Јзі»зҡ„жң¬иҙЁеҢәеҲ«жҳҜеҲҶж•ЈиҙЁзІ’еӯҗзӣҙеҫ„зҡ„еӨ§е°ҸеңЁ1-100 nmд№Ӣй—ҙ BпјҺеҸҜд»ҘеҲ©з”ЁдёҒиҫҫе°”ж•Ҳеә”еҢәеҲҶиғ¶дҪ“е’Ңжә¶ж¶І CпјҺиғ¶дҪ“еқҮиғҪеҸ‘з”ҹеёғжң—иҝҗеҠЁе’Ңз”өжіізҺ°иұЎ DпјҺиғ¶дҪ“еңЁдёҖе®ҡжқЎд»¶дёӢиғҪзЁіе®ҡеӯҳеңЁ
|
|
| 7. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҢ–еӯҰеҸҚеә”еҜ№еә”зҡ„зҰ»еӯҗж–№зЁӢејҸд№ҰеҶҷжӯЈзЎ®зҡ„жҳҜпјҲВ В В В В пјү AпјҺз”ЁFeCl3жә¶ж¶Іи…җиҡҖеҚ°еҲ·з”өи·ҜжқҝпјҡFe3++Cu=Fe2++Cu2+ BпјҺзўҳж°ҙдёӯйҖҡе…ҘйҖӮйҮҸзҡ„SO2пјҡI2пјӢSO2пјӢ2H2O=2IпјҚпјӢSO42вҲ’пјӢ4HпјӢ CпјҺNH4Al(SO4)2жә¶ж¶Ідёӯж»ҙеҠ е°‘йҮҸзҡ„NaOHпјҡNH4++OHпјҚ=NH3В·H2O DпјҺеҗ‘дёҖе®ҡйҮҸKAl(SO4)2жә¶ж¶Ідёӯж»ҙе…ҘBa(OH)2жә¶ж¶ІиҮіжІүж·Җзҡ„зү©иҙЁзҡ„йҮҸжңҖеӨ§пјҡ Al3пјӢпјӢ2SO42вҲ’пјӢ2Ba2пјӢпјӢ4OHпјҚ=AlO2вҲ’пјӢ2BaSO4вҶ“пјӢ2H2O
|
|
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зү©иҙЁзҡ„иҪ¬еҢ–еңЁз»ҷе®ҡжқЎд»¶дёӢиғҪе®һзҺ°зҡ„жҳҜпјҲВ В В В В пјү AпјҺNaCl(aq) BпјҺCuCl2 CпјҺAl DпјҺMgO(s)
|
|
| 9. | иҜҰз»ҶдҝЎжҒҜ |
|
дәҢж°§еҢ–зЎ’(SeO2)жҳҜдёҖз§Қж°§еҢ–еүӮпјҢе…¶иў«иҝҳеҺҹеҗҺзҡ„еҚ•иҙЁзЎ’еҸҜиғҪжҲҗдёәзҺҜеўғжұЎжҹ“зү©пјҢйҖҡиҝҮдёҺжө“зЎқй…ёгҖҒжө“зЎ«й…ёеҸҚеә”з”ҹжҲҗSeO2д»Ҙеӣһ收SeгҖӮеңЁеӣһ收иҝҮзЁӢдёӯж¶үеҸҠеҰӮдёӢеҢ–еӯҰеҸҚеә”пјҡ в‘ SeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2Oпјӣ в‘ЎSe+2H2SO4пјҲжө“пјү=2SO2вҶ‘+SeO2+2H2Oпјӣ в‘ўSe+4HNO3пјҲжө“пјү=SeO2+4NO2вҶ‘+2H2Oпјӣ дёӢеҲ—жңүе…іеҸҷиҝ°жӯЈзЎ®зҡ„жҳҜпјҲВ В В В В пјү AпјҺж°§еҢ–жҖ§з”ұејәеҲ°ејұзҡ„йЎәеәҸжҳҜH2SO4пјҲжө“пјүпјһSeO2пјһI2 BпјҺеҸҚеә”в‘ дёӯSeжҳҜж°§еҢ–дә§зү©пјҢI2жҳҜиҝҳеҺҹдә§зү© CпјҺеҸҚеә”в‘ дёӯз”ҹжҲҗ0.6mol I2пјҢиҪ¬з§»зҡ„з”өеӯҗж•°зӣ®дёә2.4NA DпјҺеҸҚеә”в‘Ўв‘ўдёӯзӯүйҮҸзҡ„Seж¶ҲиҖ—жө“зЎ«й…ёе’Ңжө“зЎқй…ёдёӯжә¶иҙЁзҡ„зү©иҙЁзҡ„йҮҸд№ӢжҜ”дёә2:1
|
|
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
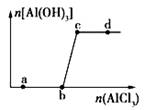
еҗ‘дёҖе®ҡйҮҸзҡ„NaOHжә¶ж¶ІдёӯйҖҗж»ҙеҠ е…ҘAlCl3жә¶ж¶ІпјҢз”ҹжҲҗжІүж·ҖAl(OH)3зҡ„йҮҸйҡҸAlCl3еҠ е…ҘйҮҸзҡ„еҸҳеҢ–е…ізі»еҰӮеӣҫжүҖзӨәгҖӮеҲҷдёӢеҲ—зҰ»еӯҗз»„еңЁеҜ№еә”зҡ„жә¶ж¶ІдёӯдёҖе®ҡиғҪеӨ§йҮҸе…ұеӯҳзҡ„жҳҜпјҲВ В В В В пјү
BпјҺbзӮ№еҜ№еә”зҡ„жә¶ж¶ІдёӯпјҡNa+гҖҒS2вҲ’гҖҒSO42вҲ’гҖҒClвҲ’ CпјҺcзӮ№еҜ№еә”зҡ„жә¶ж¶ІдёӯпјҡAg+гҖҒCa2+гҖҒNO3вҲ’гҖҒFвҲ’ DпјҺdзӮ№еҜ№еә”зҡ„жә¶ж¶ІдёӯпјҡK+гҖҒNH4+гҖҒIвҲ’гҖҒCO32вҲ’
|
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
K2Cr2O7жә¶ж¶ІдёӯеӯҳеңЁе№іиЎЎпјҡ Cr2O72вҲ’(ж©ҷиүІ)+H2O
з»“еҗҲе®һйӘҢ,дёӢеҲ—иҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜпјҲВ В В В В пјү AпјҺВ в‘ дёӯжә¶ж¶Іж©ҷиүІеҠ ж·ұпјҢв‘ўдёӯжә¶ж¶ІеҸҳй»„ BпјҺв‘ЎдёӯCr2O72вҲ’иў«C2H5OHиҝҳеҺҹ CпјҺеҜ№жҜ”в‘Ўе’Ңв‘ЈеҸҜзҹҘK2Cr2O7й…ёжҖ§жә¶ж¶Іж°§еҢ–жҖ§ејә DпјҺиӢҘеҗ‘в‘ЈдёӯеҠ е…Ҙ70%H2SO4жә¶ж¶ІиҮіиҝҮйҮҸпјҢжә¶ж¶ІеҸҳдёәж©ҷиүІ
|
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
AгҖҒBгҖҒCгҖҒDеӣӣз§Қзү©иҙЁд№Ӣй—ҙзҡ„иҪ¬еҢ–е…ізі»еҰӮеӣҫжүҖзӨәпјҲйғЁеҲҶдә§зү©е·Із•ҘеҺ»пјүпјҢдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲВ В В В В пјү AпјҺиӢҘAдёәAlCl3жә¶ж¶ІпјҢBеҸҜиғҪдёәж°Ёж°ҙпјҢеҸҚеә”в‘ зҡ„зҰ»еӯҗж–№зЁӢејҸдёәпјҡВ В В В В A13++4NH3В·H2O=AlO2вҲ’+ 4NH4++2H2O BпјҺиӢҘAдёәFeпјҢBеҸҜиғҪдёәзЁҖзЎқй…ёпјҢеҸҚеә”в‘Ўзҡ„зҰ»еӯҗж–№зЁӢејҸдёә: 3Fe+8H++2NO3вҲ’=3Fe2++2NOвҶ‘+4H2O CпјҺиӢҘAдёәNaOHжә¶ж¶ІпјҢBеҸҜиғҪдёәCO2пјҢеҸҜз”ЁCa(OH)2жә¶ж¶ІйүҙеҲ«CгҖҒDжә¶ж¶І DпјҺиӢҘAдёәCl2пјҢBеҸҜиғҪдёәNH3пјҢе®һйӘҢе®ӨеҸҜз”ЁеҠ зғӯеӣәдҪ“Cзҡ„ж–№жі•еҲ¶еҸ–NH3
|
|
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
зҺ°жңүй“ҒзІүе’ҢBr2зү©иҙЁзҡ„йҮҸйғҪдёәn molе……еҲҶеҸҚеә”пјҢеҠ ж°ҙеҫ—еҲ°жҫ„жё…жә¶ж¶ІеҗҺпјҢйҖҡе…Ҙa mol Cl2гҖӮдёӢеҲ—еҸҷиҝ°дёҚжӯЈзЎ®зҡ„жҳҜпјҲВ В В В В пјү AпјҺеҪ“a = 1/3nж—¶пјҢеҸ‘з”ҹзҡ„еҸҚеә”дёә2Fe2++Cl2пјқ2Fe3++2ClпјҚ BпјҺеҪ“a = 3/2nж—¶пјҢеҸ‘з”ҹзҡ„еҸҚеә”дёә2Fe2++4BrпјҚ+3Cl2пјқ2Fe3++2Br2+6ClпјҚ CпјҺиӢҘжә¶ж¶ІдёӯBrпјҚжңүдёҖеҚҠиў«ж°§еҢ–ж—¶пјҢжә¶ж¶Ідёӯc(Fe3+): c(BrпјҚ):c(ClпјҚ) пјқ1:1:3 DпјҺеҪ“0пјңaпјң1/2nж—¶пјҢжә¶ж¶Ідёӯе§Ӣз»Ҳж»Ўи¶і2c(Fe2+)+3c(Fe3+)+c(H+)пјқc(ClпјҚ)+c(BrпјҚ)+ c(OHпјҚ)
|
|
| 14. | иҜҰз»ҶдҝЎжҒҜ | |||||
|
CO2дёҺH2зҡ„ж··еҗҲж°”дҪ“5gпјҢеңЁ150в„ғж—¶е’Ңи¶ійҮҸзҡ„ж°§ж°”ж··еҗҲпјҢз”Ёз”өзҒ«иҠұе……еҲҶеј•зҮғпјҢеңЁзӣёеҗҢзҠ¶еҶөдёӢеҶҚе°ҶеҸҚеә”еҗҺжүҖеҫ—ж··еҗҲж°”дҪ“йҖҡе…ҘеҲ°и¶ійҮҸзҡ„Na2O2дёӯпјҢжөӢеҫ—Na2O2еӣәдҪ“еўһйҮҚзҡ„иҙЁйҮҸдёә3.4gпјҢеҲҷеҺҹж··еҗҲж°”дҪ“дёӯCO2зҡ„иҙЁйҮҸеҲҶж•°дёәпјҲВ В В В В пјү
|
||||||
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
еҸ–зӯүзү©иҙЁзҡ„йҮҸжө“еәҰзҡ„NaOHжә¶ж¶ІдёӨд»ҪAе’ҢBпјҢжҜҸд»Ҫ10mLпјҢеҲҶеҲ«еҗ‘AгҖҒBдёӯйҖҡе…ҘдёҚзӯүйҮҸзҡ„CO2пјҢеҶҚ继з»ӯеҗ‘дёӨжә¶ж¶ІдёӯйҖҗж»ҙеҠ е…Ҙ0.2mol/Lзҡ„зӣҗй…ёпјҢж ҮеҮҶзҠ¶еҶөдёӢдә§з”ҹзҡ„CO2ж°”дҪ“дҪ“з§ҜдёҺжүҖеҠ зҡ„зӣҗй…ёжә¶ж¶ІдҪ“з§Ҝд№Ӣй—ҙзҡ„е…ізі»еҰӮеӣҫжүҖзӨәпјҢдёӢеҲ—еҸҷиҝ°жӯЈзЎ®зҡ„жҳҜпјҲВ В В В В пјү AпјҺAжӣІзәҝиЎЁжҳҺеҺҹNaOHжә¶ж¶ІдёӯйҖҡе…ҘCO2еҗҺпјҢжүҖеҫ—жә¶ж¶Ідёӯзҡ„жә¶иҙЁжҲҗеҲҶжҳҜNa2CO3е’ҢNaHCO3 BпјҺBжӣІзәҝдёӯж¶ҲиҖ—зӣҗй…ё0<v(HCl)<25mLж—¶еҸ‘з”ҹзҡ„зҰ»еӯҗеҸҚеә”дёәпјҡOHпјҚ+H+=H2OВ H++CO32пјҚ=HCO3пјҚ CпјҺBжӣІзәҝиЎЁжҳҺеҺҹNaOHжә¶ж¶ІдёӯйҖҡе…ҘCO2еҗҺпјҢжүҖеҫ—жә¶ж¶ІеҠ зӣҗй…ёеҗҺдә§з”ҹCO2ж°”дҪ“дҪ“з§ҜпјҲж ҮеҮҶзҠ¶еҶөпјүзҡ„жңҖеӨ§еҖјдёә224mLВ В В DпјҺеҺҹNaOHжә¶ж¶Ізҡ„зү©иҙЁзҡ„йҮҸжө“еәҰдёә1.0mol/L
|
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
|
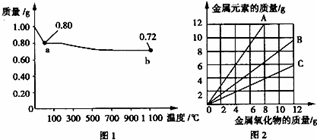
й“ңжңүдёӨз§Қеёёи§Ғзҡ„ж°§еҢ–зү©CuOе’ҢCu2OгҖӮжҹҗеӯҰд№ е°Ҹз»„еҸ–0.98gпјҲз”ЁзІҫеҜҶеӨ©е№іжөӢйҮҸпјүCu(OH)2еӣәдҪ“еҠ зғӯпјҢжңүй“ңзҡ„ж°§еҢ–зү©з”ҹжҲҗпјҢе…¶иҙЁйҮҸйҡҸжё©еәҰеҸҳеҢ–еҰӮеӣҫ1жүҖзӨәпјҡеҸҰеӨ–пјҢжҹҗеҗҢеӯҰз»ҳеҲ¶дәҶдёүжқЎиЎЁзӨәйҮ‘еұһж°§еҢ–зү©дёҺе…¶жүҖеҗ«йҮ‘еұһе…ғзҙ зҡ„иҙЁйҮҸзҡ„е…ізі»жӣІзәҝпјҢеҰӮеӣҫ2жүҖзӨәгҖӮеҲҷдёӢеҲ—еҲҶжһҗжӯЈзЎ®зҡ„жҳҜпјҲВ В В В В пјү
AпјҺеӣҫ1дёӯпјҢaеҲ°bзҡ„иҝҮзЁӢдёӯжңү0.01 molз”өеӯҗеҸ‘з”ҹдәҶиҪ¬з§» BпјҺеӣҫ1ж•ҙдёӘиҝҮзЁӢдёӯе…ұз”ҹжҲҗ0.26 gж°ҙ CпјҺеӣҫ2дёүжқЎжӣІзәҝдёӯпјҢиЎЁзӨәCuOе’Ңе…¶жүҖеҗ«Cuе…ғзҙ иҙЁйҮҸе…ізі»зҡ„жӣІзәҝжҳҜA DпјҺеӣҫ1дёӯAе’ҢBеҢ–еӯҰејҸеҲҶеҲ«дёәCu2Oе’ҢCuO
|
|
| 17. | иҜҰз»ҶдҝЎжҒҜ |
|
йӣҫйңҫдёҘйҮҚеҪұе“Қдәә们зҡ„з”ҹжҙ»дёҺеҒҘеә·пјҢжҹҗең°еҢәзҡ„йӣҫйңҫдёӯеҸҜиғҪеҗ«жңүеҰӮдёӢеҸҜжә¶жҖ§ж— жңәзҰ»еӯҗпјҡNa+гҖҒNH4+гҖҒMg2+гҖҒAl3+гҖҒSO42пјҚгҖҒNO3пјҚгҖҒClпјҚгҖӮжҹҗеҗҢеӯҰ收йӣҶдәҶиҜҘең°еҢәзҡ„йӣҫйңҫпјҢз»Ҹеҝ…иҰҒзҡ„йў„еӨ„зҗҶеҗҺзҡ„иҜ•ж ·жә¶ж¶ІпјҢи®ҫ计并е®ҢжҲҗдәҶеҰӮдёӢе®һйӘҢпјҡ е·ІзҹҘпјҡ3NO3пјҚ+8Al+5OHпјҚ+2H2O
ж №жҚ®д»ҘдёҠзҡ„е®һйӘҢж“ҚдҪңе’ҢзҺ°иұЎпјҢиҜҘеҗҢеӯҰеҫ—еҮәзҡ„з»“и®әдёҚжӯЈзЎ®зҡ„жҳҜпјҲВ В В В В пјү AпјҺиҜ•ж ·дёӯиӮҜе®ҡеӯҳеңЁNH4+гҖҒMg2+гҖҒSO42пјҚе’ҢNO3пјҚ BпјҺиҜ•ж ·дёӯдёҖе®ҡдёҚеҗ«Al3+ CпјҺиҜ•ж ·дёӯеҸҜиғҪеӯҳеңЁNa+гҖҒClпјҚ DпјҺиҜҘйӣҫйңҫдёӯеҸҜиғҪеӯҳеңЁNaNO3гҖҒNH4Clе’ҢMgSO4
|
|
| 18. | иҜҰз»ҶдҝЎжҒҜ |
|
е·ІзҹҘжҹҗж··еҗҲзү©еҗ«жңүAеҚ•иҙЁдёҺеҢ–еҗҲзү©BпјҢеңЁдёҖе®ҡжқЎд»¶дёӢеҸҜжҢүеӣҫжүҖзӨәеҸ‘з”ҹиҪ¬еҢ–гҖӮ
пјҲ1пјүжІүж·ҖHеҸҳжІүж·ҖIзҡ„еҢ–еӯҰж–№зЁӢејҸ_____________________________гҖӮ пјҲ2пјүеҸҚеә”в‘Ўзҡ„еҢ–еӯҰж–№зЁӢејҸ_____________________________гҖӮ пјҲ3пјүжә¶ж¶ІEдёӯйҖҡе…ҘиҝҮйҮҸдәҢж°§еҢ–зўізҡ„зҰ»еӯҗж–№зЁӢејҸ_______________________________гҖӮ пјҲ4пјүз”ЁеҢ–еӯҰеҸҚеә”ж–№зЁӢејҸе’Ңз®ҖжҙҒзҡ„иҜӯиЁҖи§ЈйҮҠеӣҫдёӯжә¶ж¶ІKеҲ¶еҸ–еҢ–еҗҲзү©Cзҡ„иҝҮзЁӢпјҡ _________________________________________________________________________гҖӮ пјҲ5пјүиӢҘиҰҒдҝқеӯҳFжә¶ж¶ІпјҢеә”еҗ‘жә¶ж¶ІдёӯеҠ е…ҘдёӨз§Қзү©иҙЁдёәпјҡ_________гҖҒ________пјҲеЎ«еҢ–еӯҰејҸпјүгҖӮ
|
|
| 19. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||||
|
зӮјй”ҢеҺӮзҡ„й“ңй•үеәҹжёЈдёӯеҗ«жңүй“ңгҖҒй”ҢгҖҒй•үгҖҒй“ҒгҖҒз ·зӯүе…ғзҙ пјҢе…¶еҗ«йҮҸдҫқж¬ЎеҮҸе°‘гҖӮеҜ№иҝҷдәӣе…ғзҙ иҝӣиЎҢжҸҗеҸ–еҲҶзҰ»иғҪеҮҸе°‘зҺҜеўғжұЎжҹ“пјҢеҗҢж—¶еҲ¶еҫ—ZnSO4вҖ§7H2Oе®һзҺ°иө„жәҗзҡ„еҶҚеҲ©з”ЁгҖӮе…¶жөҒзЁӢеӣҫеҰӮдёӢгҖӮе·ІзҹҘFeAsO4йҡҫжә¶дәҺж°ҙпјӣZnSO4вҖ§7H2Oжҳ“жә¶дәҺж°ҙпјҢйҡҫжә¶дәҺд№ҷйҶҮгҖӮВ
иҜ·еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ пјҲ1пјүжҸҗй«ҳжөёеҮәзҺҮеҸҜд»ҘйҮҮз”Ёзҡ„ж–№жі•жҳҜпјҲеҶҷеҮәе…¶дёӯдёҖзӮ№еҚіеҸҜпјү______________гҖӮВ AпјҺж°ҙ В В В В В В BпјҺд№ҷйҶҮВ В В В В В В CпјҺ йҘұе’ҢзЎ«й…ёй”Ңжә¶ж¶ІВ В В В В DпјҺзЁҖзЎ«й…ё
|
|||||||||||||||||||
| 20. | иҜҰз»ҶдҝЎжҒҜ |
|
зЎ«й…ёдәҡй“Ғй“ө[(NH4)2Fe(SO4)2]жҳҜдёҖз§ҚйҮҚиҰҒзҡ„еҢ–е·ҘеҺҹж–ҷпјҢз”ЁйҖ”еҚҒеҲҶе№ҝжіӣгҖӮе®ғеҸҜд»ҘдҪңеҮҖж°ҙеүӮпјҢеңЁж— жңәеҢ–еӯҰе·ҘдёҡдёӯпјҢе®ғжҳҜеҲ¶еҸ–е…¶е®ғй“ҒеҢ–еҗҲзү©зҡ„еҺҹж–ҷгҖӮ гҖҗжҹ»йҳ…иө„ж–ҷгҖ‘йҡ”з»қз©әж°”еҠ зғӯиҮі500в„ғж—¶зЎ«й…ёдәҡй“Ғй“өиғҪе®Ңе…ЁеҲҶи§ЈпјҢеҲҶи§Јдә§зү©дёӯеҗ«жңүй“Ғж°§еҢ–зү©гҖҒзЎ«ж°§еҢ–зү©гҖҒж°Ёж°”е’Ңж°ҙи’ёж°”зӯүгҖӮ гҖҗе®һйӘҢжҺўз©¶гҖ‘жҹҗеҢ–еӯҰе°Ҹз»„йҖүз”ЁдёӢеӣҫжүҖзӨәйғЁеҲҶиЈ…зҪ®иҝӣиЎҢе®һйӘҢпјҲйғЁеҲҶеӨ№жҢҒиЈ…зҪ®з•Ҙпјү
пјҲ1пјүйӘҢиҜҒеҲҶи§Јдә§зү©дёӯеҗ«жңүж°Ёж°”е’Ңж°ҙи’ёж°”пјҢ并жҺўз©¶ж®Ӣз•ҷеӣәдҪ“жҲҗеҲҶгҖӮ в‘ жүҖйҖүз”ЁиЈ…зҪ®зҡ„жӯЈзЎ®иҝһжҺҘйЎәеәҸдёәпјҲВ В В В В пјүгҖӮ AпјҺA-B-C-D В В В В В В BпјҺA-C-B-DВ В В В В В В CпјҺA-D-B-CВ В В В DпјҺA-D-C-B в‘ЎеҸ–Aдёӯж®Ӣз•ҷеӣәдҪ“пјҢеҠ е…ҘйҖӮйҮҸзЁҖзЎ«й…ёпјҢдҪҝе…¶е®Ңе…Ёжә¶и§Јеҫ—еҲ°жә¶ж¶ІBпјҢдёӢеҲ—е“Әз»„е®һйӘҢиғҪеӨҹиҜҒжҳҺAдёӯж®Ӣз•ҷеӣәдҪ“д»…дёәFe2O3пјҢиҖҢдёҚеҗ«В FeOВ жҲ–В Fe3O4пјҲВ В В В В пјү AпјҺеҗ‘жә¶ж¶ІBдёӯж»ҙеҠ й…ёжҖ§й«ҳй”°й…ёй’ҫжә¶ж¶ІпјҢй«ҳй”°й…ёй’ҫжә¶ж¶ІдёҚиӨӘиүІ BпјҺеҗ‘жә¶ж¶ІBдёӯеҠ е…ҘиӢҜй…ҡпјҢжә¶ж¶Іе‘Ҳзҙ«иүІ CпјҺеҗ‘жә¶ж¶ІBдёӯйҖҡе…Ҙи¶ійҮҸж°Ҝж°”пјҢеҠ е…ҘзЎ«ж°°й…ёй’ҫжә¶ж¶ІеҸҳзәўиүІ DпјҺеҗ‘жә¶ж¶ІBдёӯеҠ е…Ҙй“Ғж°°еҢ–й’ҫжә¶ж¶ІпјҢж— зҺ°иұЎ пјҲ2пјүжҺўз©¶еҲҶи§Јдә§зү©дёӯзҡ„зЎ«ж°§еҢ–зү©пјҢиҝһжҺҘиЈ…зҪ®AвҖ”EвҖ”FвҖ”BиҝӣиЎҢе®һйӘҢгҖӮ в‘ е®һйӘҢиҝҮзЁӢдёӯи§ӮеҜҹеҲ°пјҡEдёӯжІЎжңүжҳҺжҳҫзҺ°иұЎпјҢFдёӯжә¶ж¶ІиӨӘиүІпјҢжҚ®жӯӨеҫ—еҮәиҜҘзЎ«еҢ–зү©жҳҜ__________гҖӮ в‘Ўе®һйӘҢиҜҒжҳҺ(NH4)2Fe(SO4)2еҸ—зғӯеҲҶи§ЈйҷӨдёҠиҝ°дә§зү©еӨ–пјҢиҝҳжңүN2з”ҹжҲҗпјҢеҶҷеҮәAдёӯеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸ_____________________________________________гҖӮ
|
|
| 21. | иҜҰз»ҶдҝЎжҒҜ |
|
з«ҜзӮ”зғғеңЁеӮ¬еҢ–еүӮеӯҳеңЁдёӢеҸҜеҸ‘з”ҹеҒ¶иҒ”еҸҚеә”пјҢз§°дёәGlaserеҸҚеә”гҖӮ
иҜҘеҸҚеә”еңЁз ”究新еһӢеҸ‘е…үжқҗж–ҷгҖҒи¶…еҲҶеӯҗеҢ–еӯҰзӯүж–№йқўе…·жңүйҮҚиҰҒд»·еҖјгҖӮеҰӮеӣҫжҳҜз”ЁеҲ©з”ЁGlaserеҸҚеә”еҲ¶еӨҮеҢ–еҗҲзү©Eзҡ„дёҖз§ҚеҗҲжҲҗи·Ҝзәҝпјҡ
еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ пјҲ1пјүBзҡ„еҢ–еӯҰеҗҚз§°дёәВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В гҖӮ пјҲ2пјүв‘ўзҡ„еҸҚеә”зұ»еһӢдёәВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В гҖӮ пјҲ3пјүEзҡ„з»“жһ„з®ҖејҸдёәВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В гҖӮз”Ё1 mol EеҗҲжҲҗ1,4-дәҢиӢҜеҹәдёҒзғ·пјҢзҗҶи®әдёҠйңҖиҰҒж¶ҲиҖ—ж°ўж°”В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В molгҖӮ пјҲ4пјүеҢ–еҗҲзү©пјҲ пјҲ5пјүиҠійҰҷеҢ–еҗҲзү©FжҳҜCзҡ„еҗҢеҲҶејӮжһ„дҪ“пјҢе…¶еҲҶеӯҗдёӯеҸӘжңүдёӨз§ҚдёҚеҗҢеҢ–еӯҰзҺҜеўғзҡ„ж°ўпјҢж•°зӣ®жҜ”дёә3пјҡ1пјҢеҶҷеҮәе…¶дёӯ2з§Қзҡ„з»“жһ„з®ҖејҸВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В гҖӮ
|
|
- еӨ©жҙҘй«ҳдёүеҢ–еӯҰй«ҳиҖғжЁЎжӢҹпјҲ2019е№ҙдёҠеҚҠжңҹпјүе…Қиҙ№иҜ•еҚ·е®Ңж•ҙзүҲ
- еҗүжһ—2018е№ҙй«ҳдёүдёҠеҚҠжңҹеҢ–еӯҰжңҲиҖғжөӢйӘҢеёҰзӯ”жЎҲдёҺи§Јжһҗ
- дё№дёңеёӮ2020е№ҙй«ҳдёҖеҢ–еӯҰдёҠжңҹжңҹжң«иҖғиҜ•еёҰзӯ”жЎҲдёҺи§Јжһҗ
- еҗҲиӮҘеёӮй«ҳдёүеҢ–еӯҰ2020е№ҙеүҚеҚҠжңҹе…Қиҙ№жЈҖжөӢиҜ•еҚ·
- дёҠжө·еёӮй«ҳдёүеҢ–еӯҰ2018е№ҙеүҚеҚҠжңҹй«ҳиҖғжЁЎжӢҹзҪ‘дёҠеңЁзәҝеҒҡйўҳ
- иӢҸе·һдёӯеӯҰй«ҳдёҖеҢ–еӯҰдёӢеҶҢејҖеӯҰиҖғиҜ•еңЁзәҝжөӢйӘҢе®Ңж•ҙзүҲ
- 马关еҺҝ第дәҢдёӯеӯҰ2019е№ҙй«ҳдёҖеҢ–еӯҰдёӢеӯҰжңҹејҖеӯҰиҖғиҜ•еңЁзәҝзӯ”йўҳ
- 2018иҮі2019е№ҙй«ҳдәҢдёҠеӯҰжңҹйҳ¶ж®өжөӢиҜ•еҢ–еӯҰе…Қиҙ№иҜ•еҚ·пјҲе№ҝдёңзңҒжұ•еӨҙеёӮиҫҫжҝ еҚҺдҫЁдёӯеӯҰгҖҒдёңеҺҰдёӯеӯҰпјү