实验3-2 几种有机物的检验 知识点题库
①福尔马林 ②甲酸 ③甲酸乙酯 ④乙酸甲酯 ⑤甲酸钠 ⑥醋酸 ⑦葡萄糖 ⑧乙醇
《化学与生活》

-
(1) 把新制的氢氧化铜悬浊液加入到某病人的尿液中并微热,如果观察到红色沉淀,说明尿液中可能含有的物质是
A.尿酸 B.蔗糖 C.蛋白质 D.葡萄糖
-
(2) 垃圾处理无害化、减量化和资源化逐渐被人们认识.垃圾的分类收集是实现上述理念的重要措施.某垃圾箱上贴有如图所示的标志,向此垃圾箱中丢弃的垃圾是
A.危险垃圾 B.有害垃圾 C.可回收物 D.其他垃圾
-
(3) 人类生命活动所需的各种营养主要来自于食物,食物的选择与身体健康关系很大.表格是某位同学的早餐食谱:
主食
面包
副食
酱牛肉
饮品
豆浆
表中主食含有的营养素主要是 (填“糖类”、“油脂”或“蛋白质”,下同);副食含有的营养素主要是 ,豆浆所属的分散系为 ( 填“溶液”“浊液”或“胶体”).考虑到营养成分的均衡搭配,你认为应该增加的配菜是
-
(1) 实验准备:先向一支新试管中加入适量的 溶液,加热几分钟后,用清水冲洗干净.其目的是除去内表层上的油污.油脂发生的该反应属于 反应类型,工业上又把这种反应叫做 反应.
-
(2) 银氨溶液的制备:向洁净的试管中先加入适量的 溶液,再逐渐滴加 溶液,边滴加边摇荡,当观察到 现象时,即配成了所需要的银氨溶液.
-
(3) 继续向试管中加入足量的葡萄糖溶液,混匀后静置,放在 中加热几分钟后,即形成银镜.该反应的化学方程式为 反应中若有2.0×10﹣3mol电子发生了转移,则发生反应的氧化剂的物质的量为 mol,消耗的还原剂为 mol.
-
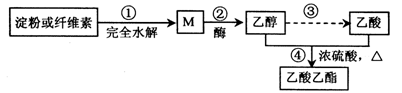
(1) 确定四种有机物的名称:
A,B,C,D。
-
(2) 写出D的同分异构体发生水解的化学方程式:。
-
(3) 写出A、B分别与银氨溶液发生反应的化学方程式:。
| 选项 | 实验目的 | 实验操作 |
| A | 制备Fe(OH)3胶体 | 将NaOH浓溶液滴加到饱和FeCl3溶液中 |
| B | 证明淀粉水解后产生葡萄糖 | 淀粉溶液加稀硫酸,水浴加热一段时间后,加新制的Cu(OH)2悬浊液,加热 |
| C | 配制 0.1000 mol/L的NaOH溶液 | 称取1.0 g NaOH固体于烧杯中,加人少量蒸馏水溶解,转移至250mL 容量瓶中定容 |
| D | 探究维生素C的还原性 | 向盛有2 mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化 |
下列说法正确的是( )
| 实验操作 | 实验目的 | |
| A | 将黄豆大小的钠分别投入等体积的水和乙醇 | 比较羟基中氢原子的活泼性 |
| B | 淀粉溶液中加入稀硫酸加热得水溶液,再加入银氨溶液后水浴加热 | 判断淀粉是否水解 |
| C | 向含有少量乙酸得乙酸乙酯中加入足量的 NaOH溶液,搅拌 | 除去乙酸乙酯中的乙酸 |
| D | 向苯酚浓溶液中滴加少量稀溴水 | 研究苯环对羟基的影响 |
 ,它们互为同分异构体
C . 已知
,它们互为同分异构体
C . 已知  该反应的有机产物是有毒物质
D .
该反应的有机产物是有毒物质
D .  二氯代物只有2种
二氯代物只有2种
-
(1) 取少量甲酸加入NaOH溶液中和其酸性,反应的离子方程式为。
-
(2) 在(1)的溶液中加入足量银氨溶液,加热,产生了银镜。甲酸钠溶液与银氨溶液发生银镜反应的离子方程式为。
-
(3) 某同学很成功的做了银镜反应,他肯定没有进行的操作___________(写字母):A . 用洁净的试管 B . 向银氨溶液中加入硝酸酸化 C . 用前几天配制好的银氨溶液 D . 直接在银氨溶液里加入稍过量的甲酸; E . 在浓度为2%的NH3∙H2O中滴入稍过量的浓度为2%的硝酸银
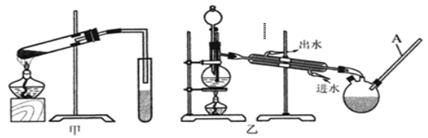
然后,同学们对甲酸与甲醇的酯化反应进行了研究:
-
(4) 写出
 和CH3—18OH进行酯化反应的化学方程式。
和CH3—18OH进行酯化反应的化学方程式。
-
(5) 你认为选择甲装置还是乙装置好?,原因是。
-
(6) 实验中饱和碳酸钠溶液的作用是。从饱和碳酸钠溶液中分离出酯需要用到的主要实验仪器是。
-
(7) 一同学用装有饱和氢氧化钠的三颈烧瓶接收甲酸甲酯,几乎没有收集到产物,请给予合理的解释。
 C . 乙烯和聚乙烯都能使酸性KMnO4 溶液褪色
D . 甲酸乙酯、葡萄糖、麦芽糖、淀粉这四种物质的共同性质是,它们既可以发生水解反应,又可以发生银镜反应
C . 乙烯和聚乙烯都能使酸性KMnO4 溶液褪色
D . 甲酸乙酯、葡萄糖、麦芽糖、淀粉这四种物质的共同性质是,它们既可以发生水解反应,又可以发生银镜反应
 ,
,  ,
,  三种元素
三种元素
| 选项 | 实验操作 | 实验目的 |
| A | 在苯和苯酚的混合液中加入足量的浓溴水,振荡、过滤 | 分离出苯酚 |
| B | 向卤代烃水解后的溶液中加入 | 判断卤素原子种类 |
| C | 淀粉与20%的硫酸混合溶液在沸水浴中充分加热后滴加碘水 | 验证淀粉是否水解完全 |
| D | 向 | 证明 |
资料:ⅰ.[Ag(NH3)2]+⇌ [Ag(NH3)]++NH3 K1=10−3.81
[Ag(NH3)]+⇌ Ag++NH3 K2=10−3.24
ⅱ.AgOH不稳定,极易分解为黑色Ag2O,Ag2O溶于氨水
-
(1) 实验发现:乙醛和AgNO3溶液水浴加热无明显现象;银氨溶液水浴加热无明显现象;滴加乙醛的银氨溶液水浴加热,试管壁逐渐出现一层光亮的银镜。
①有研究表明:配制银氨溶液时,AgNO3和氨水生成Ag(NH3)2NO3 , 写出生成Ag(NH3)2NO3的化学方程式。
②从氧化还原角度分析:发生银镜反应时,氧化性微粒可能是Ag+、。
-
(2) 甲同学查阅资料:银镜反应时,Ag+被还原成Ag。
①电极反应式:
ⅰ.还原反应:Ag++e−=Ag
ⅱ.氧化反应:。(碱性条件下)
②从电极反应角度分析物质氧化性和还原性的变化:
ⅰ.随c(Ag+)降低,Ag+氧化性减弱。
ⅱ.随c(OH−)增大,乙醛还原性增强。
③补充实验验证②中的分析。

实验操作及现象:
实验Ⅰ.插入“饱和KNO3溶液”盐桥,电流表指针偏转;
实验Ⅱ.电流稳定后向右侧烧杯滴加NaOH溶液,指针偏转幅度增大;
实验Ⅲ.电流再次稳定后向左侧烧杯滴加氨水,指针偏转幅度减小
乙同学认为实验Ⅲ不能证明“随c(Ag+)降低,Ag+氧化性减弱”,理由是。
-
(3) 设计实验进一步验证。
实验
实验操作
实验现象
Ⅳ
往盛有银氨溶液的试管中滴加浓氨水,无明显现象,加入3滴乙醛,振荡,水浴加热
闻到刺激性气味,溶液略显灰色,试管壁未见银镜
Ⅴ
往盛有银氨溶液的试管中滴加较浓的NaOH溶液至pH与实验Ⅳ相同,振荡,溶液变浑浊,加入3滴乙醛,振荡,水浴加热
试管壁立即出现银镜
①乙同学认为通过实验Ⅳ能证明“随c(Ag+)降低,Ag+氧化性减弱”,你认为是否合理并说明原因。
②分析实验Ⅴ中“立即出现银镜的原因”,提出假设:随c(OH−)增大,可能是
 也参与了还原
也参与了还原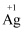 。经检验该假设成立,实验方案及现象是。
。经检验该假设成立,实验方案及现象是。 -
(4) 总结:ⅰ.银氨溶液和乙醛发生银镜反应时,氧化剂主要是Ag+ , 还原剂主要是乙醛;ⅱ.银氨溶液中滴加较浓的NaOH溶液能促进银镜反应的发生,此法不适用于检验醛基,请解释原因。
 反应,银氨溶液的溶质应是[Ag(NH3)2]NO3。该小组拟用自制的氨水制取银氨溶液,并探究其主要成分。回答下列问题:
反应,银氨溶液的溶质应是[Ag(NH3)2]NO3。该小组拟用自制的氨水制取银氨溶液,并探究其主要成分。回答下列问题:
-
(1) I.氨水的制备(如图1)
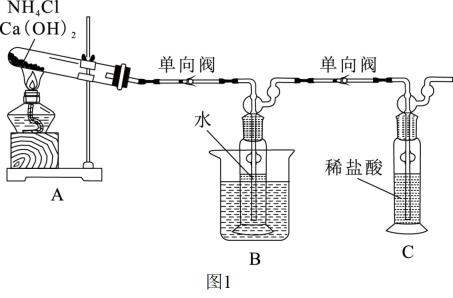
C装置的名称是;C装置的作用是。
-
(2) A中反应的化学方程式为;A装置还能用于制备气体。
-
(3) 使用加装单向阀的导管,目的是;为有利于制备氨水,装置B的大烧杯中应盛装(填“热水”或“冰水”),氨气溶于水时放热或吸热的主要原因是。
-
(4) 制得的氨水稀释到质量分数约2%,并用盐酸标准溶液标定,测得浓度为1.275mol·L-1 , 标定时应选用的指示剂为(填“酚酞”或“甲基橙”)。
-
(5) II.银氨溶液的制备及其主要成分探究
如图2所示装置,向25.00c(AgNO3)=0.12mol·L-1溶液中逐滴加入上述自制氨水,所加氨水体积由滴数传感器测量,实验测得烧杯内溶液的pH随氨水加入体积的变化曲线如图3所示。

滴加氨水过程中,BC段溶液的pH变化不大,原因是。
关于D点溶液有两种假设。
假设1:溶质为强碱性的[Ag(NH3)2]OH。25.00mLc(AgNO3)=0.12mol·L-1溶液中加入5.00mL氨水恰好澄清时,计算溶液的理论pH约为。
假设2:溶质为[Ag(NH3)2]NO3。由于银氨离子一定程度解离出氨,理论计算pH=10.26,非常接近实验值;假设1或假设2成立的是。
-
(6) 乙醛发生银镜反应的化学方程式被认为是CH3CHO+2[Ag(NH3)2]OH
 CH3COONH4+2Ag↓+3NH3+H2O,若银氨溶液的溶质为[Ag(NH3)2]NO3 , 则上述化学方程式应改为。
CH3COONH4+2Ag↓+3NH3+H2O,若银氨溶液的溶质为[Ag(NH3)2]NO3 , 则上述化学方程式应改为。
 溶液
溶液 溶液中滴入酸性
溶液中滴入酸性 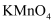 溶液
溶液


