固体溶解度的概念 知识点题库
t℃时,将一定量的某物质的溶液分成三等份,分别加热,再降温到t℃。已知从三份溶液中蒸发掉的溶剂分别为10克、20克、30克,析出的晶体分别为a克、b克、c克,则“a、b、c三者关系为 ( )
A . c=a+b
B . c=a+2b
C . c=2a+b
D . c=2b-a
t℃时,某物质的溶解度为10g,在其饱和溶液中溶液、溶剂、溶质之间的质量比正确的是( )
A . 溶液:溶质=11:1
B . 溶液:溶质=10:11
C . 溶剂:溶质=11:10
D . 溶质:溶剂=10:11
临床上发现,用25%的硫酸镁溶液l0~20 mL与10%的葡萄糖溶液500 mL的混合液可以治疗支气管哮喘。下表是硫酸镁的部分溶解度数据:
温度(℃) | 10 | 20 | 30 | 40 | 60 | 80 |
溶解度(g/100g水) | 28.2 | 33.7 | 38.9 | 44.5 | 54.6 | 55.8 |
-
(1) 若用无水硫酸镁固体配制400g 25%的硫酸镁溶液,则需要水的体积为 mL(假设此实验条件下水的密度为lg/mL),在配制溶液过程中玻璃棒的作用是 。
-
(2) 若要配制30%的硫酸镁溶液,则配制时应控制的溶液温度至少达到 ℃。
在20摄氏度时往盛有20毫升水的烧杯中,加入两药匙蔗糖后搅拌,蔗糖很快溶解完,再加入一药匙蔗糖,充分搅拌后仍有部分蔗糖不能溶解,关于上述现象,说法正确的是( )
A . 降低水的温度可以使蔗糖完全溶解
B . 加入的蔗糖越多,能够溶解的数量就越多
C . 在一定条件下,物质能够溶解的数量是有限的
D . 在20摄氏度时,20毫升水中不能溶解两药匙的蔗糖
如图所示为氯化钠和碳酸钠(俗称纯碱)在水中的溶解度曲线。请回答:

-
(1) 当温度为10 ℃时,碳酸钠的溶解度为。
-
(2) 当温度时,氯化钠的溶解度大于碳酸钠的溶解度。
-
(3) 生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”。请你解释原因。
20℃时氯化钠的溶解度是36g,则氯化钠属于( )
A . 易溶物质
B . 可溶物质
C . 微溶物质
D . 难溶物质
20℃时,将等质量的甲、乙两种固体物质(不含结晶水),分别加入到盛有100克水的烧杯中。图1为充分搅拌后的现象,图2为加热到50℃时的现象(不考虑水分蒸发),图是甲、乙两种物质的溶解度。下列说法正确的是( )




A . 表中N表示的是甲物质的溶解度
B . 图1中乙的溶液一定是不饱和溶液
C . 图2中两溶液溶质质量分数一定相等
D . 图2中两溶液降温至30℃都会析出晶体
为了探究硝酸钾溶液能否导电,实验步骤如下:①将硝酸钾晶体溶解在盛有自来水的烧杯中;②连接如图电路;③闭合开关,观察小灯泡能否发光。

-
(1) 硝酸钾溶液中含有的微粒有(用符号表示)。
-
(2) 针对该实验目的,下列评价或改进正确的是 。A . 实验步骤正确、完整 B . 应补做硝酸钾晶体能否导电的实验 C . 应将自来水改为蒸馏水 D . 应分别补做硝酸钾晶体、蒸馏水能否导电的实验
-
(3) 已知硝酸钾在不同温度下的溶解度如下表。若把溶质质量分数为32%的该盐溶液,由50℃逐渐冷却,则开始有晶体析出的温度范围是。
温度(℃)
0
10
20
30
40
溶解度(克)
13.3
20.9
31.6
45.8
63.9
下图所示,下列判断正确的是( )


A . Y的溶解度比X的溶解度大
B . t1℃时,X、Y两种饱和溶液的溶质质量分数都是20%
C . 把水滴入盛有氢氧化钠(NaOH) 固体的烧杯中,若烧杯内有晶体析出,则烧杯中饱和溶液的溶质为Y
D . t2℃时,若X、Y的饱和溶液质量相等,则溶液中溶质的质量X<Y
在盛有适量蒸馏水的烧杯中加入氢氧化钠颗粒,不断搅拌,用温度传感器记录溶解过程中的温度变化,如图所示。a、c、d三点时观察到烧杯中有固体存在,b点时固体完全消失。

-
(1) 氢氧化钠溶于水是(选填“放热”或“吸热”)过程。
-
(2) a、c两点时,氢氧化钠的溶解度(选填“相同”或“不相同”)
-
(3) c、d两点时,观察到固体较多的是。
甲、乙两种物质的溶解度曲线如图所示,若分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述不正确的是( )

A . 甲仍是饱和溶液,乙变为不饱和溶液
B . 所含溶剂质量:甲>乙
C . 溶液质量:甲<乙
D . 溶质质量分数:甲>乙
20℃时,KCl 和 KNO3 的溶解度分别为 34g 和 31.6g。小金在 20℃时进行了如图所示的操作,得到溶液①②③④。下列有关溶液①~④的分析错误的是( )


A . 属于 20℃时的饱和溶液的是②和④
B . 溶质的质量相等的是②和④
C . 溶液的溶质质量分数相等的是①和③
D . 溶液的质量②﹥④﹥③=①
20 ℃时,四个实验小组分别取不同质量的食盐,逐渐加入到各盛有50 g水的烧杯中,不断搅拌直到不再溶解为止,然后分别称量剩余食盐的质量。记录数据如表:
下列说法错误的是( )
| 实验小组 | 第一组 | 第二组 | 第三组 | 第四组 |
| 水的质量/g | 50 | 50 | 50 | 50 |
| 所取食盐的质量/g | 15 | 20 | 25 | 30 |
| 剩余食盐的质量/g | 0 | 2 | 7 | 12 |
A . 20 ℃时,50 g食盐饱和溶液中含有18 g食盐
B . 用恒温蒸发溶剂的方法可以使不饱和溶液变成饱和溶液
C . 第二组所得溶液的溶质与溶剂的质量比为9∶25
D . 相同温度下,食盐在水中的溶解度与水的质量无关
如表是氯化钾和硝酸钾的溶解度表格,如图是二者的溶解度曲线图。
|
温度/℃ |
20 |
40 |
60 |
80 |
100 |
|
|
溶解度/g |
氯化钾 |
34.0 |
40.0 |
45.5 |
51.1 |
56.7 |
|
硝酸钾 |
31.6 |
63.9 |
110.0 |
169.0 |
246.0 |
|

-
(1) 在溶解度曲线中,t1 的取值范围应该为。
-
(2) 若硝酸钾中含有少量的氯化钾,提纯硝酸钾的方法应该为。
-
(3) 下列说法正确的是(多选)。
A.P点表示t1℃时,硝酸钾和氯化钾的溶解度相等
B.t2℃时,A和B两种饱和溶液中溶剂的质量A比B少
C.t2℃时,要将接近饱和的B溶液变为饱和溶液可采取恒温蒸发溶剂的方法
D.将等质量的A和B两种溶液从t2℃降温到t1℃,A析出的晶体质量一定比B多
下表是氯化钠和硝酸钾在不同温度时的溶解度,请回答下列问题:
|
温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
|
|
溶解度/克 |
氯化钠 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
37.8 |
|
硝酸钾 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
138 |
|
-
(1) 在50℃时,100g水中加入100g硝酸钾,充分溶解后所得溶液质量为克
-
(2) T℃时,氯化钠的溶解度为36.5克,则T℃时硝酸钾的溶解度可能是__________克(选填下列选项)A . 40 B . 50 C . 60 D . 70
在一定温度下,某未饱和溶液蒸发掉 15 克水(部分)后,析出 2 克晶体(不含结晶水);
向原溶液投入 5 克溶质晶体后,溶液中还剩下 1 克固体溶质,则此温度下该溶质的溶解度为( )
A . 40 克
B . 33.3 克
C . 26.7 克
D . 13.3 克
下表是硝酸钾(KNO3)和氯化钾(KCl)在不同温度时的溶解度,请回答:
|
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
|
|
溶解度/g |
KNO3 |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
138 |
|
KCl |
27.6 |
31.0 |
34.0 |
37.0 |
40.0 |
42.6 |
45.5 |
48.3 |
|
-
(1) 由表可查知,40℃时氯化钾(KCl)的溶解度为 40 克,它的意义是。
-
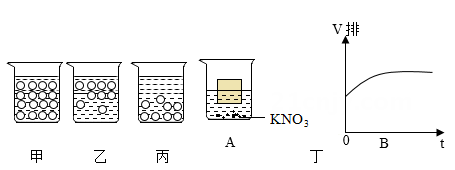
(2) 将少量硝酸钾溶解在水中,长时间放置后,硝酸钾微粒在水中的分布状况如图 所示。(填“甲”、“乙”或“丙”)(图中小圆圈代表硝酸钾微粒)
-
(3) 将一木块漂浮于50℃时的硝酸钾(KNO3)的饱和溶液中,如图丁A所示。当温度改变时(不考虑由此引起的木块和溶液体积的变化),木块排开液体的体积V排随时间t发生了如图丁B所示的变化。由此推测出温度的改变是(填“升温”或“降温”)。
在t℃时,把一定质量的固体物质A(不含结晶水)溶于水制得A溶液,现取A溶液M克,并将它分成两等份。一份加原固体物质A,达饱和时,所加A的质量恰好为此份溶液质量的1/6。另一份在t℃蒸发水份,达到饱和时,溶液质量减少1/3,则在t℃时,A物质的溶解度是,原A溶液中A的质量分数为。
20 ℃时,四个实验小组分别取不同质量的食盐,逐渐加入到各盛有50 g水的烧杯中,不断搅拌直到不再溶解为止,然后分别称量剩余食盐的质量。记录数据如表:
| 实验小组 | 第一组 | 第二组 | 第三组 | 第四组 |
| 水的质量/g | 50 | 50 | 50 | 50 |
| 所取食盐的质量/g | 15 | 20 | 25 | 30 |
| 剩余食盐的质量/g | 0 | 2 | 7 | 12 |
下列说法错误的是( )
A . 20℃时,50g食盐饱和溶液中含有18g食盐
B . 用恒温蒸发溶剂的方法可以使不饱和溶液变成饱和溶液
C . 第二组所得溶液的溶质与溶剂的质量比为9∶25
D . 相同温度下,食盐在水中的溶解度与水的质量无关
如图是 a、b、c 三种物质的溶解度曲线,下列说法正确的是( )

A . P点表示t1℃时,a、c两种物质的溶液的质量相等
B . t2℃时,a的饱和溶液的溶质质量分数为50%
C . t2℃时,将等质量的a、b、c三种物质配制成饱和溶液,所需水的质量最少的为a
D . 将t2℃时a、b、c三种物质的饱和溶液降温至t1℃,变为不饱和溶液的是a
最近更新



