钠的氧化物 知识点题库
实验序号 | 使用药品 | 现象 |
Ⅰ | Na2O2、H2O | ①试管壁发热 ②有无色无味气体产生 |
Ⅱ | Na2O2、浓盐酸 | ①试管壁发热 ②有刺激性气味的气体产生 ③反应后所得溶液呈浅黄绿色 |
请完成下列问题:
实验I中:
(1)该反应是 反应(填“放热”或“吸热”).
(2)反应的化学方程式是 .
(3)证明无色无味气体是氧气的方法是 .
实验Ⅱ中:
(4)根据现象②、③,推测生成的气体中可能含有Cl2 , 产生Cl2的化学方程式是 .
(5)若往“浅黄绿色溶液”中加入FeCl3溶液,立即产生与实验Ⅰ相同的气体,原因是 .
-
(1) NaOH溶液吸收氯气的反应:
-
(2) 铁与水蒸气在高温下的反应:
-
(3) 氢氧化铁溶于盐酸:
-
(4) 铝单质溶解在氢氧化钠溶液中:
-
(5) 过氧化钠与二氧化碳反应:.
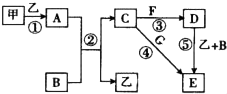
请回答下列问题:
-
(1) A是.
-
(2) 反应①~⑤中,属于氧化还原反应的是填序号).
-
(3) 反应⑤的化学方程式为;甲与B反应的离子方程式为.
-
(4) 在空气中将C溶液滴入F溶液中,观察到的现象是.

(已知:  、
、  )
)
下列分析不正确的是( )
-
(1) 请选择物质,用序号填空:①新制氯水、②铁、③铜、④稀硫酸。将Fe2+转化为Fe3+ , 可选用的物质;将Fe3+转化为Fe2+ , 可选用的物质。
-
(2) 在鲜活鱼的长途运输中,必须考虑以下几点:水中需要保持适量的O2;及时除去鱼排出的CO2;防止细菌的大量繁殖。现有两种在水中起供氧灭菌作用的物质,其性能如下:
过氧化钠(Na2O2):易溶于水,与水反应生成NaOH和O2。
过氧化钙(CaO2):微溶于水,与水反应生成Ca(OH)2(微溶)和O2。
根据以上介绍,你认为运输鲜活水产时应选择(填过氧化钠或过氧化钙)加入水中,原因是。
-
(3) NaHCO3的俗名为,Na2CO3和NaHCO3都属于类(填酸、碱或盐),在生活中却被用作食用碱;往饱和的碳酸钠溶液中通入CO2 , 化学方程式为:。
| 阳离子 | H+、K+、Al3+、 |
| 阴离子 | OH−、 |
将Na2O2逐渐加入上述混合溶液中并微热,产生沉淀和气体如图所示。
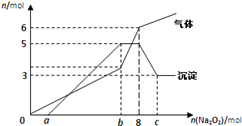
下列说法错误的是( )
 、Al3+、Mg2+、
、Al3+、Mg2+、  B . 图中a=4
C . b=7,c=9
D . 此溶液还需要用焰色反应继续检验,才能确定溶液准确组成
B . 图中a=4
C . b=7,c=9
D . 此溶液还需要用焰色反应继续检验,才能确定溶液准确组成
①Na2O与Na2O2都能和水反应生成碱,它们都是化合反应
②Na2O与Na2O2的阴阳离子个数比都是1:2
③钠在常温下不容易被氧化
④向酚酞溶液中加入Na2O2粉末,溶液先变红后褪色,并有气泡生成

-
(1) 写出装置A中反应的化学方程式。
-
(2) 写出装置B中反应的化学方程式。
-
(3) 拟用装置D收集气体产物,请将装置补充完整。
-
(4) 产物检验:检验气体产物的方法。
-
(5) 检验固体产物的方法:从B装置中取少量固体,溶于水配成溶液,。
-
(6) 有同学认为该实验装置存在明显缺陷,你认为该缺陷是什么。
-
(1) 某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,NaN3迅速分解产生N2和Na,同时放出大量的热。N2使气囊迅速膨胀,从而起到保护作用。
① KClO4的名称是,具有(填“还原性”或“氧化性”)。
② Fe2O3可处理产生的Na,反应为6Na+Fe2O3 =3Na2O+2Fe,反应中Na作(填“还原剂”或“氧化剂”)。
反应过程中氧化产物与还原产物的个数比为:。
-
(2) Na2O2可用于呼吸面具或潜水艇中氧气的来源。某实验小组利用下图装置探究Na2O2与CO2的反应。请回答下列问题:
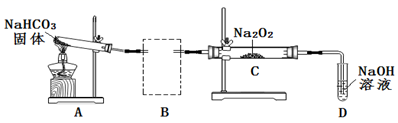
①根据实验目的,虚线框中的装置所用的试剂为。
②装置C中观察到的现象是,反应的化学方程式是。
③装置A的作用是制备CO2 , 写出A中发生反应的化学方程式是。
-
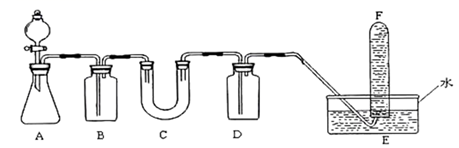
(1) 仪器C的名称是。
-
(2) 若分液漏斗中盛放的试剂是盐酸,为了除去混合气体中的氯化氢,装置B中盛放的试剂是。
-
(3) C中可能发生的化学反应的化学方程式为。
-
(4) D中盛放的试剂作用是。
-
(5) 检验F中收集到的气体的方法是。
-
(1) 常作为潜水艇和呼吸面具中氧气来源的淡黄色固体是。(填写序号,下同)
-
(2) 常用于焙制糕点的是;日常生活中常用作消毒的是。
-
(3) 实验室要放在棕色试剂瓶中保存是;除了⑤之外,能与NaOH溶液反应(NaOH参与反应)的是。
-
(4) 在高温条件下金属铝与③发生置换反应的化学方程式为。
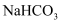 固体,D为固定有燃着蚊香的硬纸片。下列说法错误的是( )
固体,D为固定有燃着蚊香的硬纸片。下列说法错误的是( ) 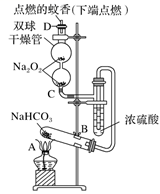
 B . 双球干燥管内发生反应的化学方程式为
B . 双球干燥管内发生反应的化学方程式为  C . 实验过程中可观察到双球干燥管中淡黄色的
C . 实验过程中可观察到双球干燥管中淡黄色的 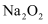 变为白色粉末,蚊香燃烧更剧烈
D . 若将试管A中的
变为白色粉末,蚊香燃烧更剧烈
D . 若将试管A中的 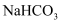 换成
换成  ,会出现相同的实验现象
,会出现相同的实验现象
 B .
B . 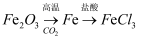 C .
C .  D .
D . 
 、
、 



