纯碱工业(侯氏制碱法) 知识点题库

化学与生产、生活密切相关.下列与化学有关的事实及其相关化学方程式的书写都正确的是( )
选项 | 事实 | 化学方程式 |
A | 常温下,可用铝制容器盛放浓硝酸 | A l+3HNO3(浓)=Al(OH)3+3NO2↑ |
B | 可用生石灰做工业废气脱硫酸 | 2CaO+2SO2+O2=2CaSO4 |
C | 电解MgCl2溶液冶炼Mg | MgCl2 |
D | 侯德榜用饱和食盐水、氨水、CO2制备纯碱 | 2NaCl+2NH3+CO2+H2O=2NH4Cl+NaCO3 |
NH3+CO2+H2O=NH4HCO3;
NH4HCO3+NaCl=NaHCO3↓+NH4Cl;
2NaHCO3 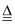 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
-
(1) 碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是
a.碳酸氢钠难溶于水
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
-
(2) 某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验.
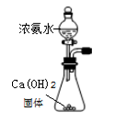
①一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出).

试回答下列有关问题:
(Ⅰ)乙装置中的试剂是;
(Ⅱ)丁装置中稀硫酸的作用是;
(Ⅲ)实验结束后,分离出NaHCO3 晶体的操作是(填分离操作的名称).
②另一位同学用图中戊装置(其它装置未画出)进行实验.
(Ⅰ)实验时,须先从管通入气体,再从管中通入气体;
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是;
-
(3) 请你再写出一种实验室制取少量碳酸氢钠的方法:.
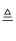 Na2CO3+H2O+CO2↑,实验室模拟该过程包括制备NH3、制取NaHCO3、分离及灼烧NaHCO3四个步骤,下列图示装置能达到实验目的是( )
Na2CO3+H2O+CO2↑,实验室模拟该过程包括制备NH3、制取NaHCO3、分离及灼烧NaHCO3四个步骤,下列图示装置能达到实验目的是( )
 制备氨气
B .
制备氨气
B . 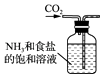 制取NaHCO3
C .
制取NaHCO3
C .  分离NaHCO3
D .
分离NaHCO3
D .  灼烧NaHCO3
灼烧NaHCO3
下列分析正确的是()
 制取氨气
B .
制取氨气
B .  制取NaHCO3
C .
制取NaHCO3
C . 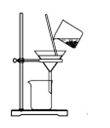 分离NaHCO3
D .
分离NaHCO3
D . 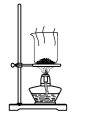 分解 NaHCO3
分解 NaHCO3
-
(1) 和索氏制碱法相比,侯氏制碱法的优势有;
-
(2) 工业纯碱中常含有少量NaCl杂质,解释原因,检验是否含有氯化钠杂质的方法为;
-
(3) 使用重量法测定纯碱的纯度,用到的试剂有;
-
(4) 使用滴定法测定纯碱的纯度,用(填仪器名称)称量1.200g工业纯碱样品,溶解,用1mol/L盐酸做标准液,滴定过程中溶液pH变化和生成CO2的量如图所示,A点溶液呈碱性的原因,计算该工业纯碱样品的质量分数。(计算结果保留两位小数)
 。
。
 ,此转化过程中氮元素被还原
C . “侯德榜制碱法”制备NaHCO3的原理是利用溶解度较大的物质制备溶解度较小的物质
D . 浸泡过高锰酸钾溶液的硅藻士可以吸收乙烯,所以可用其保鲜水果
,此转化过程中氮元素被还原
C . “侯德榜制碱法”制备NaHCO3的原理是利用溶解度较大的物质制备溶解度较小的物质
D . 浸泡过高锰酸钾溶液的硅藻士可以吸收乙烯,所以可用其保鲜水果
| 实验操作和现象 | 实验结论 | |
| A | 将惰性电极插入氢氧化铁胶体中,通电一段时间后,阴极区红褐色加深 | 氢氧化铁胶体带正电荷 |
| B | 向饱和食盐水中依次通入足量 | 该条件下溶解度: |
| C | 将苯加入到橙色的溴水中,充分振荡后静置,下层液体几乎无色 | 苯与 |
| D | 铜片投入到稀硫酸中,加热无明显现象;再加入少量硝酸钾固体,溶液变蓝色 | 硝酸钾起催化作用 |
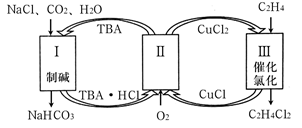
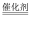 C2H4Cl2+2CuCl
C2H4Cl2+2CuCl
下列说法不正确的是( )
-
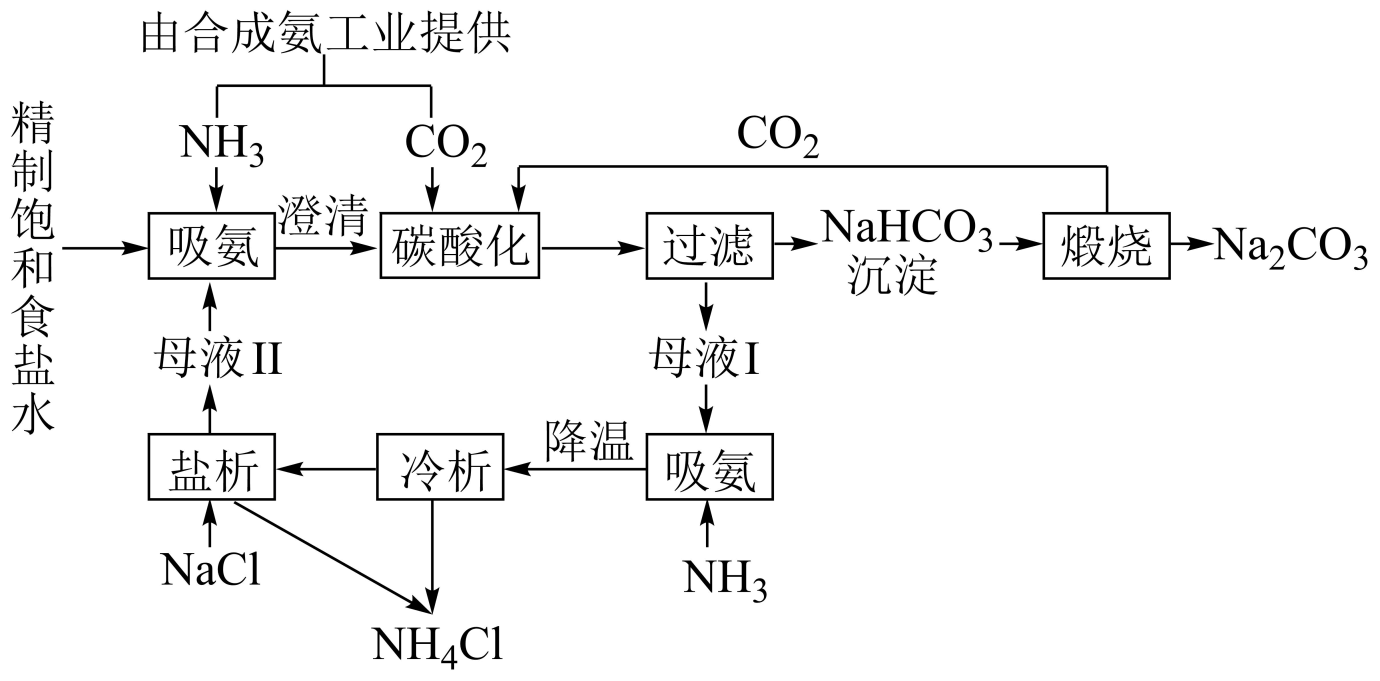
(1) Ⅰ.NaHCO3 的制备
实验流程及实验装置图如下:

回答下列问题:
a导管末端多孔球泡的作用。
-
(2) b中通入的气体是, 写出实验室制取该气体的化学方程式。
-
(3) 生成NaHCO3的总反应的化学方程式为。
-
(4) Ⅱ.Na2CO3中NaHCO3含量测定
i.称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中:
ii.移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用0.1000mol·L-1盐酸标准溶液滴定至溶液由浅红色变无色(第一滴定终点), 消耗盐酸V1mL;
iii.在上述锥形瓶中再加入2滴指示剂N,继续用0.1000mol·L-1盐酸标准溶液滴定至终点(第二滴定终点),又消耗盐酸V2mL;
iv.平行测定三次,V1 平均值为22.25,V2平均值为23.51。
回答下列问题:
指示剂N为, 第二滴定终点的现象是。
-
(5) Na2CO3中NaHCO3的质量分数为 ( 保留三位有效数字)。
-
(6) 第一滴定终点时,某同学仰视读数,其他操作均正确,则NaHCO3质量分数的计算结果(填“偏大”“偏小”或“无影响”)。
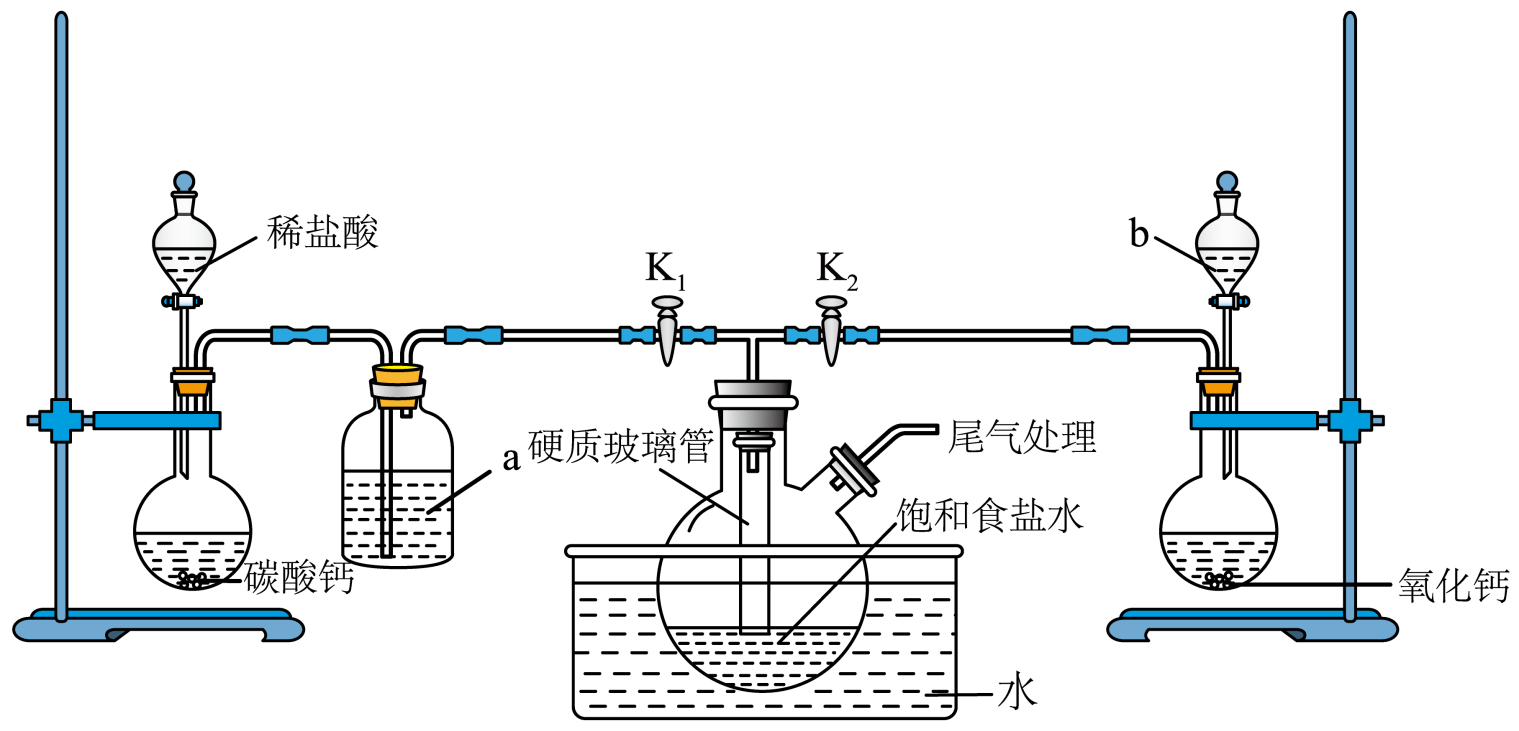
已知:NaCl、NH4HCO3、NaHCO3、NH4Cl四种盐在不同温度下的溶解度如下表所示:
温度溶解度(g) 物质 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ |
NaCl | 35.8 | 36.0 | 36.3. | 36.6 | 37.0 | 37.3 | 37.8 |
NH4HCO3 | 15.8. | 21.0 | 27.0 | 一 | 一 | — | — |
NaHCO3 | 8.15 | 9.6 | 11.1 | 12.7 | 14.45 | 。16.4 | 一 |
NH4Cl | 33.3 | 37.2 | 41.1 | 45.8 | 50.4 | 55.2 | 60.2 |
回答下列问题:
-
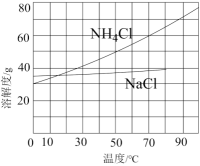
(1) 试剂b的名称是,试剂a的作用是。
-
(2) 实验时应先打开(填“K1”或“K2”)开关,持续通入气体一段时间后,关闭此开关,再打开另一开关。硬质玻璃管的作用是。
-
(3) 反应一段时间后,双颈烧瓶中观察到的实验现象为。该反应一般控制在30~35℃下进行,温度不宜过高的主要原因是(用化学方程式表示)。
-
(4) 实验结束后,过滤双颈烧瓶中的混合物,滤渣经灼烧得纯碱,并回收滤液中的NH4Cl。为促进滤液中NH4Cl析出,需向滤液中通入NH3并加入一定量NaCl固体,原因是。
-
(5) 制得的纯碱中混有NaHCO3和少量不与盐酸反应的杂质。该小组为测定其中NaHCO3的含量,取ag样品于试管中加水完全溶解,加入几滴酚酞溶液,用cmol·L-1的盐酸滴定至溶液由红色变为浅红色,消耗盐酸V1mL;再加1~2滴甲基橙指示剂,继续用盐酸滴定至溶液由黄色变为橙色,又消耗盐酸V2mL。则纯碱样品中NaHCO3质量分数为。
 、
、 、
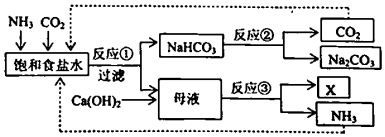
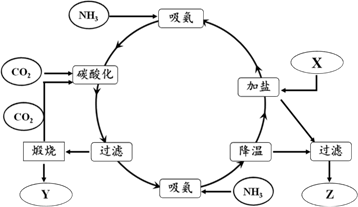
、 等杂质)为主要原料,采用“侯氏制碱法”生产纯碱和化肥
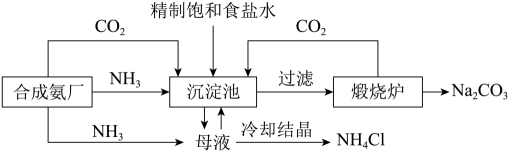
等杂质)为主要原料,采用“侯氏制碱法”生产纯碱和化肥 , 其工艺流程如下图所示(部分物质已省略)。
, 其工艺流程如下图所示(部分物质已省略)。 
-
(1) 工业粗盐溶解后,为将其中所含杂质全部沉淀,所用除杂试剂的顺序依次是。
-
(2) 向饱和食盐水中通入
 和
和 得到悬浊液,发生反应的化学方程式是。
得到悬浊液,发生反应的化学方程式是。
-
(3) 从下图可知,对溶液A进行的“系列操作”包括:蒸发浓缩、和。
-
(4) 母液中所含阳离子主要有。欲证明母液中仍然含有
 , 进行的操作和现象是。
, 进行的操作和现象是。
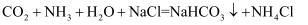 B . 吸收
B . 吸收 可使母液中的
可使母液中的 转化为
转化为 , 以提高
, 以提高 纯度
C . 该过程充分利用了合成氨工业提供的
纯度
C . 该过程充分利用了合成氨工业提供的 和
和 D . 向饱和食盐水中先通
D . 向饱和食盐水中先通 , 再通
, 再通 , 更有利于
, 更有利于 析出
析出
 Mg+Cl2↑
Mg+Cl2↑ 、
、  ,有大量晶体析出
,有大量晶体析出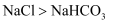
 发生了取代反应
发生了取代反应


