两性氧化物和两性氢氧化物 知识点
两性氧化物:是指既可以与酸反应生成盐和水又可以与碱反应生成盐和水的氧化物。
两性氢氧化物:既能与酸反应生成盐和水又能与强碱反应生成盐和水的氢氧化物
两性氢氧化物:既能与酸反应生成盐和水又能与强碱反应生成盐和水的氢氧化物
两性氧化物和两性氢氧化物 知识点题库
在Al2(SO4)3溶液中加入少量的NaOH溶液,观察到的现象是 ,将生成物分成两份,向第一份中加入过量的氢氧化钠溶液,向另一份中加入过量的稀硫酸,反应的离子方程式分别为 、 ,由此说明氢氧化铝是 (填物质类别).
现有以下四种物质:A.漂白粉 B.SiO2 C.Fe2O3 D.Al2O3 , 请你根据题意,选择恰当的选项用字母代号填空.
(1)可作环境消毒剂的是 ;
(2)具有两性的氧化物是 ;
(3)用作红色油漆和涂料的是 ;
(4)可作制造光导纤维的是 .
下列物质中既能与强酸又能与强碱发生氧化还原反应的是( )
A . NaHCO3
B . Mg
C . Al(OH)3
D . Al
下列物质中既能与稀H2SO4反应,又能与NaOH溶液反应的是:( )
①Al ②Fe3O4③NaHCO3 ④Al(OH)3⑤Na2CO3 .
A . ①②④
B . ②③⑤
C . ②④⑤
D . ①③④
氢氧化铝是治疗胃酸过多的内服药的主要成分,这是利用了氢氧化铝的( )
A . 弱酸性
B . 弱碱性
C . 两性
D . 不溶解性
下列物质属于两性氧化物的是( )
A . CaO
B . SO2
C . Al2O3
D . Al(OH)3
下列物质中,既能与盐酸又能与氢氧化钠溶液反应,且均有气体生成的化合物是( )
A . Si
B . NH4HCO3
C . Al
D . Al2O3
既能与稀硫酸反应,又能与NaOH溶液反应,且都有气体放出的是( )
A . NaHCO3
B . Al(OH)3
C . (NH4)2CO3
D . Al2O3
下列叙述正确的是( )
A . 某物质焰色反应为黄色,该物质中一定不含K元素
B . 合金的熔点一定比各成分金属的都高
C . SiO2属于酸性氧化物,不与任何酸反应
D . 氢氧化铝具有弱碱性,可用于制胃酸中和剂
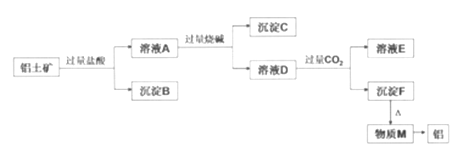
已知铝土矿的主要成分是Al2O3 , 含有杂质SiO2(不溶于盐酸和水)、Fe2O3、MgO。工业上从铝土矿中提取铝可采用如下工艺流程:
请回答下列问题:
-
(1) 溶液A转化为溶液D发生的离子方程式为。
-
(2) 由物质M制取铝的化学方程式为。
-
(3) 溶液D中通入过量CO2生成沉淀F的离子方程式为。
-
(4) 沉淀C的成分是 ,逐滴向少量沉淀C中加入过量盐酸至沉淀全部溶解,此过程的实验现象为。
有些物质既能与强酸溶液反应又能与强碱溶液反应,下列物质不具有此类性质的是( )
A . NaHCO3
B . (NH4)2CO3
C . Al
D . AlCl3
下列除去杂质的实验方法错误的是( )
A . 除去CO2中少量HCl气体:通过饱和NaHCO3溶液后再干燥气体
B . 除去Cl2中少量HCl气体:通过饱和食盐水后再干燥气体
C . 除去SiO2中的Al2O3:加入过量氢氧化钠溶液反应后过滤
D . 除去SO2中少量H2O气体:通过浓硫酸除水干燥
下列物质中既能跟盐酸反应,又能跟氢氧化钠溶液反应的化合物是( )
①Al ②Al2O3 ③Al(OH)3 ④AlCl3 ⑤NaHCO3 .
A . ① ③④
B . ②③⑤
C . ②③④
D . 全部
下列有关物质及成分、性质和用途都正确的是( )
| 选项 | 物质及成分 | 性质 | 用途 |
| A | 小苏打(Na2CO3) | 与酸反应产生二氧化碳 | 作发酵粉 |
| B | 胃舒平[Al(OH)3 ] | 与酸发生中和反应 | 做胃酸中和剂 |
| C | 磁性氧化铁(Fe2O3) | 难溶于水,颜色为红色 | 制造红色涂料 |
| D | 蓝矾(CuSO4·5H2O) | 蓝色 | 检验水蒸气 |
A . A
B . B
C . C
D . D
(Ga)与铝同主族,曾被称为“类铝”,其氧化物、氢氧化物均为两性化合物。工业制备镓的流程如图所示。下列判断不合理的是( )
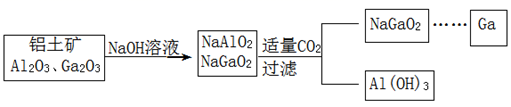
A . Al、Ga均处于ⅢA族
B . Ga(OH)3可与NaOH反应生成 NaGaO2
C . 酸性:Al(OH)3>Ga(OH)3
D . Ga2O3可与盐酸反应生成GaCl3
某无色稀溶液X中,可能含有下表所列离子中的某几种。
| 阴离子 | CO |
| 阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂Y体积(V)的关系如图所示,下列说法正确的是( )
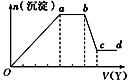
A . 若Y是盐酸,则Oa段转化为沉淀的离子(上表中,下同)只有[Al(OH)4]-
B . 若Y是盐酸,则溶液中可能含有的阳离子是Al3+
C . 若Y是NaOH溶液,则bc段反应的离子方程式为Al(OH)3+OH-=[Al(OH)4]-
D . 若Y是NaOH溶液,则X溶液中只存在四种离子,是Al3+、Fe3+、NH4+、Cl-
下列各组中的两种物质作用时,反应物用量改变,不会引起产物改变的是( )
A . NaOH和CO2
B . Al2(SO4)3和NaOH
C . Na2CO3和HCl
D . Al2O3和NaOH
下列物质中,既能跟盐酸反应,又能和NaOH溶液反应的是( )
A . SO3
B . Na2O
C . Al(OH)3
D . CO2
铍(4Be)的右下角元素是铝,根据“对角线规则”,下列描述错误的( )
A . BeO是两性氧化物
B . 已知AlCl3是共价化合物,则BeCl2也可能是共价化合物
C . Be(OH)2既能与H2SO4溶液反应也能与NaOH溶液反应
D . Be(OH)2与NaOH溶液反应后生成NaBeO2和H2O
常温下能用铝制容器盛放的是( )
A . 浓盐酸
B . 浓硝酸
C . 稀硫酸
D . 稀硝酸
最近更新



