常见金属元素的单质及其化合物的综合应用 知识点题库
向含有FeCl2、FeCl3、AlCl3、NH4Cl的混合溶液中先加入过量Na2O2固体,微热搅拌后再加入过量盐酸,溶液中阳离子数目变化最小的是( )
A . Fe2+
B . Fe3+
C . Al3+
D . NH4+
下列物质之间的转化都一步能实现的是( )
A . Si→SiO2→H2SiO3→Na2SiO3
B . Al→Al2O3→Al(OH)3→NaAlO2
C . Na→Na2O→Na2O2→NaOH→Na2CO3→NaHCO3
D . S→SO3→H2SO4→SO2→Na2SO3→Na2SO4
下列有关金属及其化合物的说法正确的是( )
A . Mg和Al都可以用电解法冶炼得到
B . Na2O2、Na2O组成元素相同,与CO2反应产物也相同
C . 用过量的KSCN溶液除去FeCl2溶液中的少量FeCl3
D . Na和Fe在一定条件下与水反应都生成H2和对应的碱
一定条件下,下列物质可以通过化合反应制得的共有( )
①硫酸铝
②小苏打
③氯化亚铁
④氢氧化铜
⑤氢氧化铁
⑥磁性氧化铁.
A . 3种
B . 4种
C . 5种
D . 6种
下列说法不正确的是( )
A . 钢是铁合金,钢的含碳量低于生铁,性能优于生铁
B . 金属具有的物理通性是延展性、导热性、银白色光泽、导电性
C . 符号Al既能表示铝元素,又能表示一个铝原子,还能表示铝单质
D . 焊锡是锡铅合金,把铅加入锡中制成合金的主要目的是降低熔点
A、B、C、X均为中学化学常见物质,一定条件下它们有如下转化关系(其它产物已略去),下列说法正确的是( )
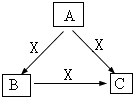
A . 若X为KOH溶液,则A可能为Al
B . 若A、B、C均为焰色反应呈黄色的化合物,则X一定为CO2
C . 若X为O2 , 则A可为非金属单质硫
D . 若X为Fe,则C可能为Fe(NO3)2溶液
类比是研究物质性质的常用方法之一,可预测许多物质的性质.但类比是相对的,不能违背客观事实.下列各种类比推测的说法中正确的是( )
A . 已知Fe与S能直接化合生成FeS,推测Cu与S可直接化合生成CuS
B . 已知CaCO3与稀硝酸反应生成CO2 , 推测CaSO3与稀硝酸反应生成SO2
C . 已知Na与水反应生成NaOH,推测Fe与水蒸汽反应生成Fe(OH)3
D . 已知Fe与CuSO4溶液反应,推测Fe与AgNO3溶液也能反应
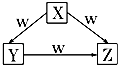
X、Y、Z、W是中学化学常见的四种物质,它们之间具有如图所示转化关系,则下列组合不可能的是( )
X | Y | Z | W | |
A | C | CO | CO2 | O2 |
B | Na | Na2O | Na2O2 | O2 |
C | AlCl3 | Al(OH)3 | NaAlO2 | NaOH |
D | Fe | FeCl2 | FeCl3 | Cl2 |
A . A
B . B
C . C
D . D
下列物质不能通过化合反应制得的是( )
A . Na2CO3
B . NaHCO3
C . Al(OH)3
D . Fe(OH)3
W是由A、B两种元素组成的AB 2型化合物。
-
(1) 若W和焦炭在高温下发生反应,所制得的半导体材料应用广泛。则W为(填化学式)。
-
(2) 若取两支试管分别加入少量W溶液,往一支试管中滴入KSCN溶液,无明显现象。往另一支试管中加入足量氯水,再加入适量CCl 4 , 振荡,静置,下层溶液呈紫红色;往上层溶液中滴入KSCN溶液,溶液呈红色。
①W溶液中所含金属阳离子为。
②上述实验中,W与足量氯水反应的离子方程式为。
-
(3) 若W是离子化合物,其阴、阳离子均含18个电子,且阴、阳离子个数比为1∶1。
①阴离子的电子式为。
②1 mol W与足量水充分反应,转移电子的物质的量为mol。
下列物质在空气中不容易发生风化或潮解的是( )
A . 石碱
B . 氯化钙
C . 食盐
D . 烧碱
信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含 70%Cu、25%Al、4%Fe 及少量
Au、Pt 的合金,并设计出由合金制备硫酸铜和硫酸铝晶体的路线:
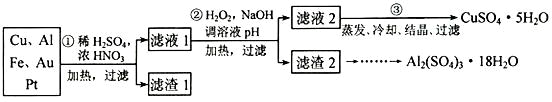
请回答下列问题:
-
(1) 第①步 Cu与酸反应的离子方程式为,得到滤渣 1的主要成分为。
-
(2) 第②步加 H2O2的作用是做氧化剂,将溶液中的 Fe2+氧化为 Fe3+ , 用 H2O2做氧化剂的优点是。
-
(3) 滤渣 2的主要成分是 Al(OH)3和 Fe(OH)3 , 在生产中如何分离两种沉淀,写出反应的离子方程式。
-
(4) 第③步蒸发所需玻璃仪器为。
某实验小组研究 FeCl3 溶液与 Na2SO3 溶液之间的反应,进行如下实验探究

-
(1) 配制 FeCl3 溶液时,先将 FeCl3 溶于浓盐酸,再稀释至指定浓度。结合化学用语说 明浓盐酸的作用:。
-
(2) 甲同学认为,上述实验在开始混合时观察到的现象不涉及氧化还原反应,实验 I中红褐色比 II 中略浅的原因是。
-
(3) 乙同学认为实验 II 可能发生了氧化还原反应,为了探究反应的产物做了实验 III和生成物检验。
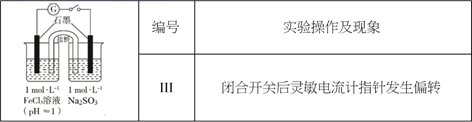
①取少量 Na2SO3 溶液电极附近的混合液,加入,产生白色沉淀,证明产生了 SO42-。
②该同学又设计实验探究另一电极的产物,取少量FeCl3溶液电极附近的混合液,加入铁氰化钾溶液,产生,证明产生了Fe2+。
-
(4) 实验 III 发生反应的方程式是。
-
(5) 实验小组查阅资料:溶液中 Fe3+、 SO32- 、OH-三种微粒会形成红色配合物并存在如下转化:

从反应速率和化学平衡两个角度解释实验 I、II 现象背后的原因可能是:。
已知X、Y、Z均为中学化学常见物质,且均含有同一种元素,其中X是单质,它们之间的转化关系如图所示。则X、Y、Z不可能是( )

| 物质 选项 | X | Y | Z |
| A | Na | Na2O | NaOH |
| B | Fe | FeCl3 | FeCl2 |
| C | Mg | Mg(OH)2 | MgO |
| D | Si | SiO2 | Na2SiO3 |
A . A
B . B
C . C
D . D
已知下列转化关系中M、N均为单质 ,则M、N可能是( )
M+N  Q
Q  Q溶液
Q溶液 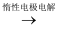 M+N
M+N
A . Cu、Cl2
B . S、O2
C . O2、Na
D . Al、Cl2
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间的转化关系如图所示(反应条件己略去)。下列有关物质的推断正确的是( )
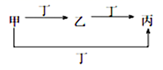

A . A
B . B
C . C
D . D
为探究某黄色固体的组成和性质,设计如下实验:

请回答:
-
(1) X 的化学式是。
-
(2) X 在空气中充分灼烧的化学方程式为。
-
(3) 溶液 A 与烧碱反应生成 B 和浅黄色沉淀(0.01mol)的化学方程式为。
在给定条件下,下列物质间转化能实现的是( )
A . S  SO2
SO2  H2SO3
B . NH3
H2SO3
B . NH3 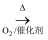 NO2
NO2  HNO3
C . Fe2O3
HNO3
C . Fe2O3  Fe
Fe  FeCl3
D . Al
FeCl3
D . Al  NaAlO2
NaAlO2  Al(OH)3
Al(OH)3
 SO2
SO2  H2SO3
B . NH3
H2SO3
B . NH3 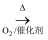 NO2
NO2  HNO3
C . Fe2O3
HNO3
C . Fe2O3  Fe
Fe  FeCl3
D . Al
FeCl3
D . Al  NaAlO2
NaAlO2  Al(OH)3
Al(OH)3
央视《典籍里的中国》因袁隆平、宋应星两位科学家跨越时空的“握手”被刷上热搜。宋应星所著《天工开物》被誉为“百科全书之祖”。下列说法错误的是( )
A . “凡播种先以稻麦稿包浸数日俟其生芽撒于田中生出寸许其名曰秧。”。其中“稻麦稿”的主要成分纤维素。
B . “水火既济而土合······后世方土效灵人工表异陶成雅器有素肌、玉骨之象焉”以上所述的“陶成雅器”的主要原料是黏土、石灰石
C . “凡火药,硫为纯阳,硝为纯阴,此乾坤幻出神物也”,“硝”指的是硝酸钾。
D . “凡铸镜模用灰沙铜用锡和”该法所制铜镜主要成分为青铜。
关于化合物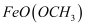 的性质,下列推测不合理的是( )
的性质,下列推测不合理的是( )
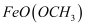 的性质,下列推测不合理的是( )
的性质,下列推测不合理的是( )
A . 与稀盐酸反应生成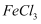 、
、 、
、 B . 隔绝空气加热分解生成
B . 隔绝空气加热分解生成 、
、 、
、 C . 溶于氢碘酸(
C . 溶于氢碘酸(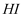 ),再加
),再加 萃取,有机层呈紫红色
D . 在空气中,与
萃取,有机层呈紫红色
D . 在空气中,与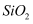 高温反应能生成
高温反应能生成
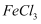 、
、 、
、 B . 隔绝空气加热分解生成
B . 隔绝空气加热分解生成 、
、 、
、 C . 溶于氢碘酸(
C . 溶于氢碘酸(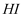 ),再加
),再加 萃取,有机层呈紫红色
D . 在空气中,与
萃取,有机层呈紫红色
D . 在空气中,与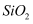 高温反应能生成
高温反应能生成
最近更新



