高三化学上学期上册试题
合金已成为飞机制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.
【实验方案一】将铝镁合金与足量NaOH溶液反应,测定剩余固体质量.实验中发生反应的化学方程式是______
【实验步骤】
(1)称取5.4g铝镁合金粉末样品,溶于VmL 2.0mol/LNaOH溶液中,充分反应.则NaOH溶液的体积V≥ ______ .
(2)过滤、洗涤、干燥、称量固体.该步骤中若未洗涤固体,测得镁的质量分数将______ (填“偏高”、“偏低”或“无影响”).
【实验方案二】
将铝镁合金与足量稀硫酸溶液反应,测定生成气体在通常状况(约20℃,1.01105Pa)的体积.
【问题讨论】
(3)同学们拟选用图1实验装置完成实验:
![]()
①你认为最简易的装置其连接顺序是:A接______ 接______ 接______ (填接口字母,可不填满.)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶.请你帮助分析原因.______ .
③实验结束时,在读取测量实验中生成氢气的体积时,你认为合理的是______ .
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平,读取量筒中水的体积
(4)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小.于是他们设计了图2所示的实验装置.
①装置中导管a的作用是______ .
②实验前后碱式滴定管中液面读数分别为V1mL、V2mL.则产生氢气的体积为______ mL.
广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其它简单仪器组成各种功能的装置.下列各图中能用作防倒吸安全瓶的是( )
A.  B.
B.  C.
C.  D.
D. 
生活中碰到的某些问题,常需要用化学知识解释,下列说法不正确的是
A.做馒头时加少量小苏打,是为了使馒头更加松软
B.药皂中掺入少量的苯酚,是由于苯酚有杀菌作用
C.食盐中加入少量碘酸钾,人食用后可补充人体内碘元素的不足
D.腌制火腿时添加少量NaNO2,是为了使火腿肉的味道更加美味可口
在某温度下可逆反应:Fe2(SO4)3+6KSCN![]() 2Fe(SCN)3+3K2SO4达到平衡状态后加入少量下列何种固体物质,该平衡几乎不发生移动( )
2Fe(SCN)3+3K2SO4达到平衡状态后加入少量下列何种固体物质,该平衡几乎不发生移动( )
A、NH4SCN B、K2SO4 C、NaOH D、FeCl3·6H2O
某学生准备用37%、密度为1.19 g/mL的浓盐酸配制0.1 mo1·L-1的稀盐酸500 mL。请回答下列问题:
(1)量取浓盐酸的体积为 mL,应选用量筒的规格为 mL。
(2)配制时应选用容量瓶的规格为 mL。
(3)配制时(除容量瓶外)还需选用的仪器主要有烧杯、 、 和试剂瓶。
短周期主族元素X、Y、Z、W原子序数依次增大,其中只有Y、Z处于同一周期且相邻,Z是地壳中含量最多的元素,W是短周期中金属性最强的元素。下列说法正确的是( )
A.原子半径:r(X) < r(Y) < r(Z) < r(W)
B.W的最高价氧化物的水化物是一种弱碱
C.Y的单质的氧化性比Z的强
D.X、Y、Z 三种元素可以组成共价化合物和离子化合物
氮及其化合物的转化过程如图所示。下列分析合理的是

A.催化剂a表面发生了极性共价键的断裂和形成
B.N2与H2反应生成NH3的原子利用率为100%
C.在催化剂b表面形成氮氧键时,不涉及电子转移
D.催化剂a、b能提高反应的平衡转化率
某学习小组设计了下列装置进行相关实验,装置和使用的药品均正确且能达到相应实验目的的是( )

A.制备Cl2 B.干燥并收集SO2
C.制硝酸铜 D.制备NaHCO3
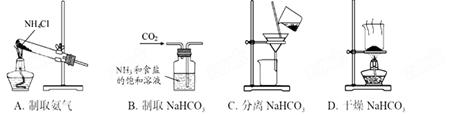
根据侯氏制碱原理制备少量NaHCO3的实验,经过制取氨气、制取NaHCO3、分离NaHCO3、干燥NaHCO3四个步骤,下列图示装置和原理能达到实验目的的是( )
氮的氧化物是大气的主要污染物,是当前环保工作的重要研究内容之一。
(1)氨气还原氮的氧化物
①N2(g)+O2(g)=2NO(g) △H1 ②4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H2
则4NH3(g)+6NO(g)=5N2(g)+6H2O(1) △H=________。(用含△H1、△H2的式子表示)
依据反应②,可将氨气直接用于燃料电池,用KOH溶液作电解质溶液,写出负极电极反应式: 。
 (2)一定温度下,向2L恒容密闭容器中充入4.0mol NO2和4.0mol CO,在催化剂作用下发生反应4CO(g)+2NO2(g)
(2)一定温度下,向2L恒容密闭容器中充入4.0mol NO2和4.0mol CO,在催化剂作用下发生反应4CO(g)+2NO2(g) ![]() N2(g)+4CO2(g) △H<0,测得相关数据如下:
N2(g)+4CO2(g) △H<0,测得相关数据如下:
①0~5min,用NO2的浓度变化表示的反应速率为____。
②以下表述能说明该反应己达到平衡状态的是____。
A.气体颜色不再变化 B.气体密度不再变化 C.气体平均相对分子质量不再变化
③20 min时,保持温度不变,继续向该容器中加入l.0mol NO2和l.0molCO,在t1时反应再次达到平衡,则NO2的转化率比原平衡____(填“增大”、“减小”或“不变)。
④该温度下反应的化学平衡常数K= _____。
(3)湿法脱硝:采用NaClO2 溶液作为吸收剂可对烟气进行脱硝。323 K 下,向足量碱性NaClO2 溶液中通入含NO 的烟气,充分反应后,溶液中离子浓度的分析结果如下表:
| 离子 | NO3- | NO2- | Cl- |
| c/(mol • L-1) | 2.0×10-4 | 1.0×10-4 | 1.75×10-4 |
①NaClO2 溶液显碱性,用离子方程式解释原因_______________________。
②依据表中数据,写出NaClO2溶液脱硝过程中发生总反应的离子方程式____________。
中国古代“炼丹术”中蕴含了丰富的化学知识,为近代化学的建立和发展奠定了基础。下列关于“炼丹术”中涉及的史实解释错误的是
| 选项 | 史实 | 解释 |
| A | “胡粉 | 复分解反应原理 |
| B | “有硇水者,剪银塊(Ag)投之,则旋而为水” | 氧化还原反应原理 |
| C. | “曾青(硫酸铜)涂铁,铁赤色如铜……外变而内不化也” | 置换反应原理 |
| D | “铁釜代替土釜,加热丹砂(HgS),可增采也” | 平衡移动原理 |
A.A B.B C.C D.D
(1)X、Y、Z三种液体的近似pH如图,下列判断正确的是___________。

A.X一定是酸或强酸弱碱盐溶液 B.Y一定是90℃时的纯水
C.Y液体一定呈中性 D.Z可能是Na2SiO3溶液
(2)物质的量浓度相同的三种溶液:①NH4Cl②氨水③NH4HSO4,c(NH4+)大小顺序正确的
是___________。
A.①>②>③ B.③>①>② C.②>③>① D.③>②>①
(3)比较填空(选填“>"或“ <"或"=”)
①常温下两种溶液:a.pH=4盐酸 b.pH=4NH4Cl溶液,其中水的电离程度大小:a__________b。
 ②已知某可逆反应aA(g)+bB(g)
②已知某可逆反应aA(g)+bB(g)![]() cC(g)+dD(g)。当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如右图所示,则反应物和生成物的化学计量数之和:a+b ______c+d。
cC(g)+dD(g)。当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如右图所示,则反应物和生成物的化学计量数之和:a+b ______c+d。
(4)在一定体积的密闭容器中加入1molCO2和1mol H2,进行如下化学反应:CO2(g)+ H2(g) ![]() CO(g)+H2O(g) ,其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g) ,其化学平衡常数K和温度T的关系如下表:
| T(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
①该反应的化学平衡常数表达式为K=__________________________。
②反应为___________反应(填“吸热”或“放热”)。
③800℃,向容器内充入lmolCO2、lmolH2、lmol CO、lmolH2O,此刻反应的v正_______v逆(填“>"或“<”或“=”)
(1)有机反应类型很多,下列反应类型中可能属于加成反应范畴的是(填编号) 。
A.氧化反应 B.还原反应
C.加聚反应 D.缩聚反应
E.硝化反应 F.酯化反应
G.裂化反应 H.磺化反应
L.水解反应 J.皂化反应
K.油脂的氢化反应
(2)已知1 mol某有机物含碳原子n mol,在恰好完全燃烧时消耗氧气1.5 n mol,生成产物只有二氧化碳和水,则该有机物的化学式可能为 (用n表示分子内碳原子数,你认为有几种化学式就填几种)。
下列说法正确的是( )
A.乙烯和甲烷都能发生加聚反应
B.甲烷和乙烯都可以与氯气反应
C.酸性高锰酸钾溶液可以氧化苯和甲烷
D.乙烯可以与氢气发生加成反应,苯不能与氢气加成
关于氧化物的叙述正确的是( )
A、酸性氧化物都可以跟强碱溶液反应
B、与水反应可生成酸的氧化物都是酸性氧化物
C、金属氧化物都是碱性氧化物
D、不能跟酸反应的氧化物一定能跟碱反应
下列各组物质中,前者属于电解质,后者属于非电解质的是( )
A.二氧化碳、BaSO4 B.盐酸、蔗糖 C.KNO3、乙醇 D.NaOH、氯气
像对待生命一样对待生态环境” ,下列做法不符合这一思想的是( )
A.推广使用可降解塑料及布质购物袋,以减少“白色污染”
B.用Ba(OH)2消除水中Cu2+等重金属离子污染
C.汽油抗爆:甲基叔丁基醚代替四乙基铅
D.大力推广燃料“脱硫、脱硝”技术,减少硫氧化物和氮氧化物对空气的污染
“中国名片”中航天,军事、天文等领城的发展受到世界瞩目,它们与化学有着密切联系。下列说法错误的是
A. “中国天眼”的“眼眶”是钢铁结成的圈梁,其属于黑色金属材料
B. “歼—20” 飞机上大量使用的碳纤维是一种新型有机高分子材料
C. “神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷是新型无机非金属材料
D. “天宫二号”空间实验室的硅电池板将光能直接转换为电能
A、B、C、D、E、F是六种短周期主族元素,其中D、E同主族,C、E同周期,A的核电荷数等于其电子层数,B、D形成的化合物可用于制不粘锅的保护膜,B、E形成的某种化合物是一种常见的有机溶剂,C的次外层电子数是最外层电子数的4倍,D的单质可与水反应置换出F的单质。下列说法不正确的是
A.离子半径:E>F>D>C>A B.含氧酸的酸性可能为:B>E
C.A、B、F形成的某种化合物可使澄清石灰水变浑浊 D.A与C形成的化合物溶于水显酸性
下列说法正确的是( )
A.投入铁片产生H2的溶液中可大量存在H+、Mg2+、SO![]() 、NO
、NO![]()
B.将过量二氧化硫气体入冷氨水中:SO2+NH3·H2O===HSO![]() +NH
+NH![]()
C.用酒精萃取碘水中的碘,水从分液漏斗下口放出,碘的酒精溶液从分液漏斗上口倒出
D.高炉炼铁原理是用一氧化碳还原四氧化三铁



