福建省“百校联考”2020届高三7月教学摸底质量检查理科综合化学免费试卷
| 1. 选择题 | 详细信息 |
|
历史文物本身蕴含着许多化学知识,下列说法错误的是( ) A.战国曾侯乙编钟属于青铜制品,青铜是一种合金 B.秦朝兵马俑用陶土烧制而成,属硅酸盐产品 C.宋王希孟《千里江山图》所用纸张为宣纸,其主要成分是碳纤维 D.对敦煌莫高窟壁画颜料分析,其绿色颜料铜绿的主要成分是碱式碳酸铜 |
|
| 2. 选择题 | 详细信息 |
以高硫铝土矿(主要成分为Al2O3、Fe2O3,还含有少量FeS2)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如图,下列叙述错误的是( ) A.烧渣分离可以选择用磁铁将烧渣中的Fe3O4分离出来 B.隔绝空气焙烧时理论上反应消耗的n(FeS2)∶n(Fe2O3)=1∶5 C.向滤液中通入过量CO2、过滤、洗涤、灼烧沉淀可制得Al2O3 D.加入CaO可以减少SO2的排放同时生成建筑材料CaSO4 |
|
| 3. 选择题 | 详细信息 |
煤的干馏实验装置如图所示。下列说法错误的是( ) A.c口导出的气体可使新制氯水褪色 B.从b层液体中分离出苯的操作是分馏 C.长导管的作用是导气和冷凝 D.可用蓝色石蕊试纸检验a层液体中含有的NH3 |
|
| 4. 选择题 | 详细信息 |
X、Y、Z、W是原子序数依次增大的短周期元素,且X、Z原子序数之和是Y、W原子序数之和的1/2。甲、乙、丙、丁是由这些元素组成的二元化合物,M是某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下)。上述物质间的转化关系如图所示(部分反应物和生成物省略)。下列说法正确的是( ) A.含W元素的盐溶液可能显酸性、中性或碱性 B.化合物N与乙烯均能使溴水褪色,且原理相同 C.原子半径:r(Y)>r(Z)>r(W) D.Z与X、Y、W形成的化合物中,各元素均满足8电子结构 |
|
| 5. 选择题 | 详细信息 |
铅蓄电池是常见的二次电池,其原理图如图所示。铅蓄电池的工作原理为:Pb+PbO2+2H2SO4 A.铅蓄电池的结构中O2的作用可提高电池的工作效率 B.铅蓄电池放电时Pb电极的电极反应为:Pb-2e-=Pb2+ C.电池工作时,H+移向PbO2板 D.实验室用铅蓄电池作电源,用惰性电极电解CuSO4溶液,当阴极析出2.4g铜时,铅蓄电池内消耗H2SO4物质的量至少是0.075mol |
|
| 6. 选择题 | 详细信息 |
我国科研人员以蹄叶橐吾为原料先制得化合物Ⅰ再转化为具有抗癌抑菌活性的倍半萜化合物Ⅱ,有关转化如图所示,下列有关说法错误的是( ) A.化合物Ⅰ能使酸性KMnO4溶液褪色 B.检验化合物Ⅱ中是否含化合物Ⅰ,可用Br2的CCl4溶液 C.化合物Ⅱ一定条件下能发生取代、消去及加成反应 D.化合物Ⅰ分子中含有5个手性碳原子 |
|
| 7. 选择题 | 详细信息 |
25℃时,NaCN溶液中CN-、HCN浓度所占分数(δ)随pH变化的关系如图甲所示。向10mL0.01mol·L-1NaCN溶液中逐滴加入0.01mol·L-1的盐酸,其pH变化曲线如图乙所示[其中a点的坐标为(9.5,0.5)]。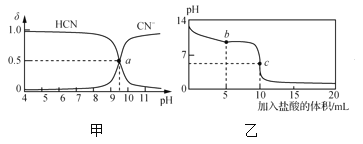 下列溶液中的关系中正确的是( ) A.常温下,NaCN的水解平衡常数:Kh(NaCN)=10-4.5mol/L B.图甲中pH=7的溶液:c(Cl-)=c(HCN) C.图乙中b点的溶液:c(CN-)>c(Cl-)>c(HCN)>c(OH-)>c(H+) D.图乙中c点的溶液:c(Na+)+c(H+)=c(HCN)+c(OH-)+c(CN-) |
|
| 8. | 详细信息 |
粉煤灰是燃煤产生的重要污染物,主要成分有A12O3、Fe2O3、Fe3O4和SiO2等物质。综合利用粉煤灰不仅能够防止环境污染,还能获得纳米Fe2O3等重要物质。 已知:i伯胺R-NH2能与Fe3+反应:3R-NH2+Fe3++SO42-+H2O ii Fe3+在水溶液中能与Cl-反应:Fe3++6Cl- (1)写出过程I中Fe2O3发生反应的离子方程式:____。 (2)过程II加入过量H2O2的作用是 ___ 。 (3)过程II加入伯胺一煤油对浸取液进行分离,该操作的名称是_____。 (4)从化学平衡角度解释过程III利用NaCI溶液进行反萃取的原理:_____。 (5) N2H4具有碱性,可与H+结合生成N2H5+。过程IV中先用过量的N2H4将水层2中Fe3+转化为Fe2+并生成N2,反应的离子方程式为____,得到的Fe2+再被O2氧化为FeOOH。 (6)纳米Fe2O3在常压电化学法合成氨过程中起催化作用。该电解装置如图所示。 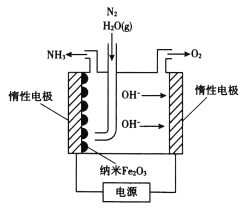 已知熔融NaOH-KOH为电解液,Fe2O3在阴极发生电极反应生成中间体Fe。用化学用语表示Fe2O3在阴极催化生成NH3的反应过程。 第一步:____, 第二步:____。 |
|
| 9. 实验题 | 详细信息 |
甲苯(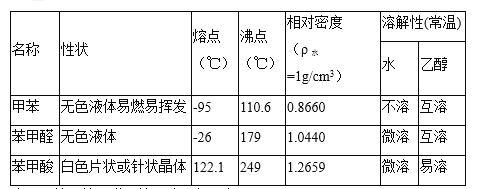 注:甲苯、苯甲醛、苯甲酸三者互溶。 实验室可用如图装置模拟制备苯甲醛。实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入2mL甲苯和一定量其它试剂,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时。  (1)装置a的名称是_____,主要作用是________。三颈瓶中发生反应的化学方程式为_______。 (2)经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是_________。 (3)反应完毕,反应混合液经过自然冷却至室温后,还应经过__________、________(填操作名称)等操作,才能得到苯甲醛粗产品。 (4)实验中加入过量的过氧化氢并延长反应时间时,会使苯甲醛产品中产生较多的苯甲酸。 ①若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的实验步骤是______(按步骤顺序填字母)。 a.对混合液进行分液 b.过滤、洗涤、干燥 c.水层中加入盐酸调节pH=2 d.与适量碳酸氢钠溶液混合振荡 ②若对实验①中获得的苯甲酸(相对分子质量为122)产品进行纯度测定,可称取2.500g产品,溶于200mL乙醇配成溶液,量取所得的乙醇溶液20.00mL于锥形瓶,滴加2~3滴酚酞指示剂,然后用预先配好的0.1000 mol/L KOH标准液滴定,到达滴定终点时消耗KOH溶液18.00mL。产品中苯甲酸的质量分数为_______(保留一位小数)。下列情况会使测定结果偏低的是____(填字母)。 a.滴定终了俯视读取数据 b.KOH标准液长时间接触空气 c.配制KOH标准液时仰视定容 d.将指示剂换为甲基橙溶液 |
|
| 10. 综合题 | 详细信息 |
|
NO2和N2O4的相互转化2NO2(g) Ⅰ.将N2O4 (g)转化为N2O4(l),可用来制备硝酸。 (1)已知2NO2(g) 下列能量变化示意图正确的是__________。 A.  B. B. C. C. (2)NO2和N2O4物质的量之比为1:1与O2和H2O恰好完全反应的化学方程式为__________。 Ⅱ.对于2NO2(g) 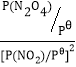 ,其中Pθ为标准压强(1×105 Pa),P(N2O4)和P(NO2)为各组分平衡分压(平衡分压=总压×物质的量分数)。 ,其中Pθ为标准压强(1×105 Pa),P(N2O4)和P(NO2)为各组分平衡分压(平衡分压=总压×物质的量分数)。(1)若起始NO2的物质的量设为1mol,反应在恒定温度和标准压强下进行,N2O4的平衡产率为0.75,则Kθ=____________。 (2)利用现代手持技术传感器可以探究压强对2NO2(g)  ①B点时NO2的转化率为_______。 ②E、H两点对应气体的平均相对分子质量ME____MH(填“<、>或=”)。 Ⅲ.以连二硫酸根(S2O42-)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:  (3)①阴极区的电极反应式为_________。 ②NO吸收转化后的主要产物为NH4+,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标准状况下的体积为____mL。 Ⅳ.常温下,将a mol·L-1的醋酸与bmol·L-1Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=_____(用含a和b的代数式表示)。 |
|
| 11. 综合题 | 详细信息 |
|
已知可以由下列反应合成三聚氰胺:CaO+3C (1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:_____。 CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和___(填化学式),由此可以推知CN22-的空间构型为___。 (2)尿素分子中C原子采取____杂化。尿素分子的结构简式是____。 (3)三聚氰胺  俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸 俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸 后,三聚氰酸与三聚氰胺分子相互之间通过____结合,在肾脏内易形成结石。 后,三聚氰酸与三聚氰胺分子相互之间通过____结合,在肾脏内易形成结石。(4)H2与O2发生反应的过程用模型图示如下(“—”表示化学键):  其中过程Ⅰ是___过程(填“吸热”、“放热”或“没有能量变化”)。图④中产生了由极性键构成的_______分子(填“极性”或“非极性”)。 (5)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为_____。  已知CaO晶体的密度为ρ,求晶胞中距离最近的两个钙离子之间的距离_____(列出计算式)CaO晶体和NaCl晶体的晶格能分别为:CaO3401kJ·mol-1、NaCl786kJ·mol-1。导致两者晶格能差异的主要原因是________。 |
|
| 12. 推断题 | 详细信息 |
有机物K是某药物的前体,合成路线如图所示: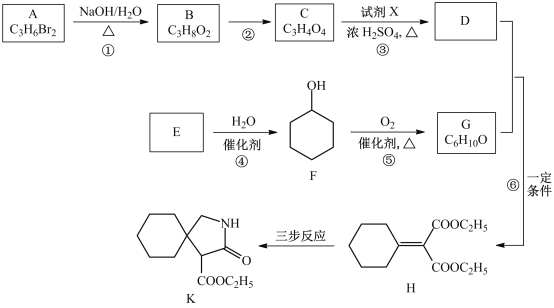 已知:R-CN (1)A的名称是_____________。 (2)反应①的化学方程式是___________________。 (3)反应②的类型是__________________。 (4)反应③中的试剂X是________________。 (5)E属于烃,其结构简式是_________________。 (6)H中所含的官能团是_________________。 (7)反应⑥的化学方程式是_____________________。 (8)H经三步反应合成K,写出中间产物I和J的结构简式______________。 |
|
最近更新



