元江哈尼族彝族傣族自治县第一中学高二化学2019年上册开学考试免费试卷完整版
| 1. 选择题 | 详细信息 |
|
焰色反应不呈黄色的是( ) A. 氯化钠 B. 过氧化钠 C. 氢氧化钠 D. 氢氧化钾 |
|
| 2. 选择题 | 详细信息 |
|
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂,实验室可通过以下反应制得:2KClO3+H2C2O4+H2SO4===2ClO2↑+2CO2↑+K2SO4+2H2O。下列有关该反应的说法正确的是( ) A. KClO3在反应中失去电子 B. ClO2是还原产物 C. H2C2O4在反应中被还原 D. 1 mol H2C2O4参加反应有4 mol电子转移 |
|
| 3. 选择题 | 详细信息 |
|
将ag某物质在足量氧气中充分燃烧再将气体生成物通入足量的Na2O2充分反应,固体增重为bg,若a<b,则该物质可能是( ) A. H2 B. CO C. 乙酸(CH3COOH) D. 甲烷(CH4) |
|
| 4. 选择题 | 详细信息 |
|
下列物质中同时含有氯分子和氯离子的是( ) A. 氯水 B. 液态氯化氢 C. 液氯 D. 氯酸钾溶液 |
|
| 5. 选择题 | 详细信息 |
|
关于气体摩尔体积的下列叙述中正确的是 ( ) A. 气体摩尔体积是单位物质的量的气体所占的体积 B. 标准状况下,气体摩尔体积约为22.4 L C. 标准状况下,1 mol任何物质所占的体积约是22.4 L D. 标准状况下,1 mol氢气所占的体积约是22.4 L·mol-1 |
|
| 6. 选择题 | 详细信息 |
|
萃取在生产和科学实验中有着广泛应用。下列混合物的分离中,需要应用萃取这种分离方法的是 A. 海水淡化 B. 分离豆浆和豆渣 C. 用海水晒盐 D. 从碘水中提取碘 |
|
| 7. 选择题 | 详细信息 |
|
NA表示阿伏加德罗常数的值,下列说法正确的是 A. 标准状况下,0.1NA个水分子所占的体积约为2.24 L B. 11.2 L CO2的物质的量为0.5 mol C. NH3的摩尔质量等于NA个氨分子的质量之和 D. 101 kPa、4 ℃时,18 mL水和202 kPa、27 ℃时32 g O2所含分子数均为NA |
|
| 8. 选择题 | 详细信息 |
|
已知氯化碘(ICl)的性质类似于卤素,有很强的化学活性。ICl跟Zn、H2O分别发生如下反应:2ICl+2Zn=ZnCl2+ZnI2,ICl+H2O=HCl+HIO,下列叙述正确的是( ) A. 在Zn跟ICl的反应中,ZnCl2既是氧化产物又是还原产物 B. 在Zn跟ICl的反应中,ZnCl2既不是氧化产物又不是还原产物 C. 在H2O跟ICl的反应中,ICl既是氧化剂又是还原剂 D. 在H2O跟ICl的反应中,ICl既不是氧化剂又不是还原剂 |
|
| 9. 选择题 | 详细信息 |
|
下列叙述中不正确的是( ) A. 氯化氢的摩尔质量是36.5g·mol-1 B. 含有6.02×1023个氧原子的磷酸的物质的量是0.25mol C. amol水和amol二氧化碳所含分子数目相同 D. 2H既可以表示2个氢原子又可以表示2 mol氢原子 |
|
| 10. 选择题 | 详细信息 |
海藻中含有丰富的碘元素。如图是实验室从海藻里提取碘的流程的一部分。下列判断正确的是 A. 步骤④的操作是过滤 B. 可用淀粉溶液检验步骤②的反应是否进行完全 C. 步骤①、③的操作分别是过滤、萃取 D. 步骤③中加入的有机溶剂可能是酒精或四氯化碳 |
|
| 11. 选择题 | 详细信息 |
|
下列有关电解质的说法中正确的是( ) A. 固体氯化镁不导电,所以氯化镁不是电解质 B. 三氧化硫水溶液的导电性很好,所以三氧化硫是电解质 C. 熔融的铁导电性很好,所以铁是电解质 D. 氯化钾熔融状态能导电,所以氯化钾是电解质 |
|
| 12. 选择题 | 详细信息 |
|
将两支盛有液态苯的试管分别插入95 ℃的水和4 ℃的水中,发现苯分别沸腾和凝固,以上事实说明( ) A. 苯的熔点比水的低、沸点比水的高 B. 苯的熔点比水的高、沸点比水的低 C. 苯的熔点、沸点都比水的高 D. 苯的熔点、沸点都比水的低 |
|
| 13. 选择题 | 详细信息 |
|
下列微粒中,核外电子总数为10的是( ) A. Na+ B. CO2 C. CO D. N2 |
|
| 14. 选择题 | 详细信息 |
|
下列过程没有发生化学键变化的是 A. 生石灰投入水中 B. 氯化氢气体通入水中 C. 冰融化成水 D. 高锰酸钾固体受热分解 |
|
| 15. 选择题 | 详细信息 |
|
下列叙述不正确的是( ) A. 苯和乙烯分子都是平面结构 B. 苯和乙烯分子中都含有C=C双键,它们的性质相似 C. 苯属于不饱和烃,能与氢气发生加成反应 D. 苯分子中碳碳键是介于单键和双键之间的独特的键 |
|
| 16. 选择题 | 详细信息 |
|
海水提溴过程中,将溴吹入吸收塔,使溴蒸气和吸收剂SO2发生作用以达到富集的目的,化学反应为Br2+SO2+2H2O=2HBr+H2SO4,下列说法正确的是( ) A. Br2在反应中表现氧化性 B. SO2在反应中被还原 C. Br2在反应中失去电子 D. 1mol Br2在反应中得到1mol电子 |
|
| 17. 选择题 | 详细信息 |
|
下列物质中,使溴水和酸性高锰酸钾溶液都能褪色的是( ) A. 丙烯 B. 苯 C. 乙烷 D. 硝酸 |
|
| 18. 选择题 | 详细信息 |
|
某胶体遇盐卤(MgCl2)或石膏水发生凝聚,而遇食盐水或硫酸钠溶液不易发生凝聚,下列说法中错误的是( ) A. 胶体粒子直径在l~100 nm之间 B. 遇BaCl2溶液或氢氧化铁胶体可发生凝聚 C. 电泳时,该胶体向阴极方向移动 D. 钠离子使此胶体凝聚的效果不如Ca2+、Mg2+ |
|
| 19. 选择题 | 详细信息 |
|
下列说法正确的是( ) A. 从锂到铯,碱金属的单质都能与氯气反应 B. Na2O2是过氧化物,KO2是超氧化物,它们都不是氧化物 C. 碱金属单质都能与氧气反应,反应条件是加热或点燃 D. 碱金属单质在空气中燃烧,都能生成过氧化物 |
|
| 20. 选择题 | 详细信息 |
|
能将太阳能转化为电能的材料是( ) A. 硅 B. 二氧化硅 C. 硅酸钠 D. 硅酸钙 |
|
| 21. 选择题 | 详细信息 |
|
区别乙醇、苯和溴苯,最简单的方法是( ) A. 加入金属钠 B. 加酸性高锰酸钾溶液后振荡,静置 C. 加蒸馏水后振荡,静置 D. 加硝酸银溶液后振荡,静置 |
|
| 22. 选择题 | 详细信息 |
|
下列关于 SO2性质的说法中,不正确的是( ) A. 能KMnO4溶液褪色 B. 能使品红溶液褪色 C. 能与 NaOH 溶液反应 D. 能与水反应生成硫酸 |
|
| 23. 选择题 | 详细信息 |
|
向碘水中加入适量CCl4并振荡,静置后观察到的现象是 A. 形成均匀的无色溶液 B. 形成均匀的紫红色溶液 C. 液体分层,下层呈紫红色 D. 液体分层,上下层均呈无色 |
|
| 24. 选择题 | 详细信息 |
|
加入Al能产生H2的溶液中一定能大量共存的是 A. K+、Na+、Br﹣、SO42- B. Na+、Ba2+、ClO﹣、Cl﹣ C. Ca2+、Cl﹣、HCO3-、K+ D. NH4+、K+、OH﹣、SO42- |
|
| 25. 选择题 | 详细信息 |
|
下列说法中错误的是( ) ①化学性质相似的有机物是同系物 ②分子组成相差一个或几个CH2原子团的有机物是同系物 ③若烃中碳、氢元素的质量分数相同,它们必定是同系物 ④互为同分异构体的两种有机物的物理性质有差别,但化学性质必定相似 A. ①②③④ B. 只有②③ C. 只有③④ D. 只有①②③ |
|
| 26. 推断题 | 详细信息 |
(1)将红热的固体单质甲放入显黄色的浓乙溶液中,剧烈反应,产生混合气体A,A在常温下不与空气作用,发生如下图所示的变化。 则:①写出下列物质的化学式: 丙__________,B____________,C__________, D____________。 ②写出甲跟乙反应的化学方程式:__________________________。 ③单质丙与溶液乙反应生成气体B的离子方程式:___________________。 (2)如图是各物质的反应关系图:已知A和E都是黄色粉末,F有刺激性气味且有漂白性。请据此回答下列问题: 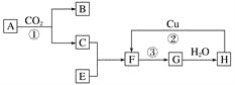 写出图中编号的化学方程式: ①_______________________; ②_______________________; ③______________________。 |
|
| 27. 综合题 | 详细信息 |
已知:A 是石油裂解气的主要产物之一,其产量常用于衡量一个国家石油化工发展水平的标志。下列是有机物 A~G 之间的转化关系: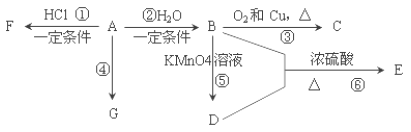 请回答下列问题: (1)A 的官能团的名称是___________; C 的结构简式是________; (2)E 是一种具有香味的液体, 由 B+D→E 的反应方程式为___________, 该反应类型是______________; (3)G 是一种高分子化合物,其结构简式是______________; (4)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射物质 F(沸点 12.27°C)进行应急处理.写出由A 制 F 的化学反应方程式______________。 (5)E 的同分异构体能与 NaHCO3溶液反应,写出该同分异构体的结构简式_______。 |
|
| 28. 实验题 | 详细信息 |
下图是一个实验室制取氯气并以氯气为原料进行特定反应的装置(B中有导管和一个连通外界的长颈漏斗):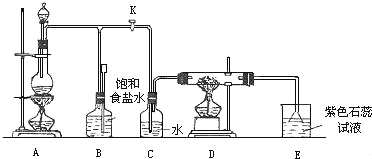 (1)A是氯气发生装置,其中反应的化学方程式为__________________________. (2)实验开始时,先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处酒精灯,Cl2通过C瓶后再进入D。D装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为CO2和HCl。试写出D中反应的化学方程式:___________________;装置C的作用是_________________ 。 (3)在E处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是__。 (4)若将E处烧杯中溶液改为澄清石灰水,反应过程中现象为___。(选填标号) (A)有白色沉淀生成(B)无明显变化(C)先生成白色沉淀,而后白色沉淀消失 (5)D处反应完毕后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有Cl2产生,此时B中的现象是__,B的作用是___________________________________。 |
|
| 29. 实验题 | 详细信息 |
实验室用燃烧法测定某固体有机物A的分子组成,测定装置如图(铁架台、铁夹、酒精灯等未画出):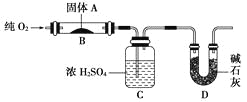 取17.1 g A放入装置中,通入过量O2燃烧,生成CO2和H2O,请回答下列有关问题: (1)通入过量O2的目的是______________________________________________。 (2)C装置的作用是__________________________________________; D装置的作用是_____________________________________________。 (3)通过该实验,能否确定A中是否含有氧原子?________。 (4)若A的摩尔质量为342 g/mol,C装置增重9.99 g,D装置增重26.4 g,则A分子式为____________。 (5)写出A燃烧的化学方程式_____________________________________。 (6)A可发生水解反应,1 mol A可水解生成2 mol同分异构体,则A在催化剂作用下水解的化学方程式为_________________________________________。 |
|
| 30. 推断题 | 详细信息 |
已知A、B、F是家庭中常见的有机物,E是石油化工发展水平的标志,F是一种常见的高分子材料。根据下面转化关系回答下列问题: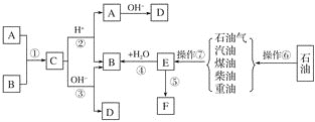 (1)操作⑥、操作⑦的名称分别为________、________。 (2)下列物质中沸点最高的是________。 A 汽油 B 煤油 C 柴油 D 重油 (3)在①~⑤中属于取代反应的是________;原子利用率为100%的反应是________。(填序号) (4)写出结构简式:A________、F________。 (5)写出反应③的离子方程式:___________。 (6)作为家庭中常见的物质F,它给我们带来了极大的方便,同时也造成了环境污染,这种污染称为________。 |
|
最近更新



