2018年至2019年高二上册期中考试化学试卷(河北省辛集中学)
| 1. 选择题 | 详细信息 |
|
下列说法正确的是 A. 氯水能导电,所以氯气是电解质 B. 碳酸钡不溶于水,所以它是非电解质 C. 固体磷酸是电解质,所以磷酸在熔融状态下和溶于水时都能导电 D. 胆矾虽不能导电,但它属于电解质 |
|
| 2. 选择题 | 详细信息 |
|
在醋酸溶液中,CH3COOH的电离达到平衡的标志是 A. 溶液显电中性 B. 溶液中无CH3COOH分子 C. 氢离子的浓度恒定不变 D. c(H+)=c(CH3COO-) |
|
| 3. 选择题 | 详细信息 |
|
下列各式中,属于正确的电离方程式的是 A. HCO3-+H2O B. HCO3-+OH-=H2O+CO32- C. NH3+H+=NH4+ D. NH3•H2O |
|
| 4. 选择题 | 详细信息 |
用如图所示装置分别进行下列各组物质的导电性实验,小灯泡的亮度比反应前明显减弱的是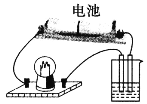 A. 向亚硫酸钠溶液中通入氯气 B. 向硝酸银溶液中通入少量氯化氢 C. 向氢碘酸饱和溶液中通入少量氧气 D. 向氢氧化钠溶液中通入少量氯气 |
|
| 5. 选择题 | 详细信息 |
|
已知NaHSO4在水中的电离方程式为NaHSO4 A. 该温度高于25 ℃ B. 由水电离出来的H+的浓度为1×10-10 mol·L-1 C. 加入NaHSO4晶体会抑制水的电离 D. 取该溶液加水稀释100倍,溶液中的c(OH-)减小 |
|
| 6. 选择题 | 详细信息 |
|
下列叙述中与盐类的水解有关的是 ①纯碱溶液去油污 ②铁在潮湿的环境下生锈 ③NH4Cl与ZnCl2溶液可作焊接工艺中的除锈剂 ④盛放Na2CO3溶液的试剂瓶用橡皮塞而不能用玻璃塞 ⑤酸雨在空气中放置一段时间pH降低 ⑥草木灰与铵态氮肥不能混合施用 A. ①③④⑥ B. ①②⑤⑥ C. ①③④⑤ D. 全部 |
|
| 7. 选择题 | 详细信息 |
|
对于常温下pH为2的硫酸,下列叙述正确的是 A. c(H+)=c(SO42-)+c(OH-) B. 与等体积pH=12的氨水混合后所得溶液显酸性 C. 由H2O电离出的c(H+)=1.0×10-12 mol·L-1 D. 与等体积0.01 mol·L-1的乙酸钠溶液混合后所得溶液中:c(SO42-)=c(CH3COO-) |
|
| 8. 选择题 | 详细信息 |
|
用标准盐酸滴定未知浓度的NaOH溶液,下列各操作不会引起实验误差的是 A. 用蒸馏水洗净滴定管后,装入标准盐酸进行滴定 B. 用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,而后装入一定体积的NaOH溶液进行滴定 C. 用碱式滴定管取10.00 mL NaOH溶液放入用蒸馏水洗净的锥形瓶中,再加入适量蒸馏水进行滴定 D. 用25 mL碱式滴定管取NaOH溶液,起始时读数为15.00 mL,到滴定终点时NaOH溶液恰好全部放出 |
|
| 9. 选择题 | 详细信息 |
|
在温度不变的条件下,将0.1 mol·L-1氨水加水稀释,随着水的加入,下列关系式的数值变小的是 A. |
|
| 10. 选择题 | 详细信息 |
|
将10 mL pH =1的CH3COOH 溶液加水稀释至100 mL后,溶液的pH为 A. 2 B. 2<pH<7 C. 1<pH<2 D. 无法判断 |
|
| 11. 选择题 | 详细信息 |
|
下列有关CaCO3的溶解平衡的说法中不正确的是 A. CaCO3沉淀析出和沉淀溶解不断进行,但速率相等 B. CaCO3难溶于水,其饱和溶液不导电,属于弱电解质溶液 C. 升高温度,CaCO3的溶解度增大 D. 向CaCO3沉淀中加入纯碱固体,CaCO3溶解的量减少 |
|
| 12. 选择题 | 详细信息 |
如图表示的是某离子X的水解过程示意图,则离子X可能是( ) A.CO32- B.HCO3- C.Na+ D.NH4+ |
|
| 13. 选择题 | 详细信息 |
|
一定温度下,下列溶液的离子浓度关系式正确的是 A. pH=5的H2S溶液中,c(H+)= c(HS-)=1×10—5mol·L—1 B. pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 C. pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+ c(H+)= c(OH-)+c( HC2O4-) D. pH相同的①CH3COO Na②NaHCO3③NaClO三种溶液的c(Na+):①>②>③ |
|
| 14. 选择题 | 详细信息 |
|
常温下某氨水的pH=x,某盐酸的pH=y,已知x+y=14,且x<11,若将上述氨水与盐酸等体积混合后,所得溶液中各种离子浓度由大到小的排列顺序为 A. c(Cl-)>c(NH4+)>c(OH-)>c(H+) B. c(Cl-)>c(NH4+)> c(H+)> c(OH-) C. c(NH4+)> c(Cl-)> c(H+)> c(OH-) D. c(NH4+)> c(Cl-)> c(OH-)> c(H+) |
|
| 15. 选择题 | 详细信息 |
|
某溶液中只含有Na+、H+、OH-、A-四种离子,下列说法正确的是( ) A.若溶液中c(A-)=c(Na+),则溶液一定呈中性 B.溶液中不可能存在:c(Na+)> c(A-)> c(OH-)> c(H+) C.若c(OH-)> c(H+),溶液中不可能存在:c(Na+)> c(OH-)> c(A-)> c(H+) D.若溶质为NaA、HA,则一定存在:c(A-)> c(Na+)> c(H+)> c(OH-) |
|
| 16. 选择题 | 详细信息 |
|
常温下将pH=8的NaOH溶液稀释1000倍,稀释后溶液中c(Na+)与c(OH-)之比接近( ) A. 1:102 B. 1:1 C. 102:1 D. 1:103 |
|
| 17. 选择题 | 详细信息 |
|
常温下,pH=8与 pH=10的NaOH溶液按体积比1:100混合后,溶液中c(H+)接近 A. 10-10 B. 10-8 C. 2×10-10 D. 2×10-8 |
|
| 18. 选择题 | 详细信息 |
某温度时,AgCl(s)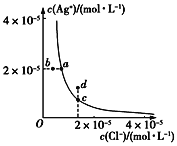 A. 加入AgNO3可以使溶液由c点变到d点 B. 加入固体NaCl,则AgCl的溶解度减小,Ksp也减小 C. d点有AgCl沉淀生成 D. a点对应的Ksp小于b点对应的Ksp |
|
| 19. 选择题 | 详细信息 |
25℃时不断将水滴入0.1mol·L-1的氨水中,下列图像变化合理的是( )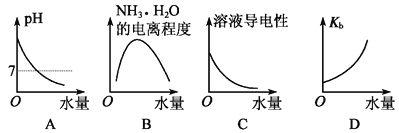 A. A B. B C. C D. D |
|
| 20. 选择题 | 详细信息 |
|
铝和镓的性质相似,如M(OH)3都是难溶的两性氢氧化物。在自然界镓常以极少量分散于铝矿(如Al2O3) 中。用NaOH溶液处理铝矿(Al2O3)时,生成NaAlO2、NaGaO2;而后通入适量CO2, 得 Al(OH)3沉淀,而NaGaO2留在溶液中(循环多次后成为提取镓的原料)。发生后一步反应是因为 A. 镓酸酸性强于Al(OH)3 B. Al(OH)3酸性强于镓酸 C. 镓浓度小,所以不沉淀 D. Al(OH)3酸性强于碳酸 |
|
| 21. 选择题 | 详细信息 |
|
常温下,若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,原因可能是 A. 生成了一种强酸弱碱盐 B. 弱酸溶液和强碱溶液反应 C. 强酸溶液和弱碱溶液反应 D. 一元强酸溶液和二元强碱溶液反应 |
|
| 22. 选择题 | 详细信息 |
|
下列有关物质的量浓度关系正确的是 A. 物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合,溶液呈酸性:c(CH3COO-)<c(CH3COOH) B. pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(CH3COONa)<c(Na2CO3) C. 0.1mol·L-1的NaHA溶液,其pH=4,则c(HA-)>c(H+)>c(H2A)>c(A2-) D. pH=2的HA溶液与pH=12的MOH溶液任意比混合后溶液中离子浓度关系:c(H+)+c(M+) = c(OH-)+c(A-) |
|
| 23. 计算题 | 详细信息 |
|
t ℃时,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1。已知a+b=12,请回答下列问题: (1)该温度下水的离子积常数Kw=________________。 (2)该溶液中由水电离出的c(OH-)=_________________。 (3)该温度下,将NH3溶于水得100 mL 0.1 mol·L-1的氨水,测得pH=9,则该条件下,NH3· H2O的电离平衡常数Kb为______________________。 |
|
| 24. 填空题 | 详细信息 |
|
(1)向K2CO3溶液中滴加酚酞,观察到的现象____________________,产生这种现象的原因是(用离子方程式回答)___________________________________________若将此溶液微热,观察到的现象________________________________,原因是__________________________________ (2)向K2CO3溶液中加入AlCl3溶液,反应的离子方程式是__________________________ (3)将K2CO3溶液蒸干得到的物质是______________________ 若将KHCO3溶液蒸干灼烧得到的物质是__________ |
|
| 25. 实验题 | 详细信息 | |||||||||||||||||||||||
|
某烧碱样品含有少量不与酸作用的杂质,为了测定其纯度,进行以下滴定操作: A. 在250 mL的容量瓶中定容配制250 mL烧碱溶液; B. 用碱式滴定管移取25.00 mL烧碱溶液于锥形瓶中并滴入2滴甲基橙指示剂; C. 在天平上准确称取烧碱样品2.0 g,在烧杯中用蒸馏水溶解; D. 将物质的量浓度为0.100 0 mol·L-1的标准盐酸装入酸式滴定管,调整液面记下开始读数为V1; E. 在锥形瓶下垫一张白纸,滴定至终点,记下读数V2。 就此实验完成下列填空: (1)正确的操作步骤的顺序是(用编号字母填写) ________→________→________→D→________。 (2)上述E中锥形瓶下垫一张白纸的作用是_______________________________ (3)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视______________。直到加入一滴盐酸后,溶液____________________________ (填颜色变化)。 (4)下列操作中可能使所测NaOH溶液的浓度数值偏低的是(____________) A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸 B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥 C.酸式滴定管在滴定前有气泡,滴定后气泡消失 D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 (5)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为________mL。 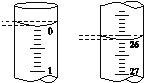 (6)某学生根据3次实验分别记录有关数据如表:
|
||||||||||||||||||||||||
| 26. 综合题 | 详细信息 | ||||||||||||||||||
利用水钴矿[主要成分为Co2O3和Co(OH)3,还有少量Fe2O3、Al2O3、MnO等]制取CoCl2·6H2O的工艺流程如图所示: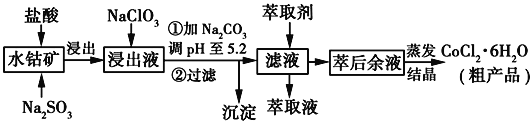 已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等: 已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等:②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
|
|||||||||||||||||||
最近更新