2019黑龙江高一上学期人教版(2019)高中化学期末考试
| 1. | 详细信息 |
|
下列有关金属及其合金的说法不正确的是 A.目前我国流通的硬币是由合金材料制造的 B.生铁、普通钢和不锈钢中的碳含量依次增加 C.镁在空气中燃烧发出耀眼的白光,可用于制作照明弹 D.日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 |
|
| 2. | 详细信息 |
|
如将物质按照单质、氧化物、酸、碱、盐分类,下列各组物质中,类别相同的是 A.氧气、氧化镁、四氯化碳、水 B.硫酸铜、氯化钠、碳酸钙、硫化钾 C.硫酸、碳酸钠、氯化镁、氧化钠 D.硝酸银、氢氧化钠、醋酸钠、氯化钾 |
|
| 3. | 详细信息 |
|
同温同压下,等质量的下列气体所占有的体积最大的是 A.CH4 B.O2 C.CO2 D.SO2 |
|
| 4. | 详细信息 |
|
在水溶液中能大量共存,且加入过量稀硫酸时,有气体生成的是 A. Na+、Ag+、CO32-、Cl- B. K+、 Ba2+、 SO42-、Cl- C. Na+、K+、CO32-、Cl- D. Na+、K+、Cl-、SO42- |
|
| 5. | 详细信息 |
|
离子方程式BaCO3 + 2H+ = CO2↑ + H2O + Ba2+ 中的H+不能代表的物质是 ①HCl;②H2SO4;③HNO3;④NaHSO4;⑤CH3COOH A.①③ B.①④⑤ C.②④⑤ D.①⑤ |
|
| 6. | 详细信息 |
|
粗盐提纯实验用到的试剂中,不是为了除去原溶液中杂质离子的是 A.盐酸 B.烧碱溶液 C.纯碱溶液 D.氯化钡溶液 |
|
| 7. | 详细信息 |
|
下列离子方程正确的是 A.饱和石灰水中通入过量二氧化碳:OH- + CO2 = HCO3- B.向稀硫酸中投入铁粉:2Fe +6H+ = 2Fe3+ +3H2 ↑ C.实验室制取二氧化碳:CO32- + 2H+ = H2O +CO2 ↑ D.氢氧化钡溶液中加入硫酸:H+ + OH- =H2O |
|
| 8. | 详细信息 |
|
下列反应中,铁元素被氧化的是 A.FeS +2HCl = FeCl2 + H2S↑ B.Fe +H2SO4 = FeSO4 +H2↑ C.FeO + 2HCl =FeCl2 +H2O D.2FeCl3 +Cu = 2FeCl2 + CuCl2 |
|
| 9. | 详细信息 |
|
把Ba(OH)2溶液滴入明矾溶液中,使SO42-全部转化成BaSO4沉淀,此时铝元素的主要存在形式是 A.Al3+ B.Al(OH)3 C.AlO2- D.Al3+和Al(OH)3 |
|
| 10. | 详细信息 |
|
硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液中,形成无色的溶液,其化学方程式是:PbSO4+2CH3COONH4===Pb(CH3COO)2+(NH4)2SO4。当Pb(CH3COO)2(醋酸铅)溶液中通入H2S时,有黑色沉淀PbS和弱电解质CH3COOH生成。表示这个反应的有关离子方程式正确的是 A.Pb(CH3COO)2+ H2S=== PbS↓+2CH3COOH B.Pb2++H2S ===PbS↓+2H+ C.Pb2++2CH3COO-+ H2S===PbS↓+2CH3COOH D.Pb2++2CH3COO-+2H++S2-===PbS↓+2CH3COOH |
|
| 11. | 详细信息 |
|
取一块金属钠放在燃烧匙里加热,观察到下列实验现象:①金属钠熔化 ②在空气中燃烧,放出紫色火花 ③燃烧后得到白色固体 ④燃烧时火焰为黄色 ⑤燃烧后生成淡黄色的固体物质,描述正确的是 A.①② B.①②③ C.①④ D.①④⑤ |
|
| 12. | 详细信息 |
|
将a g由CO和H2组成的混合气体在足量的O2中充分燃烧后,将生成的所有产物通过足量的Na2O2固体,Na2O2固体增加的质量为 A.a g B. C. |
|
| 13. | 详细信息 |
|
用含有少量镁的铝片制取纯净的氢氧化铝,下述操作步骤中最恰当的组合是 ①加盐酸溶解 ②加过量烧碱溶液溶解 ③过滤 ④通入过量CO2生成Al(OH)3沉淀 ⑤加入盐酸生成Al(OH)3沉淀 ⑥加入过量烧碱溶液生成Al(OH)3沉淀 A.①⑤⑥③ B.②③⑥③ C.②③④③ D.②③⑤③ |
|
| 14. | 详细信息 |
|
某溶液中有Na+、Mg2+、Fe2+、Al3+四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是 A.Na+ B.Mg2+ C.Fe2+ D.Al3+ |
|
| 15. | 详细信息 | |||||||||||||||
|
材料与化学密切相关,表中对应关系错误的是
|
||||||||||||||||
| 16. | 详细信息 |
|
下列应用与二氧化硅的性质无关的是 A.氢氟酸不能用玻璃瓶盛装 B.实验室中盛放碱液的试剂瓶用橡皮塞而不用玻璃塞 C.可用来做石英钟、石英表,耐高温的石英玻璃 D.硅胶是常用的干燥剂及催化剂的载体 |
|
| 17. | 详细信息 |
|
下列叙述中正确的是 A.液溴易挥发,在存放液溴的试剂瓶中应加水封 B.能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 C.某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- D.某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+ |
|
| 18. | 详细信息 |
|
向100mLFeBr2溶液中通入标况下氯气3.36L,氯气全部被还原,测得溶液c(Br-)=c(Cl-),原溶液中FeBr2溶液的浓度(mol·L-1) A.1 B.1.5 C.2 D.2.5 |
|
| 19. | 详细信息 |
|
羟氨(NH2OH)是一种还原剂.将25.00mL 0.049mol/L的羟氨酸性溶液与足量硫酸铁在煮沸条件下反应,生成的Fe2+又恰好被24.50mL 0.020mol/L的酸性KMnO4溶液所氧化.在上述反应中,羟氨的氧化产物为 A.NO2 B.NO C.N2O D.N2 |
|
| 20. | 详细信息 | ||||||||||||||||||||||||||||||
|
奥运会会旗是五环旗,假定奥运五环旗中的每一环表示一种物质,相连环的物质间一定条件下能发生常见反应,不能相连环的物质间不能发生反应,且四种反应中必须包含化合反应、置换反应及复分解反应,则下列适合的一组可能是
|
|||||||||||||||||||||||||||||||
| 21. | 详细信息 |
|
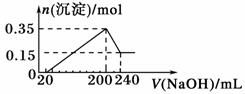
将一定质量的Mg和Al的混合物投入500 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如下图所示。则下列说法正确的是 A.Mg和Al的总质量为8 g B.原稀硫酸溶液的物质的量浓度为5 mol·L-1 C.生成的H2在标准状况下的体积为11.2 L D.NaOH溶液的物质的量浓度为5 mol·L-1 |
|
| 22. | 详细信息 |
|
有一铁的氧化物样品,用50mL 5mol·L-1盐酸可恰好使其完全溶解。所得溶液可吸收标准状况下0.56L氯气,使其中的Fe2+全部转化为Fe3+。该样品可能的化学式为 A.Fe4O5 B.Fe3O4 C.Fe5O7 D.Fe8O11 |
|
| 23. | 详细信息 |
|
下列物质在一定条件下都能导电,属于电解质的是 A.铜 B.NaOH C.SO3 D.浓硫酸 |
|
| 24. | 详细信息 |
|
下列各物质,所含原子数目最多的是 A.标准状况下,22.4L甲烷 B.标准状况下,44.8L氮气和氧气的混合气体 C.常温常压下,66g二氧化碳气体 D.100mL 1mol/L硫酸溶液 |
|
| 25. | 详细信息 |
|
按要求回答问题: (1)完成下列化学方程式: ①将金属钠加入到硫酸铜溶液中的化学方程式: ②漂白粉失效的化学方程式: ③实验室制取氯气的化学方程式: (2)用化学方程式或离子方程式完成下列转化: ①Al3+ → AlO2-→ Al(OH)3 ②Fe(OH)2 → Fe(OH)3 ③CO2 → C |
|
| 26. | 详细信息 |
|
某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题: (1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L 的溶液。在FeCl2溶液中需加入少量铁屑,其目的是_____________。 (2)甲组同学取2 mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为________________。 (3)乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl2溶液中先加入0.5 mL 煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是_____________。 (4)丙组同学取10 ml 0.1 mol·L-1KI溶液,加入6 mL 0.1 mol·L-1 FeCl3溶液混合。分别取 2 mL 此溶液于2支试管中进行如下实验: ①第一支试管中加入1 mL CCl4充分振荡、静置,CCl4层显紫色; ②第二支试管中加入1滴KSCN溶液,溶液变红。 实验②说明:在I-过量的情况下,溶液中仍含有______(填离子符号)。 (5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为___________________________。 |
|
| 27. | 详细信息 |
|
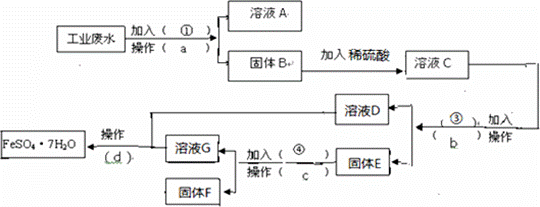
某工厂的工业废水中含有大量的FeSO4,较多的CuSO4和少量Na2SO4.为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜.请根据下列流程图,完成回收硫酸亚铁和铜的实验方案.(可供选择的试剂为铁粉、稀H2SO4、NaOH溶液等试剂) (1)操作a的名称为 ,所需要的玻璃仪器为 。 (2)固体E的成分为 ,加入的试剂④为 ,发生的化学方程式为 。 (3)加入试剂①的目的是 。 (4)从溶液D和溶液G中得到FeSO4•7H2O晶体的操作为 。 |
|
| 28. | 详细信息 |
|
实验室用浓盐酸和MnO2制Cl2,并以干燥的Cl2为原料进行实验,装置如下图所示。
(1)装置B、C中应盛放的试剂名称分别为__________、_________;从A装置导出的气体若不经过B、C装置而直接进入D管,将对实验产生的不良后果是___________________________。 (2)实验时,先点燃A处的酒精灯,让氯气充满装置,再点燃D处酒精灯,写出D中反应的化学方程式:_________________________________________。 (3)F装置所起的作用是____________________,____________________。 (4)用的石灰乳吸收氯气可制得漂粉精,写出工业制漂粉精反应的化学方程式: ___________________________________________________________________。 |
|