第5节 物质的溶解 知识点题库
向右图试管里水中加入某种物质后,U形管左端的红墨水液面降低,
则加入的物质是( )
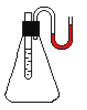
A . 氢氧化钠
B . 蔗糖
C . 硝酸铵
D . 食盐
有碳酸镁与氧化镁的混合物共重12.4克,把该混合物加入到192克稀盐酸中恰好完全反应,称得反应后溶液的质量为200克.试计算反应后所得溶液中溶质的质量分数.(写出具体计算过程)
实验室保存﹣瓶浓盐酸,瓶上的标签部分内容如图所示,请根据标签上的信息回答下列各问:
(1)这﹣瓶浓盐酸中溶质的质量是多少克?(结果精确到0.1)
(2)取100克此瓶内的浓盐酸可以稀释成1.85%的稀盐酸多少克?同时加水多少克?

实验考查中小明配制了50g15%的食盐水,经检测质量分数偏高,可能原因是( )
A . 食盐中含有不溶杂质
B . 取水时俯视读数
C . 称量时物码放反
D . 转移至细口瓶时洒出
图1可表示“M与N的并列关系”,图2可表示“M属于N的从属关系”.下列概念间的关系符合图3所示关系的是( ) 
A . X:单质;Y:纯净物;Z:混合物
B . X:悬浊液;Y:乳浊液;Z:溶液
C . X:氧化物;Y:酸碱盐;Z:化合物
D . X:饱和溶液;Y:不饱和溶液;Z:浓溶液
观察是学习化学的重要方法,以下是某同学记录的化学实验现象,其中符合事实的是.
A.打开盛放浓盐酸的试剂瓶,瓶口冒出白烟
B.硫在氧气中燃烧,发出微弱的淡蓝色火焰,产生刺激性气味的气体
C.将二氧化碳倒入放有不同高度、燃着蜡烛的烧杯中,低层的蜡烛先熄灭
D.硝酸铵固体溶于水时大量的热.
已知X物质与Y物质的溶解度都随温度的升高而增大,20℃时,10g水中最多溶解4g X物质,30℃时,20g水中最多溶解 8g Y物质,则20℃时X与Y的溶解度相比是( )
A . X=Y
B . X<Y
C . X>Y
D . 无法比较
现有60℃的硝酸钾溶液500g,保持温度不变,蒸发掉10g水,则溶液中一定保持不变的是( )
A . 溶质的质量
B . 溶剂的质量
C . 溶液的质量
D . 硝酸钾的溶解度
在 20℃时,向 100g 水中加入 40g 氯化钾,充分搅拌,形成 134g 氯化钾溶液。则该溶液中氯化钾的质量分数为;20℃时氯化钾的溶解 度是g。
某温度时,在 100g 水中最多能溶硝酸钾 25g,现有该温度下 500g 硝酸钾溶液,加热蒸发掉 300g 水以后,冷却到原温度下,发现有 50g 硝酸钾晶体析出,请计算:
-
(1) 蒸发并冷却到原温度后,溶液中有多少克硝酸钾?此时溶液中硝酸钾的质量分数是多少?
-
(2) 蒸发前的溶液中,硝酸钾的质量分数是多少?
某“天气瓶"通过樟脑在酒精溶液中的结晶情况反映气温变化。如图为该“天气瓶”在三种不同气温下的状况,则瓶内溶液一定为相应气温下樟脑饱和溶液的是( )

A . 甲、乙
B . 甲、丙
C . 乙、丙
D . 甲、乙、丙
在一定条件下,将5克食盐放进盛有10克水的烧杯中,充分溶解后,烧杯底部沉积有1.4克食盐,此溶液的质量为( )
A . 15克
B . 16.4克
C . 11.4克
D . 13.6克
为了测定石灰石中碳酸钙的含量,小东进行了如下实验;取10.0g石灰石放于烧杯中,向烧杯中滴加稀盐酸,实验测得烧杯中剩余物质的质量与加入稀盐酸的质量之间的关系如图所示。整个过程不考虑稀盐酸的挥发和气体的溶解,石灰石中的杂质也不与稀盐酸反应。求:

-
(1) 产生CO2的总质量为g。
-
(2) 石灰石中碳酸钙的质量分数(写出计算过程)。
农业上常用饱和的食盐水选种。在室温保持不变的情况下,饱和食盐水露置在空气中一段时间后,有少量固体析出。对此过程的描述,下列图像正确的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
小华实验操作考试的题目是:配制一定溶质质量分数的碳酸钠溶液.考试时,小华进行了如图1所示的操作:

-
(1) 称量时C出现了右盘低的现象,则接下来小华的操作是。
-
(2) 以上实验的正确操作顺序为(用字母表示)。
-
(3) 小华量取蒸馏水的体积如图2所示,则小华配制的碳酸钠溶液中溶质的质量分数为。
-
(4) 下列原因能导致溶质质量分数偏低的是(填序号)。
①碳酸钠不纯 ②称量时,砝码和药品放错
③向烧杯中倒水时,有水洒出 ④量取水仰视凹液面最低处读数
图1是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线,图2是30℃时,取其中两种固体各1g分别放进盛有10g水的两支试管中,充分振荡后的溶解情况,下列说法正确的是 ( )

A . 甲物质的溶解度比乙物质的溶解度大
B . 加入试管1的固体是丙
C . 向烧杯中加入硝酸铵固体后,试管2中一定有晶体析出
D . 将30℃时甲、乙、丙三种物质的饱和溶液降温至20℃,所得溶液中溶质的质量分数的大小关系是: 乙>甲=丙
“配制一定溶质质量分数的氯化钠溶液”是初中科学基础实验之一,现要配置50克溶质质量分数为0.9%的生理盐水,下列有关操作与目的分析错误的是( )
| 选项 | 操作 | 目的 |
| A | 称量时,取出的过量氯化钠不能放回原试剂瓶内 | 防止污染药品 |
| B | 用量筒量取水时,视线要与凹液面最低处保持相平 | 使量取的水更准确 |
| C | 溶解过程,要用玻璃棒不断搅拌 | 增大食盐的溶解能力 |
| D | 称量时,在天平两托盘上各垫上一张相同的白纸 | 防止腐蚀天平 |
A . A
B . B
C . C
D . D
下图是某同学配制50g质量分数为15%的蔗糖溶液的操作过程示意图。试回答:

-
(1) 配制溶液的操作步骤有:①溶解;②称量;③计算;④装瓶存放。则正确的操作顺序是(填序号①~④)。
-
(2) A操作中实际称量结果为g(1g以下用游码)。
-
(3) E操作中玻璃棒的作用是。
-
(4) 如果配制的蔗糖溶液溶质质量分数小于15%,则造成误差的原因可能有。
①称量时砝码和蔗糖放反了,并且使用了游码; ②取水时仰视读数;
③溶解时有少量水溅出; ④装瓶时有溶液洒落。
把400克硝酸钾的不饱和溶液分成两等份,在温度不变的情况下,一份蒸发60克水,析出3克晶体,另一份蒸发80克水,析出8克晶体,则该温度下硝酸钾的溶解度为( )
A . 5克
B . 10克
C . 20克
D . 25克
60℃时,硝酸钾的溶解度为110g,该温度下硝酸钾饱和溶液中有关质量关系正确的是( )
A . 溶质质量∶溶剂质量=1∶10
B . 溶剂质量∶溶液质量=20∶21
C . 溶质质量∶溶剂质量=11∶10
D . 溶液质量∶溶质质量=21∶10
最近更新



