课题 3 利用化学方程式的简单计算 知识点题库
某兴趣小组为测定某品牌白醋含醋酸的质量分数,进行了如下实验:取10.0g白醋样品并向其中滴加溶质质量分数为2.0%的氢氧化钠溶液,当梢耗氢氧化钠溶液15.0g时,恰好完全反应.计算:该品牌白醋含醋酸酸的质量分数.
[提示:醋酸(CH3COOH)与氢氧化钠反应的化学方程式为CH3COOH+NaOH═CH3COONa+H2O;忽略白醋中其他物质与氢氧化钠的反应].
加热氯酸钾和二氧化锰的混合物162.5克,完全反应后生成氧气48克,求原来有多少克氯酸钾?二氧化锰的质量是多少克?
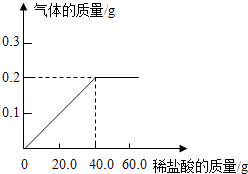
黄铜(铜锌合金)是重要的金属材料,常用来制造机械零件、仪表和日用品.为测定某黄铜材料中锌的含量,化学研究小组进行了实验:称取15.0g此黄铜材料,向其中逐渐加入稀盐酸,测定产生气体的质量和加入稀盐酸的质量,并根据实验情况绘制了产生气体质量与加入稀盐酸质量的关系图.
请你仔细分析此关系图,并进行计算:
-
(1) 15.0g黄铜材料中含锌 g.
-
(2) 稀盐酸中溶质的质量分数(写出计算过程),计算结果精确到0.1%).
学习小组的同学为探究某黄铜(铜、锌合金)样品中铜的质量分数,将10g黄铜样品放入质量为50g的烧杯中,然后向烧杯中逐滴加入稀硫酸,直至不在产生气体为止,共消耗稀硫酸的质量为100g,称量烧杯及内容物的总质量为159.9g,请计算黄铜样品中铜的质量分数.
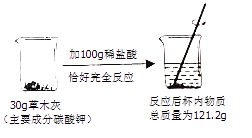
草木灰是农家肥料,其主要成分是碳酸钾,某化学兴趣小组进行如图实验,以下是他们的实验过程及数据(假设杂质不与稀盐酸反应,生成的气体全部逸出).请你回答下列问题:
-
(1) 碳酸钾中钾元素、碳元素、氧元素的质量比为;
-
(2) 反应后生成的气体质量为 g;
-
(3) 稀盐酸中溶质质量分数是多少?
如图是某胃药标签的部分内容.晓彤同学测定该药品中NaHCO3含量的过程如下:取10粒该药剂研碎后放入烧杯中,加入50g水后充分搅拌,再向其中滴加稀盐酸至溶液的pH=7时(已知药品中的其它成分既不溶于水,也不与稀盐酸反应),形成NaCl的不饱和溶液,共消耗稀盐酸11.5g,称得反应后烧杯内物质的总质量为64.3g.

请计算:
-
(1) 胃药中NaHCO3的质量分数.
-
(2) 反应后所得溶液中溶质的质量分数(计算结果精确到0.1%).
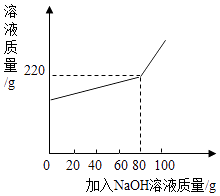
将一定量氯化镁和氯化钠的固体混合物加水配成145.8g的溶液,向所得溶液中加入一定浓度的氢氧化钠溶液,加入氢氧化钠溶液的质量与反应后溶液的质量关系如图.计算:
-
(1) 所用氢氧化钠溶液的溶质质量分数.
-
(2) 恰好完全反应时所得溶液的溶质质量分数为10%,则原固体混合物的质量是多少?
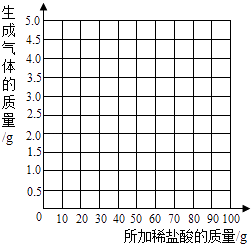
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
烧杯及所盛物质总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
请你据此分析计算:
-
(1) 第一次加入稀盐酸充分反应后,生成二氧化碳的质量是g.
-
(2) 该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
-
(3) 根据实验数据,在右边的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线.(不要求写出计算过程,只画出曲线即可)
一烧杯中盛有溶质质量分数为10%的CaCl2溶液,然后向烧杯中逐渐滴入溶质质量分数为10%的Na2CO3溶液至不再生成沉淀为止,过滤得到沉淀10g,将滤液蒸发掉90g水后,求所得溶液的溶质质量分数。
钴(Co)常见化合价为+2、+3。资料:氢氧化钴 Co(OH)2粉红色固体,难溶于水;氢氧化高钴Co(OH)₃
-
(1) 写出硫酸高钴的化学式;CoCO₃读作。
-
(2) 写出氯化钴溶液和氢氧化钠溶液反应的化学方程式。
-
(3) 2Co(OH)₃+6=2CoCl₂+Cl₂↑+6H₂O
-
(4) 177g钴在空气中加热至白热时完全燃烧生成g Co3O4
下列图象分别与选项中的操作相对应,合理的是( )
A . 向一定质量的稀盐酸中加水 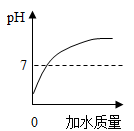 B . 一定条件下,一定质量的碳和氧气在密闭容器中反应
B . 一定条件下,一定质量的碳和氧气在密闭容器中反应 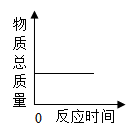 C . 等质量的镁和铁分别与足量的稀硫酸反应
C . 等质量的镁和铁分别与足量的稀硫酸反应 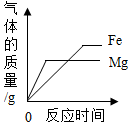 D . 一定温度下,向一定质量的饱和石灰水中加入氧化钙
D . 一定温度下,向一定质量的饱和石灰水中加入氧化钙 
 B . 一定条件下,一定质量的碳和氧气在密闭容器中反应
B . 一定条件下,一定质量的碳和氧气在密闭容器中反应  C . 等质量的镁和铁分别与足量的稀硫酸反应
C . 等质量的镁和铁分别与足量的稀硫酸反应  D . 一定温度下,向一定质量的饱和石灰水中加入氧化钙
D . 一定温度下,向一定质量的饱和石灰水中加入氧化钙 
下列四个图象,能正确反映对应变化关系的是( )
A . 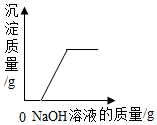 向氯化铜和盐酸的混合溶液中加入过量氢氧化钠溶液
B .
向氯化铜和盐酸的混合溶液中加入过量氢氧化钠溶液
B . 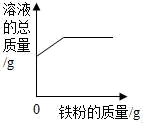 向一定量的硫酸铜溶液中加入铁粉
C .
向一定量的硫酸铜溶液中加入铁粉
C .  一定温度下,向不饱和硝酸钾溶液中加入硝酸钾
D .
一定温度下,向不饱和硝酸钾溶液中加入硝酸钾
D . 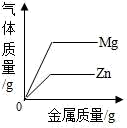 向两份等质量等浓度的稀盐酸中分别加入足量的锌粉和镁粉
向两份等质量等浓度的稀盐酸中分别加入足量的锌粉和镁粉
 向氯化铜和盐酸的混合溶液中加入过量氢氧化钠溶液
B .
向氯化铜和盐酸的混合溶液中加入过量氢氧化钠溶液
B .  向一定量的硫酸铜溶液中加入铁粉
C .
向一定量的硫酸铜溶液中加入铁粉
C .  一定温度下,向不饱和硝酸钾溶液中加入硝酸钾
D .
一定温度下,向不饱和硝酸钾溶液中加入硝酸钾
D .  向两份等质量等浓度的稀盐酸中分别加入足量的锌粉和镁粉
向两份等质量等浓度的稀盐酸中分别加入足量的锌粉和镁粉
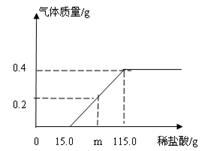
化学实验小组同学为研究某公共场所铁制护栏锈蚀的程度,将12.8g已生锈的铁片,放入一定浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如下图所示(假设铁片除有Fe2O3外,不含其他杂质)。
-
(1) m的值为;
-
(2) 该铁片中Fe2O3的质量分数(写出计算过程)。
下列四个图象能正确反映其对应实验操作的是( )
A . 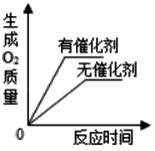 用2份完全相同的双氧水制取氧气
B .
用2份完全相同的双氧水制取氧气
B . 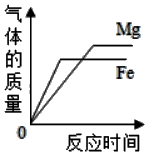 向足量且相同的稀盐酸中分别加入质量、形状相同的镁片和铁片
C .
向足量且相同的稀盐酸中分别加入质量、形状相同的镁片和铁片
C . 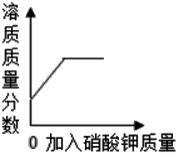 向某温度下不饱和硝酸钾溶液中加入硝酸钾晶体(温度不变)
D .
向某温度下不饱和硝酸钾溶液中加入硝酸钾晶体(温度不变)
D . 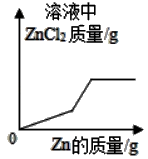 向一定质量FeCl2和CuCl2的混合溶液中逐渐加入足量锌粒
向一定质量FeCl2和CuCl2的混合溶液中逐渐加入足量锌粒
 用2份完全相同的双氧水制取氧气
B .
用2份完全相同的双氧水制取氧气
B .  向足量且相同的稀盐酸中分别加入质量、形状相同的镁片和铁片
C .
向足量且相同的稀盐酸中分别加入质量、形状相同的镁片和铁片
C .  向某温度下不饱和硝酸钾溶液中加入硝酸钾晶体(温度不变)
D .
向某温度下不饱和硝酸钾溶液中加入硝酸钾晶体(温度不变)
D .  向一定质量FeCl2和CuCl2的混合溶液中逐渐加入足量锌粒
向一定质量FeCl2和CuCl2的混合溶液中逐渐加入足量锌粒
某钢铁厂每天需消耗5000t含三氧化二铁76%的赤铁矿石,该厂理论上可日产含铁98%的生铁的质量是多少?
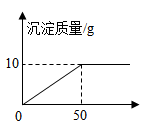
某校化学兴趣小组的同学取60g氯化钙(CaCl2)溶液,向其中加入适量碳酸钠(Na2CO3)溶液,反应完毕后过滤,所得固体用作制取牙膏摩擦剂的主要原料,同时所得滤液用来进行小麦选种(选种液要求氯化钠是质量分数在10%~20%之间)。实验过程中所加碳酸钠溶液的质量与生成碳酸钙沉淀的质量关系如图所示。通过如图可知:
-
(1) 当氯化钙恰好反应完时:消耗碳酸钠溶液的质量为g;
-
(2) 请通过计算回答,此时所得氯化钠溶液的质量分数是多少?能否用作小麦选种?
铜锌合金又称假黄金。向盛有20g铜锌合金粉末样品的烧杯中逐渐加入稀盐酸,生成氢气的质量与加入稀盐酸的质量关系如图所示,请计算:

-
(1) 合金样品中铜的质量分数。
-
(2) 恰好完全反应时,所得溶液中溶质的质量分数。(结果精确到0.1%)
如图是某种补钙药品标签上的部分文字。某兴趣小组同学,进行如下实验:取4片钙片(每片2.5g)研碎后,全部放入锥形瓶中,然后将80g稀盐酸分四次加入,每加一次盐酸充分反应后,称量锥形瓶内剩余物质质量(假设钙片中只有碳酸钙能与盐酸反应,且忽略水的蒸发及二氧化碳的溶解),然后再加稀盐酸,记录数据如下表:
|
第1次 |
第2次 |
第3次 |
第4次 |
|
|
稀盐酸的质量/g |
20 |
20 |
20 |
20 |
|
充分反应后剩余物质质量/g |
29.12 |
48.24 |
67.80 |
87.80 |
请回答下列问题:
-
(1) 第1次加入盐酸充分反应后产生二氧化碳的质量为g。
-
(2) 若要利用上述数据计算所用盐酸的浓度,应该选择第次实验数据,并求出质量分数?(写出计算过程)
-
(3) 该钙片中碳酸钙的质量分数为多少?(写出计算过程)
西安交通大学科研人员在新能源电池领域取得新进展,锂硫电池具有高的理论容量和能量密度、低成本和环境友好性等特点。其反应的化学方程式可简化为:2Li +S=Li2S,欲生产18.4克的Li2S,理论上需要金属锂的质量为多少?
4.4g丙烷(C3H8)和12.8g氧气在点燃条件下,恰好完全反应,生成CO2、CO和H2O,则生成水的质量为,该反应的化学方程式是。
最近更新



