科学探究的基本方法与意义 知识点题库
(1)需解决的内容主要有:如何判断铁矿石与铁块是不同的物质?
(2)对铁矿石和铁块分别进行通电测试,发现铁块导电,铁矿石不导电;
(3)铁块是不同于铁矿石的一种物质;
(4)分别用磁铁吸引铁矿石和铁块,发现铁块能被磁铁吸引,而铁矿石则不能;
(5)通电的方法不如用磁铁吸引的方法简便易行.
你认为以上探究活动环节中,属于提出问题的是 (填数字序号,下同);属于收集证据的是 ;属于获得结论的是 ;属于反思评价的是 .
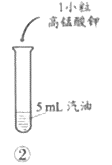
①取一小粒高锰酸钾晶体(实验室用的高锰酸钾晶体粒径为1~3mm),用毫米刻度尺测量并估算其体积为V mm3;
②将该高锰酸钾晶体溶解在有10mL水的试管1中;
③从试管1中取出1mL溶液,将其加入有9mL水的试管2中(第一次稀释);
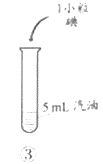
④从试管2中取出1mL溶液,将其加入有9mL水的试管3中;
⑤以上述方法继续稀释高锰酸钾溶液,到刚看不出高锰酸钾溶液的紫红色为止时,共稀释10次.
特别提示:已知在第9次稀释时,还能看出溶液呈淡紫红色.此时10mL溶液中有1 000个高锰酸根离子.该数据可作为本实验的估算比较标准.请回答以下问题:
-
(1) 在取1mL高锰酸钾溶液时,若俯视量筒读数,则所取溶液的体积. (填“大于”“等于”或“小于”)1mL.
-
(2) 下列教材中的哪一个实验,与本实验方法相似 .
A.验证植物光合作用产生氧气
B.测定空气中氧气的含量
C.用pH试纸测定溶液的酸碱度
D.探究物体所受浮力与排开水的关系
-
(3) 要提高该实验估算的准确度,下列哪两种改进方法一定正确 .
A.在一支试管中加入蒸馏水作为无色标准,与稀释后的溶液加以比对
B.每次稀释时都从试管中取2mL溶液,将其加入有18mL水的试管中
C.将高锰酸钾晶体放入盛有蒸馏水的量筒中,根据量筒中液面变化,测量其体积
D.用托盘天平称量一小粒高锰酸钾晶体的质量,根据其密度计算出体积
-
(4) 按该同学实验方法估算高锰酸根离子的大小约是 .(用式子表示)
提出问题:“假黄金”的化学组成是什么?
查阅资料:高温时炭可将金属活动顺序中铝以后的金属氧化物还原成金属单质;ZnCO3高温可分解成金属氧化物.
猜想:①“假黄金”可能由C、Zn、Cu三种单质组成;
②“假黄金”可能由ZnO、CuO、Cu2O三种氧化物组成;
③“假黄金”可能是单质和氧化物组成的混合物.
论证:他们经思考和推理后,首先排除了猜想 (选填①②或③),你觉得他们的理由是 .进而再排除了猜想 (选填①②或③).对余下的一种猜想,该同学又排除了其中的一种物质,你认为他们的依据是 .
进行实验:他们用实验鉴定了“假黄金”中所含的两种物质,请将实验过程填入下表中:
实验方法 | 观察到的现象 | |
步骤1 | | |
步骤2 | | |
得出结论:“假黄金”的化学组成是:

-
(1) 实验A可以探究水的组成。试管1产生的气体是,该反应的化学方程式为。
-
(2) B中观察到烧杯内壁有无色液滴,则该可燃性气体一定含有元素。
实验 |
|
|
|
现象 | 固体溶解,形成紫色溶液 | 固体几乎不溶解 | 固体溶解,形成紫红色溶液 |
-
(1) 对比实验①、②的现象,可得出的结论是。
-
(2) 设计实验②、③的目的是。
实验序号 | 实验目的 | 实验方案 | 实验现象 | 结论 |
实验1 | ①② | 草木灰的主要成分是碳酸钾 | ||
实验2 | 探究碳酸钾的性质 | 向碳酸钾溶液中滴入澄清石灰水 | 有白色沉淀生成 | 化学方程式为 |
实验3 | 探究实验2反应后上层清液中溶质的成分 | 上层清液中有两种溶质和 |
[反思]实验过程中产生的废液必须处理后再排放。请你对实验2反应产生的废液处理想出可行的方法。

-
(1) 写出有序号的仪器名称:①,②.
-
(2) 实验室制取氧气和二氧化碳均可选用的装置组合为,选用相同发生装置的原因是:.
-
(3) 某兴趣小组同学设计F装置,甲和乙中各盛有0.5g二氧化锰,同时将针筒Ⅰ中5mL5%的过氧化氢溶液和针筒Ⅱ中mL 15%的过氧化氢溶液注入甲和乙中,关闭弹簧夹,发现烧杯中右侧导管中产生气泡的速度比右侧快,说明化学反应速率与有关?该反应的化学方程式为:.
-
(1) 【查阅资料】①KOH与NaOH的化学性质相似。请用化学方程式解释KOH变质的原因是。
②K2CO3溶液呈碱性,CaCl2溶液,KCl溶液呈中性。
-
(2) 【猜想假设】假设I:只含KOH;假设II:含KOH和K2CO3;假设III:只含K2CO3。
【进行实验】
实验操作步骤
实验现象
实验结论
a.取少量样品于试管中,加入足量的稀盐酸
有气泡产生
假设错误
b.另取少量样品于试管中,加水溶解,加入过量的CaCl2溶液,振荡,静置
猜想II正确
c.取②中上层清液,滴加无色的酚酞试液
-
(3) 【拓展应用】完全变质的KOH也有利用价值,从K2CO3的组成或性质看,K2CO3在农业上的用途是(填一种即可)。
 改编自屠呦呦2015年12月7日瑞典演讲稿
改编自屠呦呦2015年12月7日瑞典演讲稿  。
。 很多中药古方都提到了青蒿入药抗疟疾,但当1971年开始从青蒿中提取有效成分时,结果却总是不理想,屠呦呦研究组反复研究中医古籍,其中“青蒿一握,以水两升渍,绞取汁,尽服之“激发了她的灵感,是不是高温下破坏了青蒿中抗疟的有效成分?屠呦呦立即改用乙醚在较低温度下进行提取,成功获得了抗疟有效单体的提纯物质,命名为青蒿素。
完成样品纯化后,通过元素分析、光谱测定、质谱及旋光分析等技术手段,测定相对分子质量为282,得出了青蒿素的化学式。但青蒿素的具体结构是什么样的呢?有机所得专家做了一个定性实验,加入碘化钾后,青蒿素溶液变黄了,说明青蒿素中含有过氧基团;而后专家又通过X射线衍射法等方法,最终确定了青蒿素是含有过氧基的新型倍半萜内酯。

由于自然界中天然青蒿素的资源是有限的,接下来就要把自然界的分子通过人工合成制成药物,在这一过程中,研究组又有一项重大研究成果,获得了青蒿素的衍生物,衍生物之一是双氢青蒿素,它也具有抗疟的疗效,并且更加稳定,水溶性好,比青蒿素的疗效好,10倍,进一步体现了青蒿素类药物“高效、速效、低毒”的特点。
依据文章内容,回答下列问题:
-
(1) 从中国古代青蒿入药,到2004年青蒿素类药物被世界卫生组织列为对抗疟疾的首选药物,经历了漫长的历程。将下列三项针对青蒿素的研究按时间先后排序(填数字序号)。
①确定结构 ②分离提纯 ③人工合成
-
(2) 屠呦呦用乙醚提取青蒿素,获得成功的关键在于改变了哪种条件:。
-
(3) 向无色的双氢青蒿素溶液中加入碘化钾,实验现象为。
-
(1) 实验名称。
-
(2) 实验用品。
-
(3) 实验目的 。
-
(4) 实验步骤及实验现象。
-
(5) 实验结论。
-
(6) 通过本实验,你有哪些收获?。
【查阅资料】①锌锰干电池的负极为锌筒;正极为带有铜帽的碳棒。
②滤液中可能含有NH4Cl和ZnCl2中的一种或两种。
③向ZnCl2溶液中逐滴滴入稀氨水,先生成白色沉淀,然后沉淀溶解。
-
(1) 【提出问题】黑色滤渣中可能含有哪些物质?滤液中溶质的主要成分是什么?
实验步骤
实验现象
实验结论
实验一
取黑色滤渣在氧气流中充分加热,产生无色无味气体,并将气体通入澄清的石灰水。
①澄清石灰水变浑浊,可用化学方程式表示为:
②有黑色粉末有剩余
根据现象(1)可知,黑色滤渣中一定含有元素
实验二
取实验一中剩余的黑色粉末于试管中,加入5mL5%的溶液,将带火星的木条放在试管口。
带火星的木条复燃
黑色粉末中可能含有MnO2
实验三
取少量无色滤液加入盛有NaOH固体的试管中,加热:将湿润的红色石蕊试纸放在试管口
红色石蕊试纸变蓝
滤液中溶质的成分为
另取适量无色滤液于试管中,逐滴加入稀氨水
先生成白色沉淀,然后沉淀
-
(2) 【交流反思】通过上述探究活动,体现化学学习的特点是。
A.关注物质的性质和变化
B.关注物质变化的过程以及对结果的解释和讨论