铝的化学性质 知识点题库
化学与生活密切相关,下列说法不正确的是( )
A . 为了防止食品受潮变质,常在食品包装袋中放入生石灰
B . 不可用铝制餐具长时间存放酸性或碱性食物
C . 光化学烟雾与氮氧化合物和碳氢化合物的大量排放有关
D . 为防止铁制品生锈,可以在铁制品的外层涂油漆或局部镀铜
把铝粉和某铁的氧化物(xFeO•yFe2O3)粉末配成铝热剂,分成两等份.一份在高温下恰好完全反应后,再与足量盐酸反应;另一份直接放入足量的烧碱溶液中充分反应.前后两种情况下生成的气体质量比是5:7,则x:y为( )
A . 1:1
B . 1:2
C . 5:7
D . 7:5
常温下能用铝制容器盛放的是( )
A . 稀硫酸
B . 氢氧化钠溶液
C . 浓硫酸
D . 硫酸铜溶液
给定条件下,下列选项中所示的物质间转化均能通过一步反应实现的是( )
A . 0.1 mol•L﹣1 HCl  Cl2
Cl2 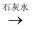 Ca(ClO)2(aq)
B . Al3+
Ca(ClO)2(aq)
B . Al3+ 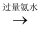 AlO2﹣
AlO2﹣  Al(OH)3
C . Al
Al(OH)3
C . Al  NaAlO2(aq)
NaAlO2(aq)  NaAlO2(s)
D . MgO(s)
NaAlO2(s)
D . MgO(s)  Mg(NO3)2(aq)
Mg(NO3)2(aq)  Mg(s)
Mg(s)
 Cl2
Cl2 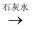 Ca(ClO)2(aq)
B . Al3+
Ca(ClO)2(aq)
B . Al3+ 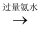 AlO2﹣
AlO2﹣  Al(OH)3
C . Al
Al(OH)3
C . Al  NaAlO2(aq)
NaAlO2(aq)  NaAlO2(s)
D . MgO(s)
NaAlO2(s)
D . MgO(s)  Mg(NO3)2(aq)
Mg(NO3)2(aq)  Mg(s)
Mg(s)
以Al2O3为原料制取氢氧化铝,最好的方法是( )
A . 将Al2O3溶于水
B . 将Al2O3先溶于盐酸中,之后滴加氢氧化钠溶液
C . 将Al2O3先溶于盐酸中,之后滴加氨水
D . 将Al2O3先溶于NaOH溶液中,之后再滴加盐酸
下列陈述Ⅰ、Ⅱ正确并且有因果关系的是( )
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | Na2O2能与二氧化碳、水反应放出O2 | Na2O2可用作呼吸面具的供氧剂 |
B | 铝比铁活泼 | 铝比铁更容易被腐蚀 |
C | 钠与水反应是放热反应 | 与水反应时,钠浮在水面上 |
D | 晶体硅熔点高硬度大 | 可用于制作半导体材料 |
A . A
B . B
C . C
D . D
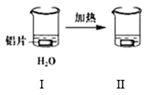
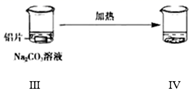
根据下列实验现象,所得结论正确的是( )
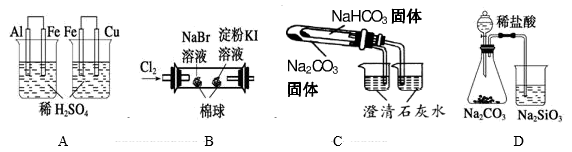
| 实验 | 实验现象 | 结论 |
| A | 左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 | 氧化性:Al3+>Fe2+>Cu2+ |
| B | 左边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
| C | 右烧杯中澄清石灰水变浑浊,左边烧杯中无明显变化 | 热稳定性:Na2CO3>NaHCO3 |
| D | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
A . A
B . B
C . C
D . D
某化学小组的同学取一定量的Al和Fe2O3的混合物进行铝热反应,并探究熔落物的成分。请回答下列问题:
-
(1) Ⅰ.引发铝热反应的实验操作是
-
(2) 做铝热反应时,内层纸漏斗底部剪一小孔用水润湿的目的是
-
(3) 反应的化学方程式为
-
(4) Ⅱ.已知:Al、Fe的熔、沸点数据如下:
物质
Al
Fe
熔点(℃)
660
1 535
沸点(℃)
2 467
2 750
某同学猜测,铝热反应所得到的熔落物是铁铝合金。理由:该反应放热能使铁熔化,而铝的熔点比铁低,所以铁和铝能形成合金。你认为他的解释是否合理?(填“合理”或“不合理”)。设计一个简单的实验方案,证明上述所得的熔落物中含有金属铝:
下列各组离子,在指定的环境中一定能大量共存的是( )
A . 某无色透明溶液中:NH4+、Ca2+、Cl-、CO32-
B . 与金属铝反应放出氢气的溶液:K+、NH4+、NO3-、Cl-
C . 滴加酚酞试液显红色的溶液:K+、Na+、CO32-、Cl-
D . c(Fe2+)=1mol/L的溶液:K+、NH4+、MnO4-、SO42-
下列反应没有氢气生成的是( )
A . 单质钠投入水中
B . 铝投入到氢氧化钠溶液中
C . 氧化钠投入水中
D . 往铁粉中通入水蒸气,并高温加热
金属及其化合物的转化关系是化学学习的重要内容之一。下列各组物质的各步转化关系中不能通过一步反应完成的是( )
A . Na→NaOH→Na2CO3
B . Fe→Fe(NO3)3→Fe(OH)3
C . Al→Al2O3→Al(OH)3
D . Mg→MgCl2→Mg(OH)2
将一定量的Mg、Al混合物投入200mL某浓度的盐酸中,金属完全溶解后,再逐滴加入2mol L-1的NaOH溶液至过量,所生成的沉淀与所加NaOH的关系如图所示。
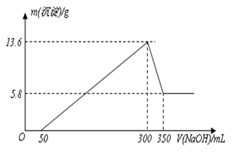
-
(1) 0~50mL段内,发生反应的离子方程式为。
-
(2) 300~350mL段内,发生反应的离子方程式为。
-
(3) 试计算该盐酸的浓度。(写出必要的计算过程)
从铝土矿(主要成分为Al2O3 , 还有少量杂质)中提取铝的工艺流程及步骤如下:
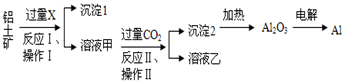
试回答下列问题:
-
(1) 试剂X为;
-
(2) 写出试剂X溶解Al2O3的化学方程式
-
(3) 操作Ⅰ、操作Ⅱ均为(填操作名称);
-
(4) 金属铝与氧化铁混合在高温下,会发生剧烈的反应,该反应的化学方程式为;
-
(5) 反应Ⅱ的离子方程式为;
-
(6) 电解熔融氧化铝制取金属铝,若有0.6 mol电子发生转移,理论上能得到金属铝的质量是g。
在含有Fe2+、Fe3+、Al3+、NH4+的溶液中加入足量的Na2O2固体,再加入过量的稀盐酸,完全反应后,离子数目几乎没有改变的是( )
A . Fe2+
B . Fe3+
C . Al3+
D . NH4+
下列指定反应的离子方程式正确的是( )
A . 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+
B . 用铝粉和NaOH溶液反应制取少量H2:Al+2OH−=  +H2↑
C . 室温下用稀HNO3溶解铜:Cu+2
+H2↑
C . 室温下用稀HNO3溶解铜:Cu+2  +2H+=Cu2++2NO2↑+H2O
D . NaHCO3溶液与足量的NaOH溶液混合:
+2H+=Cu2++2NO2↑+H2O
D . NaHCO3溶液与足量的NaOH溶液混合:  +OH-=
+OH-=  +H2O
+H2O
 +H2↑
C . 室温下用稀HNO3溶解铜:Cu+2
+H2↑
C . 室温下用稀HNO3溶解铜:Cu+2  +2H+=Cu2++2NO2↑+H2O
D . NaHCO3溶液与足量的NaOH溶液混合:
+2H+=Cu2++2NO2↑+H2O
D . NaHCO3溶液与足量的NaOH溶液混合:  +OH-=
+OH-=  +H2O
+H2O
探究铝片与  溶液的反应。
溶液的反应。
 溶液的反应。
溶液的反应。 | | | |
| 无明显现象 | 铝片表面产生细小气泡 | 出现白色浑浊,产生大量气泡(经检验主要为 |
下列说法错误的是( )
A .  溶液中存在水解平衡:
溶液中存在水解平衡: 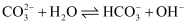 B . 对比Ⅰ、Ⅲ,说明
B . 对比Ⅰ、Ⅲ,说明  溶液能破坏铝表面的保护膜
C . 推测出现折色浑浊的可能原因为:
溶液能破坏铝表面的保护膜
C . 推测出现折色浑浊的可能原因为: 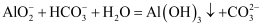 D . 加热及
D . 加热及  逸出对
逸出对  水解平衡移动方向的影响是相反的
水解平衡移动方向的影响是相反的
 溶液中存在水解平衡:
溶液中存在水解平衡: 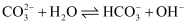 B . 对比Ⅰ、Ⅲ,说明
B . 对比Ⅰ、Ⅲ,说明  溶液能破坏铝表面的保护膜
C . 推测出现折色浑浊的可能原因为:
溶液能破坏铝表面的保护膜
C . 推测出现折色浑浊的可能原因为: 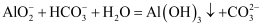 D . 加热及
D . 加热及  逸出对
逸出对  水解平衡移动方向的影响是相反的
水解平衡移动方向的影响是相反的
将a mol钠和a mol铝一同投入m g足量水中,所得溶液密度为d g·mL-1 , 该溶液中溶质质量分数为( )
A . 82a/(46a+m)%
B . 8200a/(46a+2m) %
C . 8200a/(46a+m)%
D . 8200a/(69a+m) %
下列说法正确的是( )
A . 石墨转化为金刚石是化学变化
B . 常温下,铁、铝与浓硫酸不发生反应
C . 标准状况下,2.24LNO2中含有的氧原子的数目为0.2NA
D . 向硫酸铵溶液中加入氢氧化钡溶液。发生反应的离子方程式为Ba2++ =BaSO4↓
=BaSO4↓
 =BaSO4↓
=BaSO4↓
关于浓盐酸、浓硝酸、浓硫酸的说法中,正确的是( )
A . 都是含氧酸
B . 都具有氧化性
C . 都盛放在棕色瓶中贮存
D . 室温下都能与金属铝发生钝化反应
以下化学反应的产物与反应条件、反应物的浓度或者用量有关的是( )
A . AlCl3溶液中滴入NaOH溶液
B . Cu与硝酸反应
C . H2与Cl2反应
D . NaHCO3与盐酸反应
最近更新