铝的化学性质 知识点题库
一定量的铝铁合金与300mL 2mol/L的硝酸完全反应,生成3.36L NO(标准状况),三价铁盐和铝盐等,向反应后的溶液中加入3mol/L NaOH溶液恰好使Al3+、Fe3+完全反应并生成沉淀最多,则所加入NaOH溶液的体积是( )
A . 150mL
B . 300 mL
C . 450 mL
D . 600 mL
将1molNa和1molAl的混合物投入足量水中,产生气体在标准状况下的体积为( )
A . 11.2L
B . 22.4L
C . 33.6L
D . 44.8L
某研究性学习小组为了探究“铝的燃烧”,做了如下实验:
-
(1) 甲同学用坩埚钳夹持一小块铝箔(厚约0.1mm),在酒精灯上加热至熔化,轻轻晃动,观察到的现象是,产生该现象的原因是。
-
(2) 乙同学将甲同学的实验方案进行了改进:另取一块铝箔,用砂纸仔细打磨,除去表面的保护膜,再用坩埚钳夹持在酒精灯上加热至熔化,结果观察到的现象与甲仍相同,其原因是 。
-
(3) 丙同学积极改进实验,终于观察到铝在空气中燃烧,他的实验方案是 。
-
(4) 丁同学善于思考,甲、乙两位同学的实验使他领会了为什么铝在空气中能表现出良好的抗腐蚀性,他的解释是
;受丙同学的启发,他又提出了铝燃烧的另一实验方案,结果实验成功,你认为该方案可能是
。
-
(5) 通过本次探究活动,该小组同学一致认为通过 的方法可以观察到可燃物燃烧的现象。
有一种军用烟幕弹中装有ZnO、Al粉和C2Cl6 , 其发烟过程中的化学反应为:①3ZnO+2Al═Al2O3+3Zn ②3Zn+C2Cl6═3ZnCl2+2C
下列有关叙述不正确的是( )
A . 反应①是铝热反应
B . 反应②是置换反应
C . 烟幕是小液滴分散在空气中形成的
D . C2Cl6属于卤代烃
下列关于物质用途的叙述中不正确的是( )
A . 纯碱可用于治疗胃酸过多的药剂
B . 铝制容器可用于常温下贮存、运输浓硫酸
C . 二氧化硅可用于制造光导纤维和石英坩埚
D . 过氧化钠可用作漂白剂和呼吸面具中的供氧剂
下列叙述正确的是( )
A . Na、Al、Fe金属单质在一定条件下与水反应都生成H2和对应的碱
B . 漂白粉和明矾都常用于自来水的处理,二者的作用原理不相同
C . 将SO2通入Ca(ClO)2溶液可生成CaSO3沉淀
D . 向FeCl2溶液中通入Cl2反应的离子方程式为:Fe2++Cl2═Fe3++2Cl﹣
将一固体粉末含有SiO2、Fe2O3、Al2O3 , 加入足量NaOH溶液充分反应后,过滤,向所得溶液中加入过量盐酸,过滤,将所得滤渣洗涤并灼烧至恒重,最终固体成分为( )
A . SiO2
B . Fe2O3、SiO2
C . SiO2、Al2O3
D . Fe2O3
取两块铝片,第一份与足量盐酸反应,第二份与足量烧碱溶液反应,在相同状况下产生相同体积的气体,则两份铝片的质量相比较( )
A . 前者大
B . 后者大
C . 二者相等
D . 无法确定
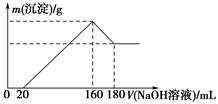
将一定质量的镁铝合金投入100 mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为5 mol/L的NaOH溶液,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。
-
(1) 加入NaOH溶液0~20 mL时的反应的离子方程式为,160~180 mL时的反应的离子方程式为。
-
(2) 合金中Mg的质量为g,所用HCl的物质的量浓度为mol/L。
下列有关金属及其化合物的说法中,正确的个数为( )
①在人类对金属材料的使用过程中,性质活泼的金属单质最早被人们冶炼和使用
②纯铁比生铁抗腐蚀性更强
③单质铝在空气中比较耐腐蚀,所以铝是不活泼金属
④向紫色石蕊试液中加入过量的Na2O2粉末,振荡,溶液变为蓝色并有气泡产生
⑤青铜、不锈钢、硬铝都是合金
⑥可通过焰色反应区分钾元素和钠元素
⑦将FeCl3溶液滴入KI-淀粉溶液中,溶液变蓝色
⑧铝粉和氧化镁粉末混合,高温能发生铝热反应
A . 4
B . 5
C . 6
D . 7
既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
A . 金属铁
B . 金属铜
C . 金属钠
D . 金属铝
相同质量的两份铝分别放入足量的盐酸和氢氧化钠溶液中充分反应,消耗的氯化氢和氢氧化钠的物质的量之比为 ( )
A . 1:1
B . 1:6
C . 2:3
D . 3:1
为分离废磷酸亚铁锂电池的正极材料(主要含LiFePO4和铝箔)中的金属,将正极材料粉碎后进行如下流程所示的转化:
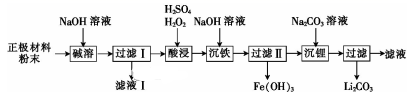
已知LiFePO4不溶于水和碱,能溶于强酸。
-
(1) “碱溶”时的离子方程式为。
-
(2) 向滤液Ⅰ中通入过量CO2会析出Al(OH)3沉淀,写出该反应的离子方程式:。
-
(3) “酸浸”时溶液中Fe2+发生反应的离子方程式为。
-
(4) 检验“沉铁”后所得溶液中是否存在Fe3+的方法是。
-
(5) 以Fe(OH)3为原料可以制取FeSO4晶体,还需的试剂有。
-
(6) “沉锂”时,检验Li+是否沉淀完全的方法是。
下列关于钠、铝的叙述错误的是( )
A . 金属钠和氧气反应,条件不同,产物不同
B . 大量的钠着火时可以用水扑灭,少量的钠应保存在煤油中
C . 钠的密度比水小,熔点低于100℃,在氧气中燃烧时火焰呈黄色
D . 铝在空气中加热时,熔化的铝不能滴落,原因是氧化铝熔点高
由下列实验操作和现象可得出结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向Co2O3中滴入浓盐酸 | 产生黄绿色气体 | 氧化性:Cl2>Co2O3 |
| B | 白铁皮(镀锌铁)出现刮痕后浸泡在饱和食盐水中,一段时间后入几滴K3[Fe(CN)6]溶液 | 无明显现象 | 该过程未发生氧化还原反应 |
| C | 用坩埚钳夹住一小块用砂纸打磨过的铝箔,在酒精灯上加热 | 铝箔熔化并滴落 | 金属铝的熔点较低 |
| D | 将10mL2mol·L-1的KI溶液与1mL1mol·L-1FeCl3溶液混合充分反应后滴加KSCN溶液 | 溶液颜色变红 | KI与FeCl3反应有可逆性 |
A . A
B . B
C . C
D . D
下列说法不正确的是( )
A . 硅酸钠是一种难溶于水的硅酸盐
B . 镁在空气中燃烧可生成氧化镁和氮化镁
C . 钠与水反应生成氢氧化钠和氢气
D . 常温下,铝遇浓硝酸或浓硫酸时会发生钝化
下列化学反应的叙述正确的是( )
A . 铁粉与Al2O3可发生铝热反应
B . AlCl3与过量氨水生成偏铝酸铵
C . 常温下Al在稀硝酸中可发生钝化
D . 电解熔融Al2O3可制金属铝
北京冬奥会火种灯的外形设计灵感来自于河北博物院的“长信宫灯”。

下列说法错误的是( )
A . 青铜的硬度大于纯铜
B . 镏金层破损后生成铜锈的主要成分为CuO
C . 铝合金表面氧化物薄膜可以保护内部金属不被腐蚀
D . 两灯所用的燃料充分燃烧后的产物均为CO2和H2O
下列有关铝及其化合物的说法错误的是( )
A . 铁易生锈,而铝在空气中较稳定,所以铁比铝活泼
B . 可用铝壶烧开水,不可用其长期存放食醋、碱水
C . 氧化铝是一种较好的耐火材料,但不可用氧化铝坩埚熔化NaOH
D . Al2O3能跟强酸、强碱溶液反应生成盐和水,所以它是两性氧化物
在给定条件下,下列选项所示的物质间转化均能一步实现的是( )
A .  B .
B . 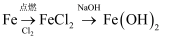 C .
C .  D .
D . 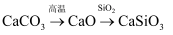
 B .
B . 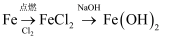 C .
C .  D .
D . 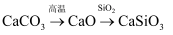
最近更新



