高中 化学
 B .
B .  C .
C .  D .
D . 
 、Ba2+、Na+、H+、SO
、Ba2+、Na+、H+、SO  、NO
、NO  、OH﹣、HCO
、OH﹣、HCO  .将这四种溶液分别标记为A、B、C、D,进行如下实验:
.将这四种溶液分别标记为A、B、C、D,进行如下实验: ①C溶液滴入另外三种溶液中,均无明显现象;
②D和B反应生成的气体能被A吸收;
③A和D反应生成的气体能被B吸收.
试回答下列问题:
-
(1) D的化学式是,判断理由是.
-
(2) 写出其余几种物质的化学式:A,B,C.
-
(3) 写出实验②中有关反应的离子方程式.
-
(4) 写出实验③中有关反应的离子方程式:.
①有色玻璃 ②淀粉溶液 ③硫酸钠溶液 ④云、雾 ⑤Fe(OH)3悬浊液
下列有关说法正确的是( )
A.丙烯的结构简式为CH2CHCH3
B.新戊烷的一氯代物有2种
C.分子式为CH4O和C2H6O的物质一定互为同系物
D.键线式为![]() 的有机物的分子式为C8H8
的有机物的分子式为C8H8
三效催化剂是最为常见的汽车尾气催化剂,其催化剂表面物质转化的关系如图所示,下列说法正确的是
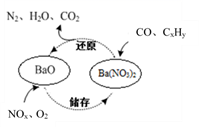
A.在转化过程中,氮元素均被还原
B.依据图示判断催化剂不参与储存和还原过程
C.还原过程中生成0.1mol N2,转移电子数为0.5 mol
D.三效催化剂能有效实现汽车尾气中CO、CxHy、NOx三种成分的净化
下列离子方程式与所述事实相符且正确的是 ( )
A.向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:
2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
B.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:
3ClO—+Fe(OH)3= FeO42—+3Cl—+H2O+H+
C.向NaAlO2溶液中通入过量CO2制Al(OH)3: AlO2-+CO2+2H2O= Al(OH)3↓+HCO3-
D.向含有a mol FeBr2的溶液中,通入x mol Cl2。若x=a,则反应的离子方程式为:
2Fe2++ 2Br-+ 2Cl2=Br2 + 2Fe3++ 4Cl-
下图为常温下向10mL0.1 mol·L-1 NH3·H2O中加入等浓度的盐酸时,NH3·H2O的物质的量随V(盐酸)的变化曲线。(电离度为已电离的NH3•H2O占初始时NH3•H2O的百分比),下列说法正确的是( )

A.测得a点时溶液的pH=11,则NH3·H2O的电离度为1%
B.b点时溶液的pH=7
C.水的电离程度:b<c
D.c点时溶液中存在关系式:2c(Cl-)=c(NH4+) +c(NH3•H2O)
下列说法正确的是( )
A.石油裂解可以得到氯乙烯
B.煤液化可得到焦炭、煤焦油、焦炉气等
C.为了提高轻质液体燃料油(汽油等)的产量和质量,在石油工业上采用的主要方法是催化裂化
D.煤可与水蒸气反应制成水煤气,水煤气的主要成分是CO和CH4
下列关于反应速率的说法正确的是
A.对于任意化学反应,其他条件不变时,增大压强都一定能加快化学反应速率
B.相同条件下,大小相等的铝片与浓硫酸反应比与稀硫酸反应放出氢气的速率大
C.可逆反应达到化学平衡状态时,正、逆反应的速率相等且都为0
D.反应速率用于衡量化学反应进行的快慢,决定反应速率的主要因素是反应物性质
NH3是一种重要的化工原料,可以制备一系列物质(见图)。下列说法正确的是( )
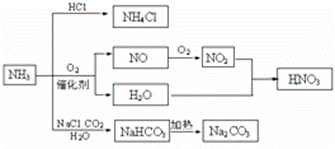
A、NH4Cl和NaHCO3都是常用的化肥 B、NH4Cl、HNO3和Na2CO3受热时都易分解
C、NH3和NO2在一定条件下可发生氧化还原反应 D、图中所涉及的盐类物质都属于正盐
.根据下列化学方程式:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O、2FeCl2+Cl2=2FeCl3、2FeCl3+2KI=2FeCl2+2KCl+I2,判断各物质氧化性由大到小的顺序正确的是
A.I2>Cl2>FeCl3>KMnO4 B.KMnO4 >Cl![]() 2>FeCl3>I2
2>FeCl3>I2
C.Cl2>I2>FeCl3>KMnO4 D.FeCl3>KMnO4>Cl2>I2
下列有关物质分类的说法中,正确的是( )
A. SiO2不能和水反应,所以它不是酸性氧化物 B. 只由一种元素组成的物质必然是纯净物
C. 烧碱、冰醋酸、石墨均为电解质 D. 海水、氯水、氨水均为混合物
A. NH4HCO3受热易分解,可用作化肥
B. 稀硫酸具有酸性,可用于除去铁锈
C. SO2具有氧化性,可用于纸浆漂白
D. Al2O3具有两性,可用于电解冶炼铝



