2018-2019年高二上册期末考试化学题开卷有益(重庆市江津中学、合川中学等七校)
| 1. 选择题 | 详细信息 |
|
化学与生活生产密切相关。下列说法中,不正确的是 A. 将海水直接电解可获得 Mg及Cl2等单质 B. 把石灰浆喷涂在树干上可消灭树皮上的过冬虫卵 C. 施用适量石膏可降低盐碱地(含较多NaCl、Na2CO3)的碱性 D. 施肥时,铵态氮肥不能与草木灰(含K2CO3)混合使用 |
|
| 2. 选择题 | 详细信息 |
|
可用来鉴别2-丁烯、四氯化碳、苯的物质或方法是( ) A. 水 B. 液溴 C. 溴水 D. 硝化反应 |
|
| 3. 选择题 | 详细信息 |
|
在密闭容器中A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示。已知v(A)、v(B)、v(C)之间有以下关系:2v(A)=3v(B),v(C)=2v(B),则此反应可表示为( ) A. 3A+2B=4C B. 2A+3B=6C C. 3A+2B=C D. 2A+3B=4C |
|
| 4. 选择题 | 详细信息 |
|
下列说法正确的是( ) A. 碳酸氢钠在水溶液中的电离方程式为:NaHCO3 = Na+ + H+ + CO32- B. 可溶性盐在水中完全电离是强电解质,难溶性盐在水中溶解度很小是弱电解质 C. 强电解质的水溶液导电性不一定强于弱电解质的水溶液 D. 强电解质都是离子化合物,在水溶液或熔融状态下完全电离,以离子形式存在 |
|
| 5. 选择题 | 详细信息 |
|
下列说法不能够用勒夏特勒原理来解释的是 A. 实验室用排饱和食盐水的方法收集氯气 B. 溴水中有下列平衡Br2+H2O C. SO2催化氧化制SO3的过程中使用过量的氧气,以提高二氧化硫的转化率 D. 恒温、恒压条件下,在2NO2 |
|
| 6. 选择题 | 详细信息 |
|
为了减缓锌和一定浓度盐酸的反应速率,而又不减少产生氢气的量,向盐酸中加入下列物质或措施可行的是( ) A. 升温 B. NaF溶液 C. NaNO3溶液 D. 几滴CuSO4溶液 |
|
| 7. 选择题 | 详细信息 |
|
下列实验装置图正确的是() A. 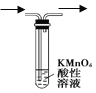 除去甲烷中混有的乙烯 除去甲烷中混有的乙烯B.  石油分馏 石油分馏C.  实验室制硝基苯 实验室制硝基苯D.  实验室制乙炔并检验乙炔 实验室制乙炔并检验乙炔 |
|
| 8. 选择题 | 详细信息 |
|
在初始温度为500 ℃的绝热恒容密闭容器中,充入1 mol HI发生如下反应:2HI(g) A. HI的生成速率是I2 消耗速率的2倍 B. 平衡常数不再改变 C. 气体密度不再改变 D. 容器内气体质量不再改变 |
|
| 9. 选择题 | 详细信息 | ||||||||||||
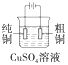
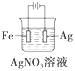
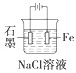
下列有关电化学装置完全正确的是( )
|
|||||||||||||
| 10. 选择题 | 详细信息 |
|
向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资料得知:Ag++2NH3·H2O A. 浊液中存在沉淀溶解平衡:AgCl(s) B. 实验表明实验室可用氨水洗涤附着有银的试管 C. 由实验可以判断K[Ag(NH3)2+]>KSP(AgCl) D. 由资料信息可推知:加浓硝酸后生成的沉淀为AgCl |
|
| 11. 选择题 | 详细信息 |
|
漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:5HClO2===4ClO2↑+H++Cl-+2H2O。(HClO2为弱酸)向NaClO2溶液中滴加H2SO4,开始时HClO2分解反应缓慢,随后反应迅速加快,其原因是( ) A. 溶液中的H+起催化作用 B. 在酸性条件下,亚氯酸钠的氧化性增强 C. ClO2逸出,使反应的生成物浓度降低 D. 溶液中的Cl-起催化作用 |
|
| 12. 选择题 | 详细信息 | |||||||||||||||
将0.2 mol·L-1的KI溶液和0.05 mol·L-1Fe2(SO4)3溶液等体积混合后,取混合液分别完成下列实验,能说明溶液中存在化学平衡“2Fe3++2I-
|
||||||||||||||||
| 13. 选择题 | 详细信息 |
全钒液流储能电池一次性充电后,续航能力可达1000 km,而充电时间只需3~5 min,被誉为“完美电池”,其原理如图所示(已知V2+呈紫色,V3+呈绿色)。电池放电时,左槽溶液质量增加。下列说法正确的是( ) A. 放电时的正极反应为V3++e-=V2+ B. 放电过程中,右槽溶液由紫色变为绿色 C. 充电时的电流方向由B电极流向A电极 D. 充电时的阴极反应为VO2++2H++e-=VO2++H2O |
|
| 14. 选择题 | 详细信息 |
|
下列有关烃类物质的说法正确的是( ) A. 石油通过减压分馏可以得到相对分子量较大的芳香烃 B. 丙烯与溴的四氯化碳溶液反应生成1,3-二溴丙烷 C. D. |
|
| 15. 选择题 | 详细信息 |
常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器里,分别充有二氧化氮和空气,现分别进行下列两上实验:(N2O4 (a)将两容器置于沸水中加热方 (b)在活塞上都加2 kg的砝码 在以上两情况下,甲和乙容器的体积大小的比较,正确的是 A.(a)甲>乙(b)甲<乙 B.(a)甲>乙(b)甲=乙 C.(a)甲<乙(b)甲>乙 D.(a)甲>乙(b)甲>乙 |
|
| 16. 选择题 | 详细信息 |
25 ℃时,不同酸性条件下的0.1 mol·L-1 HF溶液中,c(HF)、c(F-)与溶液pH的变化关系如图所示。下列说法正确的是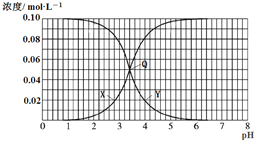 A. 随着溶液pH增大, B. 由水电离出的c(H+):Q>X=Y C. HF的电离常数Ka=1.0×10-3.2 D. 0.1 mol/L NaF溶液的pH约为8.2 |
|
| 17. 综合题 | 详细信息 |
下图是石蜡油在炽热碎瓷片的作用下分解产生某种气体,并验证其性质的装置: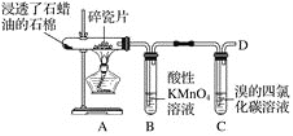 回答下列问题: (1)该气体可以衡量一个国家的石油化工生产水平,该气体的结构简式是___________。发生聚合反应的化学方程式_____________________________________。 (2)B中酸性高锰酸钾溶液和C中溴的四氯化碳溶液都褪色,说明该气体能被酸性高锰酸钾______。在C中发生的化学反应方程式为______________,反应类型为_________。 (3)该气体通过一系列反应可以得到乙炔,写出实验室制取乙炔的化学方程式:______________________________________。 (4)由乙炔可以制取甲苯,甲苯一溴代物的同分异构体有________种,其中对溴甲苯的结构简式为__________________。 (5)甲苯可用于制造烈性炸药TNT,该反应的化学方程式为______________________。 |
|
| 18. 综合题 | 详细信息 |
|
Ⅰ.通过传感器可以监测空气中甲醛的含量。该传感器的原理 如图所示:  (1)该装置的主要能量转化形式是_______________。b为______极,发生的电极反应式为_________________。 (2)在传感器工作过程中,电解质溶液硫酸的浓度___________(填“增大”“减小”“不变”)。当电路中转移0.2 mol电子时,传感器内参加反应的HCHO为_______g。 Ⅱ.用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾(电解槽内的阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过)。  (1)该电解槽的阴极发生_____反应(填“氧化”“还原”)。 (2)制得的硫酸溶液从出口_______(填“A”、“D”)导出,并简述原因________________________________________________(请用化学用语和文字解释)。 |
|
| 19. 综合题 | 详细信息 |
|
家用氯漂白剂的有效成分是NaClO,除用于漂白衣物、消除污渍外,在食品加工中也广泛应用。 Ⅰ.(1)常温下,一定浓度次氯酸钠水溶液的pH=a,则a______7(填>、<或=);结合离子方程式解释其原因是__________________________________________________,此时,溶液中由水电离出的c(OH-)=________mol/L。 (2)漂白剂与酸混合后效果更佳,将0.1000mol/L NaClO溶液与0.1000mol/L 硫酸溶液等体积混合后,关于所得溶液的以下分析正确的是____________(忽略HClO的分解;HSO4-的电离视为完全)。 A.c(HClO)+c(ClO-)=0.1000mol/L B.c(H+)>c(Na+)=c(SO42-)>c(HClO)>c(ClO-)>c(OH-) C.c(Na+)+c(H+)=c(SO42-)+c(ClO-)+c(OH-) D.c(H+)-c(OH-)=2c(ClO-)+c(HClO) Ⅱ.取20.00g家用氯漂白剂溶液配制成100mL溶液,取出10mL,加入过量KI处理,用足量稀硫酸酸化,然后立即用0.1000mol/L Na2S2O3溶液滴定生成的I2(2Na2S2O3+I2=2I-+Na2S4O6),指示剂显示滴定终点时,消耗Na2S2O3溶液30.00 mL; (1)用KI处理漂白剂生成I2的离子方程式为________________________________。 (2)该滴定过程选用的指示剂通常为___________,判断滴定终点时的现象是___________________________________________________________________________。 (3)该漂白剂中“有效氯”的含量为_________________(结果保留一位小数)。若滴定结束时,发现滴定管尖嘴部分有气泡,则测定结果________(填“偏高”“偏低”“无影响”)。 注:“有效氯”指每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。 |
|
| 20. 综合题 | 详细信息 | ||||||||||||||||
|
Ⅰ.利用测压法在刚性反应器中研究 T℃ 时: 3NO2(g)
|
|||||||||||||||||
- 2018-2019年高二上学期12月考试化学考题(云南省元江哈尼族彝族傣族自治县一中)
- 淮安市高一化学下册开学考试刷题练习
- 长春实验中学2019年高一化学上学期月考测验附答案与解析
- 广西壮族自治区桂林市崇左市防城港市2020届高三联合模拟考试理科综合化学在线考试题免费练习
- 山东省临朐县实验中学2020-2021年高二上半期12月月结学情检测化学题带参考答案
- 专题3.1 金属及其化合物(综合提升卷)--巅峰冲刺高三化学上册专题练习刷题训练
- 西藏自治区日喀则市第二高级中学2020-2021年高二上半期期中考试化学试卷在线练习
- 2019-2020年高一11月月考化学题开卷有益(河北省宣化市第一中学)