2018四川高一上学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
化学与科学、技术、社会、环境密切相关,下列有关说法中错误的( ) A.春节燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 B.为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰 C.小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂 D.青铜是我国使用最早的合金材料,目前世界上使用量最大的合金材料是钢铁
|
|
| 2. | 详细信息 |
|
制印刷电路时常用氯化铁溶液作为“腐蚀液”,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是: A. 烧杯中有铜无铁 B. 烧杯中有铁无铜
|
|
| 3. | 详细信息 |
|
含HCO3-、Cl-、Na+、CO32-等离子的溶液中,加入适量Na2O2后,离子浓度基本保持不变的是(设溶液体积不变): A. Cl- B. Na+ C. HCO3- D. CO32-
|
|
| 4. | 详细信息 |
|
能正确表示下列反应的离子方程式是: A.硫酸铁与氢氧化钡溶液反应 Ba2++SO42-=BaSO4? B.钾和水反应 K+2H2O =K++2OH-+H2? C.小苏打与烧碱溶液反应 HCO3-+OH-=CO32-+H2O D.苏打与盐酸反应 HCO3-+H+ =CO2?+H2O
|
|
| 5. | 详细信息 |
|
根据下列反应,推断盐酸应当具有的性质是: ①Zn+2HCl=ZnCl2+H2? ②2HCl+CuO=CuCl2+H2O ③MnO2+4HCl A.只有酸性 B.只有氧化性 C.只有还原性 D.有酸性、有氧化性和还原性
|
|
| 6. | 详细信息 |
|
若在加入铝粉能放出氢气的溶液中,分别加入下列各组离子,可能共存的是: A NH4+、NO3-、CO32-、Na+ B Na+、Ba2+、HCO3-、AlO2- C NO3-、Mg 2+、K+、CH3COO D NO3-、K+、AlO2-、OH
|
|
| 7. | 详细信息 |
|
下列有关元素及其化合物的说法正确的是( ) A.Al(OH)3 具有两性,所以不能用于中和胃酸 B.FeCl3 既能通过化合反应制得,也能通过金属与酸的置换反应制得 C.Na 在空气中长期放置最终变为 Na2CO3 粉末 D.等质量NaHCO3和Na2CO3分别与足量盐酸反应,生成的CO2在同温同 压下体积相同
|
|
| 8. | 详细信息 |
|
下列有关元素及其化合物的说法正确的是( ) A.将水蒸气通过灼热的铁粉,粉末变为红棕色 B.Al2O3熔点高,可用作耐高温材料 C.无水CuSO4 可用于干燥实验室制备的氢气 D.制备Fe(OH)2时,为了隔绝空气可以向FeSO4溶液加少量的酒精
|
|
| 9. | 详细信息 |
|
将一定量的CO2 通入下列溶液中: ①BaCl2溶液 ②澄清的石灰水 ③饱和Na2CO3溶液 ④K2SiO3溶液; 可能变浑浊的是: A. ①② B. ①②③ C. ①②③④ D.②③④
|
|
| 10. | 详细信息 |
|
下列说法:①硅的化学性质很稳定,因此硅在自然界中以游离态形式存在;②硅和二氧化硅晶体都是由原子构成的;③二氧化硅和二氧化碳在物理性质上有很大的差异;④二氧化硅是一种酸性氧化物,它不与任何酸发生反应。正确的是: A. ①②③④ B. ①②④ C. ①④ D. ②③
|
|
| 11. | 详细信息 |
|
宋代著名法医学家宋慈的《洗冤集录》中有“ A.X的化学式为AgS B.银针验毒时,空气中氧气失去电子 C.反应中Ag和H2S均是还原剂 D.每生成1mo
|
|
| 12. | 详细信息 |
|
下列各组中的两物质作用时,反应条件(温度、反应物用量比)改变,不会引起产物的种类改变的是: A.Na和O2 B.NaOH和CO2 C.Na2O2和CO2 D.NaHCO3和Ca(OH)2
|
|
| 13. | 详细信息 |
|
己知在碱性溶液中可发生如下反应:2R(OH)3 + 3C1O-+ 4OH- = 2RO4n-+3Cl- +5H2O。关于该反应的说法正确的是( ) A.RO4n-中 R 的化合价是+6 B.ClO-是还原剂 C.由上述离子方程式可知,该反应是由氨水提供的碱性环境 D.反应过程中生成1m
|
|
| 14. | 详细信息 |
|
.用焰色反应检验K+离子时的操作步骤有:①蘸取待测液,②置于酒精灯火焰上灼烧,③透过蓝色钴玻璃观察,④用稀盐酸洗净铂丝。其中正确的操作顺序为: A.①②③④ B. ④②①②③ C.②①②③④
|
|
| 15. | 详细信息 |
|
自来水可用氯气消毒。某学生用自来水配制下列物质的溶液: ①AgNO3 ②FeBr2 ③烧碱 ④Na2CO3 ⑤Na2S ⑥CaCl2 会引起药品变质的是: A.除②⑤③外 B.④⑤⑥ C.①②③⑥ D.除⑥外
|
|
| 16. | 详细信息 | |||||||||||||||||||||||||
|
下表各组物质中,物质之间不可能实现如下图所示转化的是( )
|
||||||||||||||||||||||||||
| 17. | 详细信息 |
|
在一定条件下,下列微粒的还原性顺序为Cl-<Br-<Fe2+<I-<SO2,由此判断以下各反应在溶液中不能发生的是( ) A.2Fe2++I2 B.I2+SO2+2H2O C.2Fe3++SO2+2H2O D.Cl2+2I-
|
|
| 18. | 详细信息 | |||||||||||||||
|
将物质X逐渐加入(或通入)Y溶液中,生成沉淀的量与加入X的物质的量关系如图所示,符合图示情况的是( )
|
||||||||||||||||
| 19. | 详细信息 |
|
含氯化镁和氯化铝的200 mL混合溶液中,c(Mg2+)为0.2 mol·L-1,c(Cl-)为1.3 mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4 mol·L-1 NaOH溶液的体积为: A.40 mL B.72 mL C.80 mL D.128 mL
|
|
| 20. | 详细信息 |
|
Fe和Fe2O3的混合物,加入200mL 5mol·L-1的盐酸,恰好完全溶解,再向其中加入KSCN溶液,未见血红色,则所得溶液中Fe2+的物质的量浓度为(假设反应后溶液 A、2.5mol·L-1 B、l mol·L-1 C、2mol·L-1 D、5mol·L-1
|
|
| 21. | 详细信息 | ||||||||||||||||||
|
选择合适的药品,把下列物质中含有的少量杂质(括号内为杂质)除去,写出所需的药品和有关的离子方程式。
|
|||||||||||||||||||
| 22. | 详细信息 |
|
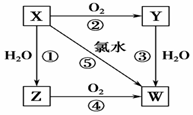
已知X气体是一种无色有刺激性气味的酸性氧化物,有关X、Y、Z、W的转
(1)Y的化学式为________,Z的化学式为________。X直接排入空气中易造成的环境问题是________。 (2)反应①~⑤中属于可逆反应的是________,属于氧化还原反应的是________。 (3)写出反应⑤的化学方程式:___________________________________________。
|
|
| 23. | 详细信息 |
|
向BaCl2 (1)若不考虑SO2与水的反应,向BaCl2溶液中通入SO2无明显现象,“ 原因是________________________________________________________________。 (2)沉淀A的化学式为____________,该沉淀能否溶于稀盐酸?____________。 (3)写出生成沉淀B的离子方程式:__________________________________________。 (4)生成2.33 g沉淀B,需消耗标准状况下的Cl2的体积为________mL。
|
|
| 24. | 详细信息 |
|
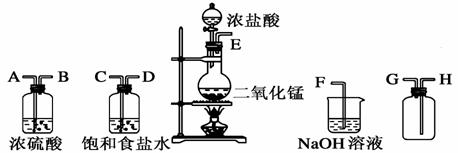
在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如下图:
(1)连接上述仪器的正确顺序(填各接口处的字母):____接____;____接____;____接____;____接____。 (2)装置中,饱和食盐水的作用是_________;NaOH溶液的作用是________。 (3)化学实验中常用湿润的淀粉-KI试纸检验是否有Cl2产生。如果有Cl2产生,可观察到________________,反应方程式______________________________。 (4)写出下列化学反应的方程式: ①气体发生装置进行的反应:__________________________________。 ②NaOH溶液中发生的反应:___________________________________。 (5)KMnO4的氧化性比MnO2强得多,实验室也可以用KMnO4固体和浓盐酸反应制取氯气,反应如右:2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2?+8H2O。 ①请标出电子转移的方向和 ②该反应中被氧化和未被氧化的HCl的物质的量之比是________,如果将20 mL、12 mol·L-1的浓盐酸与足量KMnO4充分反应,实际能收集到的氯气在标准状况下的体积将________。 A.=1.68 L B.>1.68
|
|