高中 化学
 ,已知该反应在不同温度下的平衡常数如下表,下列说法错误的是( )
,已知该反应在不同温度下的平衡常数如下表,下列说法错误的是( ) | 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
 B . 该反应的平衡常数表达式是
B . 该反应的平衡常数表达式是  C . 其他条件不变,向平衡体系充入
C . 其他条件不变,向平衡体系充入  气体,K值减小
D . 其他条件不变,升高温度时,
气体,K值减小
D . 其他条件不变,升高温度时,  的平衡转化率降低
的平衡转化率降低
-
(1) 下列关于实验的叙述正确的有(填序号).
①在气体发生装置上直接点燃一氧化碳气体时,必需要先检验一氧化碳气体的纯度.最简单的方法是用排空气的方法先收集一试管气体,点燃气体,听爆鸣声.
②配制稀硫酸时,可先在烧杯中加一定体积的水,再边搅拌边加入浓硫酸
③实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室
-
(2) 在容量瓶的使用方法中,下列操作不正确的是(填写编号) .A . 使用容量瓶前检查它是否漏水 B . 容量瓶用蒸馏水洗净后,再用待配溶液润洗 C . 配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近容量瓶刻度标线1cm~2cm处,用滴管滴加蒸馏水到刻度线 D . 定容后,盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次
-
(3) 粗盐经提纯后得到NaCl溶液,再经蒸发、结晶、烘干得精盐.
①蒸发操作中使用到的瓷质仪器的名称为.
②该同学将所得精盐配成溶液,用于另一实验.实验中需要用80mL,1mol/L的NaCl溶液,配制过程中用托盘天平称取的精盐质量为g,用于定容的玻璃仪器的规格和名称.
-
(4) 用6mol•L﹣1的硫酸配制100mL1.0mol•L﹣1硫酸,若实验仪器有:
A.100mL量筒 B.托盘天平 C.玻璃棒 D.50mL容量瓶 E.20mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
完成上述实验时应选用的仪器是(填入字母编号).
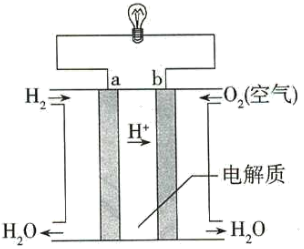
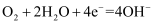 C . 电子由a通过灯泡流向b
D . 氢氧燃料电池是环保电池
C . 电子由a通过灯泡流向b
D . 氢氧燃料电池是环保电池
如图某气体X可能由H2、CO、CH4中的一种或几种组成,将X气体充分燃烧,把燃烧后生成的气体通过A、B两个洗气瓶。试回答下列问题。
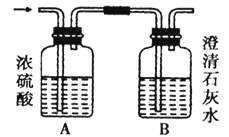
① 若A洗气瓶的质量增加,B洗气瓶的质量不变,则气体X是。
② 若A洗气瓶的质量不变,B洗气瓶的质量增加,则气体X是。
③ 若A、B两个洗气瓶的质量都增加,则气体X可能是。
Ⅰ. 

Ⅱ. 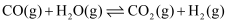

Ⅲ. 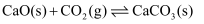

Ⅳ. 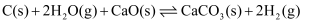

副反应:
Ⅴ. 

Ⅵ. 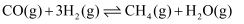
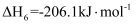
回答下列问题:
-
(1) 已知反应Ⅰ、Ⅱ的平衡常数
 、
、  随温度的变化如图1、图2所示。
随温度的变化如图1、图2所示。 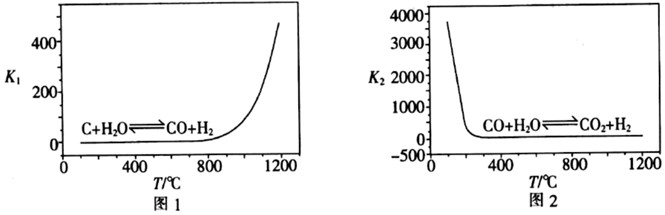
①由反应Ⅴ和反应Ⅵ可知,
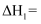 ;反应Ⅰ的
;反应Ⅰ的 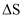 (填“>”或“<”)0。
(填“>”或“<”)0。②温度小于800℃时,
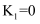 ,原因是。
,原因是。③为提高反应Ⅱ中
 的转化率,可采取的措施是(写一条)。
的转化率,可采取的措施是(写一条)。④T℃时,向密闭容器中充入1

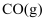 和3
和3 
 ,只发生反应Ⅱ,此时该反应的平衡常数
,只发生反应Ⅱ,此时该反应的平衡常数  ,
,  的平衡转化率为。
的平衡转化率为。 -
(2) 从环境保护角度分析,该制氢工艺中设计反应Ⅲ的优点是。
-
(3) 起始时在气化炉中加入1
 C、2
C、2 
 及1
及1 
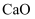 ,在2.5
,在2.5  下,气体的组成与温度的关系如图3所示。
下,气体的组成与温度的关系如图3所示。 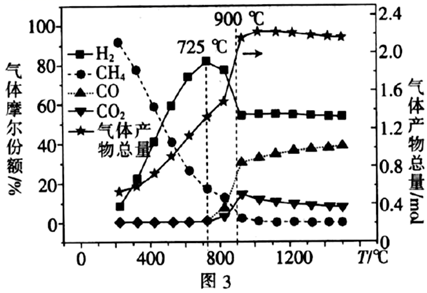
①200~725℃时,
 的量不断减少的原因是。
的量不断减少的原因是。②725~900℃时,
 的物质的量分数快速减小,其原因是。
的物质的量分数快速减小,其原因是。
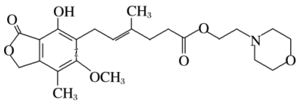 ,则下列关于MMF的说法中,错误的是( )
,则下列关于MMF的说法中,错误的是( ) ①MMF所有原子一定处在同一平面;②可以跟溴水加成;③可以被酸性KMnO4溶液氧化;④可以跟NaHCO3溶液反应;⑤MMF的分子式为C24H31O7N;⑥可以发生消去反应;⑦可以发生加聚反应;⑧可以发生水解反应;⑨可以发生取代反应
碳酸钙受热分解的方程式为CaCO3(S)![]() CaO(S)+CO2(g)在一固定容积的密闭容器中进行该反应,达到平衡后,二氧化碳的浓度为a mol·L-l ,保持温度不变,再通入一定量的二氧化碳气体,平衡后,体系中二氧化碳的浓度与原平衡相比 ( )
CaO(S)+CO2(g)在一固定容积的密闭容器中进行该反应,达到平衡后,二氧化碳的浓度为a mol·L-l ,保持温度不变,再通入一定量的二氧化碳气体,平衡后,体系中二氧化碳的浓度与原平衡相比 ( )
A. 增大 B. 减小 C. 不变 D. 无法判断
下列关于金属的一些说法不正确的是( )
A.工业上金属Mg、Cu都是用热还原法制得的
B. 合金的性质与其成分金属的性质不完全相同
C.银质器皿日久表面会逐渐变黑是由于生成了Ag2S
D.Al2O3、MgO可用耐作高温材料
下列说法正确的是
A . 糖类、蛋白质均属于天然有机高分子化合物
B . 粉末在空气中受热,迅速被氧化成
C . 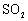
D . 镀锌铁皮的镀层破损后,铁皮会加速腐蚀
(1)油酸的化学式为C17H33COOH,结构中含有 两种官能团,通过实验检验
两种官能团,通过实验检验![]() 的方法是________________________,
的方法是________________________,
检验—COOH的方法是_________________________________________。
(2)一种油脂1.768 g完全催化加氢,需标准状况下氢气134.4 mL,同物质的量的该油脂氢化后,皂化消耗NaOH 0.24 g,若该油脂是简单甘油酯,写出它的结构简式:___________________________________。
碲(Te)广泛用于彩色玻璃和陶瓷。工业上用精炼铜的阳极泥(主要含有TeO2、少量Ag、Au)为原料制备单质碲的一种工艺流程如下:

已知TeO2微溶于水,易溶于较浓的强酸和强碱。
(1)“碱浸”时发生反应的离子方程式为_________________。
(2)碱浸后的“滤渣”可以部分溶于稀硝酸,发生反应的化学方程式是_______________。
(3)“沉碲”时控制溶液的pH为4.5~5.0,生成TeO2沉淀。酸性不能过强,其原因是______________;防止局部酸度过大的操作方法是___________________。
(4)“酸溶”后,将SO2通入TeCl4酸性溶液中进行“还原”得到碲,该反应的化学方程式是_____________。
(5)25℃时,亚碲酸(H2TeO3)的Ka1=1×10-3,Ka2=2×10-8。
①0.1mol·L-1 H2TeO3的电离度α约为_____。(α=![]() ×100%)
×100%)
②0.1mol·L-1的NaHTeO3溶液中,下列粒子的物质的量浓度关系正确的是
A.c(Na+)>c(![]() )>c(OH-)>c(H2TeO3)>c(H+)
)>c(OH-)>c(H2TeO3)>c(H+)
B.c(Na+)+c(H+)=c(![]() )+c(
)+c(![]() )+c(OH一)
)+c(OH一)
C.c(Na+)=c(![]() )+c(
)+c(![]() )+c(H2TeO3)
)+c(H2TeO3)
D.c(H+)+c(H2TeO3)=c(OH-)+c(![]() )
)
“心得安”是治疗心脏病的药物,下面是它的一种合成路线(具体反应条件和部分试剂略)。
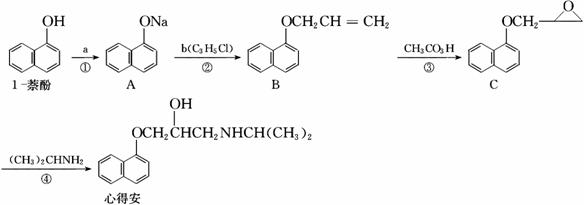
回答下列问题:
(1)试剂b的名称(系统命名法)是_________,B中官能团的名称是_________________。
(2)反应③的类型是反应_____________________。
(3)试剂b可由丙烷经三步反应合成:
![]()
反应l的试剂与条件为___________________________。X的分子中含有2种氢原子,且所含元素种类与b相同。
反应2的化学方程式为___________________________________________________。
若一次取样,检验X中所含官能团,按使用的先后顺序写出所用试剂化学式:_______________。
(4)芳香化合物D是1-萘酚的同分异构体,其分子中有两个官能团,能发生银镜反应,D分子在核磁共振氢谱图中显示4组吸收峰,则D的结构简式为_________________。
(5)以下关于心得安的说法正确的是_______________。
a.分子式为C16H20O2N
b.通常状况下为固体,易溶于水
c.能使酸性高锰酸钾溶液褪色
d.能发生消去、加成、酯化、氧化反应
已知C(石墨,s) = C(金刚石,s) △H>0,P(白磷,s) = P(红磷,s) △H<0。根据上述信息推论正确的是( )
A.前者为放热反应 B.红磷的能量比白磷低 C.红磷比金刚石稳定 D.上述变化都为物理变化
下列关于各图的叙述中正确的是( )

A.图甲表示l mol H2(g)完全燃烧生成水蒸气吸收241.8 kJ热量
B.图甲表示2 mol H2(g)所具有的能量比2 mol H2O(g)所具有的能量多483.6 kJ
C.图乙表示常温下稀释HA、HB两种酸的图像,得出结论:HA的酸性大于HB的酸性
D.图乙中起始时HA的物质的量浓度大于HB



